利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:
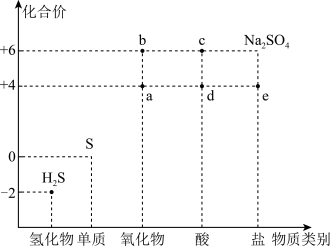
(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)将a排入大气中会引起_______ 。
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是_______ (填化学式)。向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序_______ (填序号)。

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)将a排入大气中会引起
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序
更新时间:2022-04-12 19:37:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。
请回答下列问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: 。
。 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。
(1)物质(甲)为_______ (填化学式)。
(2)反应中若产生5molNO分子,则转移电子的数目是_______ 。
Ⅱ.亚硝酸钠( )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生如下反应:
会使人中毒。已知亚硝酸钠能发生如下反应: 。
。
(3)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为_______ 。
(4)自来水中的 对人类健康会产生危害碱性条件下Al粉还原
对人类健康会产生危害碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。_______
_______Al+_______ +_______
+_______ _______
_______ _______
_______ _______
_______
请回答下列问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 。
。 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。(1)物质(甲)为
(2)反应中若产生5molNO分子,则转移电子的数目是
Ⅱ.亚硝酸钠(
 )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生如下反应:
会使人中毒。已知亚硝酸钠能发生如下反应: 。
。(3)用双线桥法标出该反应中电子转移的方向及数目:
(4)自来水中的
 对人类健康会产生危害碱性条件下Al粉还原
对人类健康会产生危害碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。_______Al+_______
 +_______
+_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
【推荐2】氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角。已知:淀粉遇碘单质(I2)变蓝色。
(1)下列粒子中,只有还原性的是_______ 。
① ②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Na+ ⑦Mg
②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Na+ ⑦Mg
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是_______ (氧化剂或还原剂)。
(3)已知反应:
①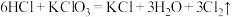
②
③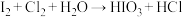 (未配平)
(未配平)
反应①中若有6molHCl参与反应,转移的电子数目为_______ ,对于反应①②③下列说法正确的是_______ 。
A.反应①中氧化剂和还原剂的物质的量之比为1:6
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:
D.氧化性由强到弱顺序:KClO3Cl2I2
(4)反应①是制取Cl2的方法,除此之外反应 也常用来制备Cl2,被氧化的HCl和参加反应的HCl的质量之比为
也常用来制备Cl2,被氧化的HCl和参加反应的HCl的质量之比为_______ 。
(1)下列粒子中,只有还原性的是
①
 ②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Na+ ⑦Mg
②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Na+ ⑦Mg(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是
(3)已知反应:
①
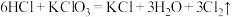
②

③
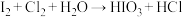 (未配平)
(未配平)反应①中若有6molHCl参与反应,转移的电子数目为
A.反应①中氧化剂和还原剂的物质的量之比为1:6
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:

D.氧化性由强到弱顺序:KClO3Cl2I2
(4)反应①是制取Cl2的方法,除此之外反应
 也常用来制备Cl2,被氧化的HCl和参加反应的HCl的质量之比为
也常用来制备Cl2,被氧化的HCl和参加反应的HCl的质量之比为
您最近一年使用:0次
【推荐3】一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
(2)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 :而中毒的事件,其原因是
:而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。下列也能实现这种转化的物质是___________ (填字母序号)。
A. B.
B. C.
C.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___________ 性。
(4)在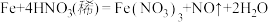 的反应中,
的反应中, 表现了
表现了___________ 性和___________ 性,每有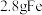 参加反应,转移电子数
参加反应,转移电子数___________ 个;生成的 (标准状况下)体积为
(标准状况下)体积为___________  。
。
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中不是以金属单质的形式存在,而是以
铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐如硫酸亚铁。(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
(2)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 :而中毒的事件,其原因是
:而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有A.
 B.
B. C.
C.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在
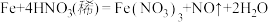 的反应中,
的反应中, 表现了
表现了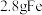 参加反应,转移电子数
参加反应,转移电子数 (标准状况下)体积为
(标准状况下)体积为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】“消洗灵”是一种广谱、高效、低毒的消毒洗涤剂,常应用于宾馆、医院床上用品的洗涤消毒,其化学组成可以表示Na10P3O13Cl·5H2O(磷酸三钠次氯酸钠)。实验室制备装置和过程如图:

已知:①“消洗灵”是一种含氯消毒剂,消毒原理与“84消毒液”相似
②磷酸三钠对金属表面具有一定的保护作用
C中Na3PO4与Na2HPO4的物质的量之比为1:2,则C中反应的化学方程式为_______ 。

已知:①“消洗灵”是一种含氯消毒剂,消毒原理与“84消毒液”相似
②磷酸三钠对金属表面具有一定的保护作用
C中Na3PO4与Na2HPO4的物质的量之比为1:2,则C中反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】H2O2是重要的化学试剂,在实验室和生产实际中应用广泛。
(1)写出H2O2的结构式:________ ,H2O2在MnO2催化下分解的化学方程式:__________ 。
(2) ①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:_______________ 。
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是____________ 。
(3)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:___________________ 。
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在________ (填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是__________________ ;
(4)H2O2是一种二元弱酸,其与过量的Ba(OH)2反应的化学方程式为_____________ 。
(1)写出H2O2的结构式:
(2) ①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
②在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是
(3)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色。
①写出反应的离子方程式:
②实验室常用酸性KMnO4标准液测定溶液中H2O2的浓度,酸性KMnO4溶液应盛放在
(4)H2O2是一种二元弱酸,其与过量的Ba(OH)2反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】近年来,我国对储氢纳米碳管的研究获得了重大进展,电弧法合成的纳米碳管常伴有大量物质——碳纳米颗粒。这种碳纳米颗粒可用氧化法提纯。其反应的化学方程式为:
_______C +_______K2Cr2O7+_______H2SO4(稀)=_____CO2+_______K2SO4+_______Cr2(SO4)3+_______
(1)完成并配平上述反应的化学方程式______ 。
(2)此反应的氧化剂是_______ ,氧化产物是_______ 。
(3)H2SO4在上述反应中表现出来的性质是_______ 。
A.酸性B.氧化性C.吸水性D.脱水性
(4)上述反应中若产生11.2 L(标准状况下)的气体物质,则转移的电子数目为_______ 。
_______C +_______K2Cr2O7+_______H2SO4(稀)=_____CO2+_______K2SO4+_______Cr2(SO4)3+_______
(1)完成并配平上述反应的化学方程式
(2)此反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
A.酸性B.氧化性C.吸水性D.脱水性
(4)上述反应中若产生11.2 L(标准状况下)的气体物质,则转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:

(1)写出Y转化为 的化学方程式
的化学方程式_______ 。
(2)W的溶液与 反应可以生成Y,写出该反应的离子方程式
反应可以生成Y,写出该反应的离子方程式_______ 。
(3)欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是_______ (填序号)。
a. b.
b. c.
c. d.
d.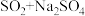
(4)小艾同学预测Y具有还原性,其理论依据是_______ ,将Y通入 溶液中,下列实验事实能够证实Y具有还原性的是
溶液中,下列实验事实能够证实Y具有还原性的是_______ 。
①反应后溶液由黄色变为浅绿色
②取反应后的溶液少许,加入 溶液,产生白色沉淀
溶液,产生白色沉淀
③取反应后的溶液少许,加入 溶液,产生沉淀,加入少量盐酸后沉淀部分溶解。
溶液,产生沉淀,加入少量盐酸后沉淀部分溶解。
(5)Y是有毒性气体,产品含量常用标准酸性高锰酸钾溶液测定,高锰酸钾被还原为 ,试写出该反应的离子方程式
,试写出该反应的离子方程式_______ 。

(1)写出Y转化为
 的化学方程式
的化学方程式(2)W的溶液与
 反应可以生成Y,写出该反应的离子方程式
反应可以生成Y,写出该反应的离子方程式(3)欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是a.
 b.
b. c.
c. d.
d.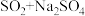
(4)小艾同学预测Y具有还原性,其理论依据是
 溶液中,下列实验事实能够证实Y具有还原性的是
溶液中,下列实验事实能够证实Y具有还原性的是①反应后溶液由黄色变为浅绿色
②取反应后的溶液少许,加入
 溶液,产生白色沉淀
溶液,产生白色沉淀③取反应后的溶液少许,加入
 溶液,产生沉淀,加入少量盐酸后沉淀部分溶解。
溶液,产生沉淀,加入少量盐酸后沉淀部分溶解。(5)Y是有毒性气体,产品含量常用标准酸性高锰酸钾溶液测定,高锰酸钾被还原为
 ,试写出该反应的离子方程式
,试写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用元素的化合价推测物质的性质是化学研究的重要手段。如图所示的是硫元素的常见化合价与部分物质类别的对应关系:

(1)将X与Y混合,可生成黄色固体。该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为________ 。

(1)将X与Y混合,可生成黄色固体。该反应中氧化剂与还原剂的物质的量之比为
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一种由黄铁矿制备硫酸的工艺流程如图:

根据所学知识,回答下列问题:
(1)上述划线的物质中,属于酸性氧化物的是___________ (填化学式)。
(2)写出黄铁矿在空气中焙烧时发生反应的化学方程式:___________ 。
(3)同温同压下,等质量的 气体和
气体和 气体的体积之比
气体的体积之比
___________ ,氧原子数之比
___________ 。
(4)用98%的浓硫酸(密度为 )配制250 mL物质的量浓度为
)配制250 mL物质的量浓度为 的稀硫酸。
的稀硫酸。
①需要量取上述浓硫酸的体积为___________ mL(保留三位有效数字)。
②稀释后的稀硫酸中 为
为___________  。
。
③从稀释好的溶液中取出10 mL,将此10 mL溶液稀释到100 mL,稀释后溶液中
___________  。
。
④下列操作可能使配制的溶液浓度偏低的是___________ (填标号)。
A.移液时,未洗涤烧杯内壁和玻璃棒
B.稀释后未经冷却就移液
C.定容时,俯视容量瓶刻度线
D.容量瓶用蒸馏水洗净后,没烘干就直接使用

根据所学知识,回答下列问题:
(1)上述划线的物质中,属于酸性氧化物的是
(2)写出黄铁矿在空气中焙烧时发生反应的化学方程式:
(3)同温同压下,等质量的
 气体和
气体和 气体的体积之比
气体的体积之比

(4)用98%的浓硫酸(密度为
 )配制250 mL物质的量浓度为
)配制250 mL物质的量浓度为 的稀硫酸。
的稀硫酸。①需要量取上述浓硫酸的体积为
②稀释后的稀硫酸中
 为
为 。
。③从稀释好的溶液中取出10 mL,将此10 mL溶液稀释到100 mL,稀释后溶液中

 。
。④下列操作可能使配制的溶液浓度偏低的是
A.移液时,未洗涤烧杯内壁和玻璃棒
B.稀释后未经冷却就移液
C.定容时,俯视容量瓶刻度线
D.容量瓶用蒸馏水洗净后,没烘干就直接使用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】选用下面的药品和装置验证 H2SO3 和H2CO3 的酸性强弱,其连接顺序:A→_______ (按气流方向用大写字母表示即可)。D装置的主要作用是_______ 。

③根据②中的数据可知,配置相同物质的量浓度的NaHSO3 和NaHCO3 溶液,其pH值大小关系为pH(NaHSO3)_______ pH(NaHCO3 )(填“>”、“<”或“=”)。

③根据②中的数据可知,配置相同物质的量浓度的NaHSO3 和NaHCO3 溶液,其pH值大小关系为pH(NaHSO3)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________ ;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________ (填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________ ;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________ ;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________ 性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______ (填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________ (用离子方程式表示)。
(1)烟气脱硫、脱硝的环境意义是
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3
 7N2+12H2O
7N2+12H2O① 上述反应中被还原的元素是
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3
 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2上述反应中NOx所起的作用是
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的
A.漂白性 B.氧化性
 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】SO2是主要大气污染物之一,其产生和治理是环境科学的主要研究方向。完成下列问题:
(1)SO2和O3是等电子体,有相似的结构质。以下关于O3的描述正确的是___________。(复选,填序号)
(2)SO2与CO2都属于酸性氧化物,以下关于两者比较正确的是___________。(复选,填序号)
(3)SO2能与稀硝酸反应生成NO,写出反应的化学方程式:___________ 。能否说明硝酸的酸性比硫酸强?说明理由___________ 。
(1)SO2和O3是等电子体,有相似的结构质。以下关于O3的描述正确的是___________。(复选,填序号)
| A.空间构型为直线形 | B.属于非电解质 |
| C.具有较强的氧化性 | D.属于极性分子 |
| A.都能使品红褪色 | B.都能使酸性KMnO4溶液褪色 |
| C.都能与Na2CO3反应 | D.都能与NaOH反应 |
您最近一年使用:0次



