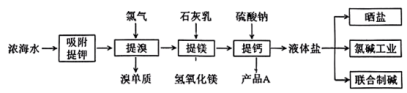
高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:

下列叙述正确的是

下列叙述正确的是
| A.反应I生成物中可能含有Fe2+ |
| B.反应II中Fe3+作氧化剂, |
| C.该生产条件下,物质的溶解性:Na2FeO4>K2FeO4 |
| D.该流程中涉及的化学反应均为氧化还原反应 |
更新时间:2023-02-06 17:56:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于消杀试剂的说法错误的是
| A.体积分数为90%的酒精溶液消毒效果不如75%的好 |
B.工业上将 通入冷的石灰乳中制备“84”消毒液 通入冷的石灰乳中制备“84”消毒液 |
C.臭氧、漂白粉、 都有杀菌消毒的效果 都有杀菌消毒的效果 |
| D.“84”消毒液与洁厕灵(主要成分HCl)混合使用会产生有毒气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列过程与氧化还原反应有关 的是
| A.热的纯碱溶液去除油污 |
B. 溶液和 溶液和 溶液混合,产生刺激性气味气体 溶液混合,产生刺激性气味气体 |
C.铜质地漏生锈变绿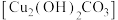 |
D.鸡蛋清溶液在饱和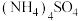 溶液中出现白色浑浊 溶液中出现白色浑浊 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】有关实验的叙述正确的是
| A.电解相同浓度NaOH、H2SO4及NaCl溶液,阴极都产生氢气,阴极区pH都增大 |
| B.少量Cl2通入FeI2溶液中,再滴加少量CCl4,振荡、静置,下层液体为紫色 |
| C.向一定体积的浓硫酸(热)中加入足量铁粉,可用烧碱溶液完全吸收生成的气体 |
| D.检验氯乙烷中的氯元素,加NaOH溶液加热后,用稀硫酸酸化,再加AgNO3溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在室温下,发生下列几种反应:①16H++10Z-+2XO =2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-,根据上述反应,判断下列结论错误的是
=2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-,根据上述反应,判断下列结论错误的是
 =2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-,根据上述反应,判断下列结论错误的是
=2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-,根据上述反应,判断下列结论错误的是| A.还原性强弱顺序为 A2+>B->Z->X2+ |
B.在溶液中可能发生反应:8H++5A2++XO =X2++5A3++4H2O =X2++5A3++4H2O |
C.X2+是 XO 的还原产物,B2是 B-的氧化产物 的还原产物,B2是 B-的氧化产物 |
D.氧化性强弱顺序为 XO >Z2>A3+>B2 >Z2>A3+>B2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室通过对市售85%磷酸溶液进行减压蒸馏除水、结晶除杂得到纯磷酸晶体,实验装置如图。

已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成 (熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。
(熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。
下列实验装置和操作不能 达到实验目的的是

已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成
 (熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。
(熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸。下列实验装置和操作
A.图甲中使用的 、浓硫酸、 、浓硫酸、 的目的均为干燥气体 的目的均为干燥气体 |
| B.向图乙得到的过饱和磷酸溶液中加入磷酸晶体,可以促进其结晶 |
| C.图丙中冷凝管的进水口是b,具支烧瓶中得到磷酸溶液 |
| D.磷酸中少量的水极难除去的原因是磷酸可与水分子间形成氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室利用度弃旧电池的铜帽(主要成分为锌铜合金)回收Cu并制备ZnCl2的部分实验过程如图所示。下列说法正确的是


| A.“溶解"时Cu发生反应的离子方程式为Cu+H2O2+2HCl=Cu2++2H2O+2Cl— |
| B.因为升高温度可以加快反应速率,所以“溶解”时适宜使用高温 |
| C.将ZnCl2溶液加热蒸干即可获得无水ZnCl2 |
| D.“调节pH=2”后,溶液中大量存在的离子有Cu2+、Zn2+、H+、Na+、Cl— |
您最近一年使用:0次

 的热分解产物提出如下4种猜想:
的热分解产物提出如下4种猜想: 、
、 、
、
 、
、 、
、 、
、 溶液中:制备
溶液中:制备 胶体
胶体 溶液滴入
溶液滴入 溶液中:检验
溶液中:检验 的还原性强于
的还原性强于