有一包固体粉末,可能含有Na2SO4、MgCl2、Al(NO3)3、FeCl3中的一种或几种,按以下步骤进行实验:
①将固体粉末溶于水得无色溶液;
②向①的无色溶液中逐渐加入NaOH溶液至过量,先生成白色沉淀,最后白色沉淀部分溶解。
根据以上实验所产生的现象,回答下列问题:
(1)该粉末中一定含有___ (填化学式,下同),一定没有___ 。
(2)要确定该粉末中是否存在Na2SO4,可以增补实验___ 。
(3)生成白色沉淀的化学方程式为___ ;写出沉淀部分溶解所涉及的离子方程式:___ 。
①将固体粉末溶于水得无色溶液;
②向①的无色溶液中逐渐加入NaOH溶液至过量,先生成白色沉淀,最后白色沉淀部分溶解。
根据以上实验所产生的现象,回答下列问题:
(1)该粉末中一定含有
(2)要确定该粉末中是否存在Na2SO4,可以增补实验
(3)生成白色沉淀的化学方程式为
更新时间:2021-01-31 15:36:53
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
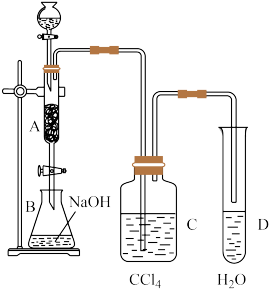
【推荐1】某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:

(1)该实验中A部分的装置是_____ (填字母)。
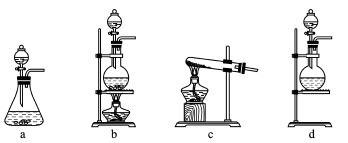
(2)装置B中的现象是_____ 。
(3)请写出装置C中发生反应的离子方程式:_____ 。请帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤):______ 。
(4)装置E的作用是______ 。
(5)制取Cl2的方法有多种,若A部分的装置是a,请再写出一种制备方法:______ (用化学方程式表示)。
 2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
2CaSO4+2Cl2↑+2H2O,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
(1)该实验中A部分的装置是

(2)装置B中的现象是
(3)请写出装置C中发生反应的离子方程式:
(4)装置E的作用是
(5)制取Cl2的方法有多种,若A部分的装置是a,请再写出一种制备方法:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某溶液中可能含有K+、Na+、CO 、Cl-中的一种或几种,为鉴别其中所含离子,现进行如表实验:
、Cl-中的一种或几种,为鉴别其中所含离子,现进行如表实验:
(1)原溶液中一定存在的离子是____ (填离子符号,下同),一定不存在的离子是____ ,可能存在的离子是____ 。
(2)为进一步确定“可能存在的离子”,另取原溶液加入足量____ ,有无色气体生成,再加____ ,有白色沉淀生成。生成白色沉淀的离子方程式为____ 。
 、Cl-中的一种或几种,为鉴别其中所含离子,现进行如表实验:
、Cl-中的一种或几种,为鉴别其中所含离子,现进行如表实验:| 序号 | 实验操作及现象 |
| 步骤① | 取原溶液,进行焰色试验,显黄色,透过蓝色钴玻璃观察无紫色 |
| 步骤② | 取原溶液,向溶液中加入盐酸,有气体产生 |
(2)为进一步确定“可能存在的离子”,另取原溶液加入足量
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】我国近代化学工业的奠基人之一侯德榜发明的“侯氏制碱法”,将制碱技术发展到了一个新的水平,在此基础上,将工业纯碱(含Mg2+、Fe3+、Cl-等杂质)进行提纯。工艺流程如下:
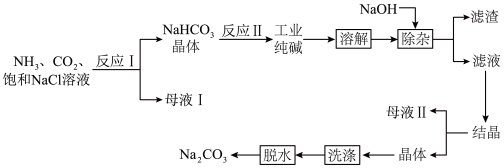
请回答下列问题。
(1)母液I中含有NH4Cl,NH4Cl的电离方程式是________ 。
(2)反应Ⅱ的化学方程式是________ 。
(3)流程中加入NaOH除去的杂质离子是________ 。
(4)结晶后的Na2CO3晶体表面附着有NaCl等杂质,需洗涤除去。检验NaCl是否已被洗涤除尽,需进行的操作和现象是________ ,有关反应的离子方程式是________ 。

请回答下列问题。
(1)母液I中含有NH4Cl,NH4Cl的电离方程式是
(2)反应Ⅱ的化学方程式是
(3)流程中加入NaOH除去的杂质离子是
(4)结晶后的Na2CO3晶体表面附着有NaCl等杂质,需洗涤除去。检验NaCl是否已被洗涤除尽,需进行的操作和现象是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】某溶液的溶质离子可能含有Mg2+、Ba2+、CO 、Cl-、SO
、Cl-、SO 、NO
、NO 中的几种,现进行如下实验:
中的几种,现进行如下实验:
1.取适量溶液,加入足量NaOH溶液,生成白色沉淀;
2.过滤,向实验1所得的滤液中加入足量H2SO4溶液,有白色沉淀生成。根据上述实验回答下列问题。
(1)溶液中一定不存在的离子是_________________
(2)写出1和2中所发生反应的离子方程式_________________
(3)为了验证溶液中是否存在Cl-、NO ,某同学提出下列假设:
,某同学提出下列假设:
①只存在Cl-;②Cl-、NO 同时存在;③
同时存在;③_____________________ 。
已知实验提供的试剂只有稀盐酸、AgNO3溶液、稀硝酸、NaOH溶液和蒸馏水。
实验方法:_________________
实验现象:_________________
实验结论:假设③正确
 、Cl-、SO
、Cl-、SO 、NO
、NO 中的几种,现进行如下实验:
中的几种,现进行如下实验:1.取适量溶液,加入足量NaOH溶液,生成白色沉淀;
2.过滤,向实验1所得的滤液中加入足量H2SO4溶液,有白色沉淀生成。根据上述实验回答下列问题。
(1)溶液中一定不存在的离子是
(2)写出1和2中所发生反应的离子方程式
(3)为了验证溶液中是否存在Cl-、NO
 ,某同学提出下列假设:
,某同学提出下列假设:①只存在Cl-;②Cl-、NO
 同时存在;③
同时存在;③已知实验提供的试剂只有稀盐酸、AgNO3溶液、稀硝酸、NaOH溶液和蒸馏水。
实验方法:
实验现象:
实验结论:假设③正确
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】现有一包固体可能由下列一种或几种物质组成:CuSO4、NaI、KNO3、NH4Cl、BaCl2、Na2CO3,为了鉴别做以下实验:
(1)将一定量的固体溶于水,得到无色澄清的溶液;
(2)将实验(1)中的溶液分成三份:在第一份溶液中加入足量的氢氧化钠溶液并加热,生成一种能使湿润红色石蕊试纸变蓝色的气体;在第二份溶液中滴入足量的稀盐酸,生成一种能使澄清石灰水变浑浊的气体;在第三份溶液中加入新制的氯水后,溶液变成深黄色,加入四氯化碳后振荡、静置,下层液体呈紫红色。试回答下列问题:
(1)原固体混合物中一定存在的物质是______________________________ ,一定不存在的物质是_______________________ 。
(2)实验(2)中第一份溶液与氢氧化钠溶液共热时发生的反应方程式
______________________________________________________________________________ 。
(1)将一定量的固体溶于水,得到无色澄清的溶液;
(2)将实验(1)中的溶液分成三份:在第一份溶液中加入足量的氢氧化钠溶液并加热,生成一种能使湿润红色石蕊试纸变蓝色的气体;在第二份溶液中滴入足量的稀盐酸,生成一种能使澄清石灰水变浑浊的气体;在第三份溶液中加入新制的氯水后,溶液变成深黄色,加入四氯化碳后振荡、静置,下层液体呈紫红色。试回答下列问题:
(1)原固体混合物中一定存在的物质是
(2)实验(2)中第一份溶液与氢氧化钠溶液共热时发生的反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某化工厂排出的废水透明、澄清、略显蓝色。某研究小组的实验探究如下:
(1)取少量废水,用稀盐酸,有不溶于稀硝酸的白色沉淀生成,该白色沉淀是______ ;过滤,将滤液分成两份,一份滤液中加入稀硫酸,有不溶于稀硝酸的白色硫酸钡沉淀生成;另一份滤液中加入足量氢氧化钠溶液,产生蓝色沉淀,该蓝色沉淀是_______ ;由此推断,该废水中一定含有的物质属于______ (填编号)。
A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐
(2)该小组又设计了一个从废水中回收金属和硫酸亚铁晶体的实验方案(提示:金属钡比金属铁活泼)。
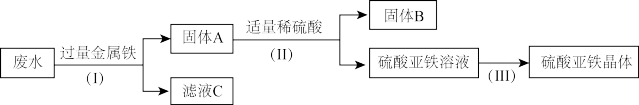
①固体B中一定含有的物质是_________ (写化学式);
②滤液C中含有的溶质是_______ 。
③步骤I、II的目的是固体和液体分离,操作名称是______ ;
④步骤II的目的是得到硫酸亚铁晶体,其操作顺序为________ (填编号)→洗涤干燥。
a.过滤 b.加热浓缩 c.冷却结晶
(1)取少量废水,用稀盐酸,有不溶于稀硝酸的白色沉淀生成,该白色沉淀是
A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐
(2)该小组又设计了一个从废水中回收金属和硫酸亚铁晶体的实验方案(提示:金属钡比金属铁活泼)。

①固体B中一定含有的物质是
②滤液C中含有的溶质是
③步骤I、II的目的是固体和液体分离,操作名称是
④步骤II的目的是得到硫酸亚铁晶体,其操作顺序为
a.过滤 b.加热浓缩 c.冷却结晶
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】无机框图推断题。A、B、C三种化合物有如下转化关系:
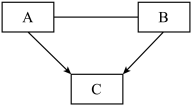
已知A是初中熟知的一元强酸,B是一元强碱,C是我们日常生活常用的调味品、是一种有咸味溶于水的白色固体。回答下列问题:
(1)将A的稀溶液中滴入紫色的石蕊试液,溶液变______ 色;将B的稀溶液中滴入无色的酚酞试液,溶液变______ 色;A是_____________ 、B是______________ (写名称)。
(2)向A中加入锌粉,该反应的离子方程式_______________ ,用单线桥法表示该反应电子转移方向和数目____________________ 。
(3)向B中通入少量的二氧化碳,该反应的离子方程式__________________________ 。
(4)将AB两物质混合,恰好完全反应。该反应的离子方程式____________________ 。
(5)检验A中阴离子的方法________________________________________________________ 。

已知A是初中熟知的一元强酸,B是一元强碱,C是我们日常生活常用的调味品、是一种有咸味溶于水的白色固体。回答下列问题:
(1)将A的稀溶液中滴入紫色的石蕊试液,溶液变
(2)向A中加入锌粉,该反应的离子方程式
(3)向B中通入少量的二氧化碳,该反应的离子方程式
(4)将AB两物质混合,恰好完全反应。该反应的离子方程式
(5)检验A中阴离子的方法
您最近一年使用:0次
【推荐2】现有一混合溶液,可能含有以下离子中的若干种:Na+、K+、Ca2+、C1-、 、
、 。取少量该混合溶液进行如下实验:
。取少量该混合溶液进行如下实验:
实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察火焰为紫色;
实验②:向混合溶液中加入足量BaCl2溶液,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解并产生气泡;
实验④:向②过滤后的溶液中加入硝酸银溶液,产生白色沉淀。
回答下列问题:
(1)由实验①推断该混合溶液中一定含有的离子是___________ (填离子符号,下同),检验该离子的实验方法的名称是___________ 。
(2)由实验②③推断该混合溶液中一定含有的离子是___________ ,一定不含的离子有___________ 。实验③中发生反应的离子反应方程式为___________ 。
(3)综合上述实验,是否能确定该混合溶液中含有Cl-_______ (填“是”或“否”)。若“是”下一空无需作答,若“否”请写出检验该混合溶液中Cl-的实验操作及现象___________ 。
 、
、 。取少量该混合溶液进行如下实验:
。取少量该混合溶液进行如下实验:实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察火焰为紫色;
实验②:向混合溶液中加入足量BaCl2溶液,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解并产生气泡;
实验④:向②过滤后的溶液中加入硝酸银溶液,产生白色沉淀。
回答下列问题:
(1)由实验①推断该混合溶液中一定含有的离子是
(2)由实验②③推断该混合溶液中一定含有的离子是
(3)综合上述实验,是否能确定该混合溶液中含有Cl-
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】已知苯与液溴在溴化铁的催化作用下可以发生反应生成溴苯。某化学课外小组用如图所示装置制取溴苯并证明苯与溴发生的是取代反应。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。已知溴可溶于溴苯中。
(1)写出A中反应的化学方程式:_______________ 。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________ ,写出有关的化学方程式__________________ 。
(3)实验时可观察到A中发生剧烈反应,反应液沸腾且有红棕色气体产生并充满A容器,说明苯与溴的反应是_______________ 反应(填“放热”或“吸热”)。
(4)向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明苯和溴发生的是取代反应而不是加成反应。另一种证明方法是向试管D中加入______________________ ,现象是________________ 。

(1)写出A中反应的化学方程式:
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(3)实验时可观察到A中发生剧烈反应,反应液沸腾且有红棕色气体产生并充满A容器,说明苯与溴的反应是
(4)向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明苯和溴发生的是取代反应而不是加成反应。另一种证明方法是向试管D中加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】有一包固体粉末,由BaCl2、KNO3、CaCO3、Na2SO4、CuSO4中的三种物质组成,取样品进行如下实验:

(1)根据上述实验现象,判断白色固体粉末中一定不含有____ (填化学式,下同),一定含有____ 。
(2)写出白色沉淀与稀盐酸反应的离子方程式:_____ 。
(3)这三种物质组成可能是_____ 。
A.BaCl2、KNO3、CaCO3 B.BaCl2、CuSO4、CaCO3
C.Na2SO4、KNO3、CaCO3 D.BaCl2、KNO3、Na2SO4
(4)实验中“过滤”操作所需要的玻璃仪器除玻璃棒外,还需要的是______ 。
(5)设计一个方案确定这三种物质的成分是(3)中的哪一种。_____ 。

(1)根据上述实验现象,判断白色固体粉末中一定不含有
(2)写出白色沉淀与稀盐酸反应的离子方程式:
(3)这三种物质组成可能是
A.BaCl2、KNO3、CaCO3 B.BaCl2、CuSO4、CaCO3
C.Na2SO4、KNO3、CaCO3 D.BaCl2、KNO3、Na2SO4
(4)实验中“过滤”操作所需要的玻璃仪器除玻璃棒外,还需要的是
(5)设计一个方案确定这三种物质的成分是(3)中的哪一种。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】有一包固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀盐酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液产生白色沉淀.
试根据上述实验事实,回答下列问题:
(1)原粉末中一定含有的物质是__________________ ,一定不含的物质是_____________ ,可能含有的物质是________________ 。(以上各种物质均写化学式)
(2)写出下列步骤中发生反应的离子方程式:
①_____________________________________________________________________ ;
②_______________________________________________________________________ ;
③_______________________________________________________________________ 。
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀盐酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液产生白色沉淀.
试根据上述实验事实,回答下列问题:
(1)原粉末中一定含有的物质是
(2)写出下列步骤中发生反应的离子方程式:
①
②
③
您最近一年使用:0次



