已知元素周期表中共有18纵行,如图实线表示元素周期表的边界。按电子排布,可把周期表里的元素划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入的电子的能级符号。
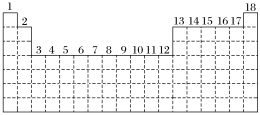
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影 和
和 表示d区和ds区。
表示d区和ds区。_______
(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在_______ 区。
(3)请在元素周期表中用元素符号标出4s轨道半充满的元素。_________
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:_______ 。
(5)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布_______ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
 和
和 表示d区和ds区。
表示d区和ds区。(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中用元素符号标出4s轨道半充满的元素。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
(5)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布
更新时间:2023-03-04 22:48:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】根据下图填写下列空格。
(1)在上面元素周期表中全部是金属元素的区域为_______________ 。
A、a区B、b区C、c区D、d区
(2)G元素与E元素形成的化合物的化学式是_________ 、_________ ,它们都是______________ (填“共价化合物”或“离子化合物”)。表格中十种元素的最高价氧化物对应的水化物中,碱性最强的是________________ (用化合物的化学式表示,下同),酸性最强的是______ ,属于两性氢氧化物的是____________________ 。
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | |||||||||||||||
| d | |||||||||||||||||
| a区 | b | 区 | c | 区 | 区 | ||||||||||||
(1)在上面元素周期表中全部是金属元素的区域为
A、a区B、b区C、c区D、d区
(2)G元素与E元素形成的化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、Z、W四种短周期元素,原子序数依次增大。且Y、Z、W为同周期元素,X、Z同主族,X、Z可形成共价化合物ZX3 和ZX2 ,Y的原子结构示意图如下图,据此填空:

(1)Y的元素名称为_______ 。
(2)X、Y、Z三种元素的原子,半径由小到大的顺序为_______ (用元素符号表示)。
(3)Y和W最高价氧化物的水化物酸性由强到弱的顺序为____________ (用化学式表示)。
(4)已知Na和单质Z可以形成离子化合物,写出该物质的电子式:__________ 。

(1)Y的元素名称为
(2)X、Y、Z三种元素的原子,半径由小到大的顺序为
(3)Y和W最高价氧化物的水化物酸性由强到弱的顺序为
(4)已知Na和单质Z可以形成离子化合物,写出该物质的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
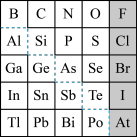
(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
②氢化物的还原性:H2O___ H2S(填“>”、“<”或“=”)。
(2)可在图中分界线(虚线部分)附近寻找___ (填序号)。
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为___ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是___ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4
②氢化物的还原性:H2O
(2)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空:
(1)元素周期表中,电负性最大的元素是___ (填元素符号),其氢化物为___ 酸(填“强”、“中强”“弱”)。
(2)以下是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
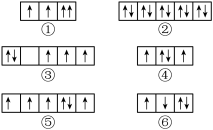
违反泡利不相容原理的有___ (填序号,下同),违反洪特规则的有___ 。
(3)海洋是元素的摇篮,海水中含有大量卤族元素。根据价层电子对互斥理论,预测ClO 的VSEPR模型
的VSEPR模型___ 形,空间构型为___ 形。
(1)元素周期表中,电负性最大的元素是
(2)以下是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。

违反泡利不相容原理的有
(3)海洋是元素的摇篮,海水中含有大量卤族元素。根据价层电子对互斥理论,预测ClO
 的VSEPR模型
的VSEPR模型
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】概率密度
用P表示电子在某处出现的概率,V表示该处的体积,则___________ 称为概率密度,用ρ表示。
用P表示电子在某处出现的概率,V表示该处的体积,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有_______ 种运动状态不同的电子,能量最高的电子,其电子云在空间有_______ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式_______ 。
(3)F在元素周期表中属于_______ 区元素,其基态原子核外共有_______ 个未成对电子。
(4)D、E两元素的第一电离能大小关系是_______ (用元素符号表示,下同),B、D两元素的电负性大小关系是_______ 。
(5)写出DA3的电子式:_______ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)D、E两元素的第一电离能大小关系是
(5)写出DA3的电子式:
您最近一年使用:0次



