电子在原子核外的区域内作高速运动,根据电子的能量高低划分为电子层,在各电子层上电子的排布也遵循着一定的规律。一些粒子的结构都可用下面的示意图来表示,且0<y≤8。
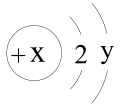
(1)若x=12时对应的元素为A,则y =_______ ;
(2)若某粒子带一个单位正电荷,则该粒子的化学符号为_______ ;
(3)若x=10,与其电子数相同的的微粒有(各举1个例子,可以是多核微粒):正离子_______ ,负离子_______ ,分子_______ 。
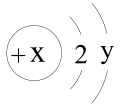
(1)若x=12时对应的元素为A,则y =
(2)若某粒子带一个单位正电荷,则该粒子的化学符号为
(3)若x=10,与其电子数相同的的微粒有(各举1个例子,可以是多核微粒):正离子
更新时间:2023-03-18 21:54:48
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
请回答下列问题。
(1)元素a中,含有1个质子和1个中子的核素的原子符号为_______ 。e的离子结构示意图为_______ ,元素 g在周期表中的位置为_______ 。
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为_______ 。
(3)非金属性,f_______ g(填“>”或“<”),能证明该结论的依据为_______ (列举一条)。
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:_______ (用相应的化学式表示)。
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式_______ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
h |
(1)元素a中,含有1个质子和1个中子的核素的原子符号为
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为
(3)非金属性,f
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】A、B、C、D四种短周期元素,0.5molA元素的离子得到的6.02×1023个电子后被还原为中性原子;0.4克A的氧化物恰好与100mL 0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等。A元素原子核外电子数比B元素原子核外电子数多1;C- 离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍。请填写下列空格:
(1)推断A、B、C、D四种元素的符号A_____ ;B____ ;C______ ;D_____ 。
(2)C的一价阴离子的结构示意图_____________________ ;
(3)D元素的最高价氧化物的结构式是:_______________ ;
(4)C、D两元素形成的化合物电子式_____________ ,分子内含有_________ 键(填“极性”或“非极性”)。
(5)用电子式表示A、C两元素形成的化合物的过程:
______________________________________________________________ 。
(6)写出A的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的化学方程式:
_______________________________________________________________________
(1)推断A、B、C、D四种元素的符号A
(2)C的一价阴离子的结构示意图
(3)D元素的最高价氧化物的结构式是:
(4)C、D两元素形成的化合物电子式
(5)用电子式表示A、C两元素形成的化合物的过程:
(6)写出A的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】钠是一种非常活泼,具有广泛应用的金属。
(1)钠的原子结构示意图为_______ 。
(2)金属钠非常活泼,通常保存在_______ 里,以隔绝空气。
(3) 、
、 、
、 、
、 久置于空气中最终都变为
久置于空气中最终都变为_______ (填化学式)。
(4)将 投入
投入 溶液中发生反应的现象有
溶液中发生反应的现象有_______ 。
(5)汽车安全气囊的气体发生剂NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
i.当汽车发生较严重的碰撞时,受热分解为Na和N2,其化学方程式为_______ ;
ii.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是_______ ;
(1)钠的原子结构示意图为
(2)金属钠非常活泼,通常保存在
(3)
 、
、 、
、 、
、 久置于空气中最终都变为
久置于空气中最终都变为(4)将
 投入
投入 溶液中发生反应的现象有
溶液中发生反应的现象有(5)汽车安全气囊的气体发生剂NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
i.当汽车发生较严重的碰撞时,受热分解为Na和N2,其化学方程式为
ii.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y在同一周期,Z与X在同一主族,Z元素的原子核内有16个质子,Y元素原子最外层电子数是K层所能容纳的电子数的2倍。试写出YX2和ZX2的化学式____ 、____ ,并用电子式表示YX2的形成过程____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知A、B、C、D、E、F、G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如下表所示。
元素B能与氢元素形成化合物BH3,在通常状况下,BH3的水溶液呈_______ (填“酸”、“碱”或“中”)性,原因为_______ (用方程式表示)。B和G的气态氢化物相互反应的化学方程式为_______ 。
| 元素 | 原子结构特征或有关物质的性质 |
| A | 原子的最外层电子数是其内层电子数的2倍 |
| B | 其单质是空气中含量最多的物质 |
| C | 原子的最外层电子数是其电子层数的4倍 |
| D | 位于第ⅡA族,其原子半径比E的大 |
| E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
| F | 原子序数16,其单质在通常状况下为固体 |
| G | 原子的最外层电子数比其次外层电子数少1个 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】有A、B、C、D、E、F六种元素,它们的相关信息如下表:
请填写下列空格:
(1)A原子的电子式:_____ 。
(2)B离子的结构示意图:_______ 。
(3)C元素的名称:___ ,C原子中能量最高的电子位于第______ 层,与C离子质子数与电子数均相同的微粒可能是______ (用微粒符号表示)。
(4)D的二价阴离子的电子式:___ ,D元素的某种同位素原子质量数为34,该原子核内的中子数为_____ 。
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:_____________ 。
| 元素代号 | 相关信息 |
| A | 最外层的电子数是次外层电子数的3倍 |
| B | 海水中含量第一位的金属元素 |
| C | L层得1个电子后成为稳定结构 |
| D | 二价阴离子核外有18个电子 |
| E | 失去一个电子后就成为一个质子 |
| F | 单质为黄绿色气体,具有刺激性气味 |
请填写下列空格:
(1)A原子的电子式:
(2)B离子的结构示意图:
(3)C元素的名称:
(4)D的二价阴离子的电子式:
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】完成下列问题。
(1)写出表示含有8个质子、10个中子的原子的化学符号:___________ 。
(2)根据下列微粒回答问题: 、
、 、
、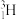 、14C、14N、16O、35Cl2、37Cl2。
、14C、14N、16O、35Cl2、37Cl2。
①以上8种微粒共有___________ 种核素,共包括___________ 种元素。
②互为同位素的是___________ 。
③质量数相等的是___________ 和___________ ,中子数相等的是___________ 和___________ 。
(3)相同物质的量的14CO2与S18O2的质量之比为___________ ;所含中子数之比为___________ ;所含电子数之比为___________ 。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)根据下列微粒回答问题:
 、
、 、
、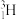 、14C、14N、16O、35Cl2、37Cl2。
、14C、14N、16O、35Cl2、37Cl2。①以上8种微粒共有
②互为同位素的是
③质量数相等的是
(3)相同物质的量的14CO2与S18O2的质量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知88 g D218O 和36 g H216O,请填空:
(1)两者所含的质子数之比为_______ 。
(2)两者所含的中子数之比为_______ 。
(3)若将它们分别与足量的金属钾反应,则两者产生的气体的质量之比为_______
(1)两者所含的质子数之比为
(2)两者所含的中子数之比为
(3)若将它们分别与足量的金属钾反应,则两者产生的气体的质量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】各种新型的电池有3000多种,金属常作为电池的电极材料。
(1)关于金属元素在自然界存在情况的叙述,不正确 的是__________ ;
A.金属元素仅存在于矿物中
B.金属元素存在于矿物和动物体内,但植物体内不含
C.少量金属元素以游离态存在,大多数金属元素以化合态存在
D.金属元素不仅存在矿物中,动物和植物体内也存在少量金属元素
(2)30号元素锌常用作电池的电极材料,画出锌的原子结构示意图____________________ ;
(3)碱性锌锰电池是日常生活中消耗量最大的电池,放电时总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。MnOOH中,Mn元素的化合价为__________ ;该电池的负极反应式为______________________ ;若某碱性锌锰电池维持电流强度0.5 A(相当于每秒通过5×10-6mol电子),连续工作80分钟即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有__________ %的锌粉未参加反应。
(1)关于金属元素在自然界存在情况的叙述,
A.金属元素仅存在于矿物中
B.金属元素存在于矿物和动物体内,但植物体内不含
C.少量金属元素以游离态存在,大多数金属元素以化合态存在
D.金属元素不仅存在矿物中,动物和植物体内也存在少量金属元素
(2)30号元素锌常用作电池的电极材料,画出锌的原子结构示意图
(3)碱性锌锰电池是日常生活中消耗量最大的电池,放电时总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。MnOOH中,Mn元素的化合价为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据下列几种粒子的结构示意图,回答问题:
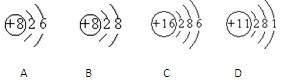
(1)属于阴离子的是______ (填粒子代号,下同)
(2)属于金属元素的是_______________________
(3)具有相似化学性质的是____________________
(4)D2C2含有的化学键类型有___________________ (选填“离子键”“极性键”“非极性键”)
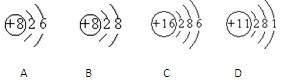
(1)属于阴离子的是
(2)属于金属元素的是
(3)具有相似化学性质的是
(4)D2C2含有的化学键类型有
您最近一年使用:0次

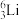 、
、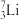 、
、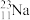 、
、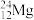 、
、 、
、 中
中

