按照要求回答下列问题。
(1)有下列物质: 、
、 、
、 、
、 、
、 、
、 、
、 。
。
①上述物质中既含共价键又含离子键的__________ ;属于共价化合物的是__________ ;
② 溶于水时破坏
溶于水时破坏__________ (填“共价键”或“离子键”,下同), 熔化时破坏
熔化时破坏__________ 。
(2)砷在元素周期表中的位置__________ 。原子序数为115的 中子数为
中子数为__________ 。
(3)向 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为__________ 。可证明非金属性:
__________ S(填“>”或“<”)。
(4)短周期元素Y的一种含氧酸化学式为 ,其结构式可表示为
,其结构式可表示为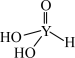 。该酸为
。该酸为__________ 元酸。写出该酸与过量 溶液反应的化学方程式:
溶液反应的化学方程式:__________ 。(用对应元素符号作答。已知信息:氢氧原子结合成的一种原子团“ ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
(1)有下列物质:
 、
、 、
、 、
、 、
、 、
、 、
、 。
。①上述物质中既含共价键又含离子键的
②
 溶于水时破坏
溶于水时破坏 熔化时破坏
熔化时破坏(2)砷在元素周期表中的位置
 中子数为
中子数为(3)向
 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为
(4)短周期元素Y的一种含氧酸化学式为
 ,其结构式可表示为
,其结构式可表示为 。该酸为
。该酸为 溶液反应的化学方程式:
溶液反应的化学方程式: ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
更新时间:2023-03-24 16:02:46
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】有下列物质:
①氢氧化钡②Al2(SO4)3③液态HCl④稀硫酸⑤二氧化碳⑥铁⑦碳酸钠⑧蔗糖⑨熔融氯化钠⑩
请回答下列问题:
(1)可以导电的有___________ (填序号)。
(2)属于电解质的有___________ (填序号)。
(3)属于非电解质的有___________ (填序号)。
(4)②在水中的电离方程式为___________ 。
(5)请写出④与⑦反应的离子方程式___________ 。
(6)请写出②与①反应的化学方程式___________ 。
①氢氧化钡②Al2(SO4)3③液态HCl④稀硫酸⑤二氧化碳⑥铁⑦碳酸钠⑧蔗糖⑨熔融氯化钠⑩

请回答下列问题:
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在水中的电离方程式为
(5)请写出④与⑦反应的离子方程式
(6)请写出②与①反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】研究水质除砷技术对保护环境有重要意义。
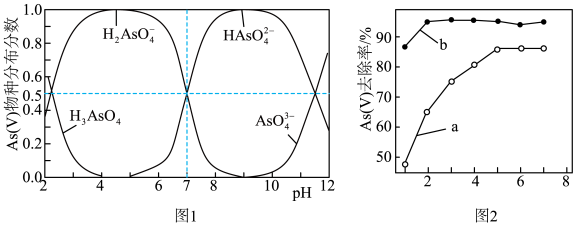
已知:As(V)在不同pH条件下的物种分布分数如图1所示。
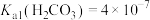 ,
,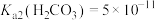 ;
;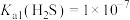 ,
,
(1)硫化法:As(Ⅲ)能与硫化剂(能提供 )反应生成雌黄(
)反应生成雌黄( )沉淀。HCHO能在硫酸盐还原菌的作用下将
)沉淀。HCHO能在硫酸盐还原菌的作用下将 还原为
还原为 ,同时生成
,同时生成 。
。
①沉淀1 mol As(Ⅲ)理论上需消耗HCHO的物质的量为______ mol。
② 能与
能与 反应:
反应: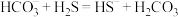 。该反应的平衡常数
。该反应的平衡常数
______ 。
(2)石灰沉淀法:向含砷(V)废水中添加石灰水,可使砷元素转化为多种砷酸钙盐沉淀。
①向中性废水中加入适量石灰水,使As(V)完全转化为 沉淀。写出该反应的离子方程式:
沉淀。写出该反应的离子方程式:____________ 。
②向含 沉淀的悬浊液中通入
沉淀的悬浊液中通入 气体,可得到
气体,可得到 。该转化能实现的原因是
。该转化能实现的原因是____________ 。
③控制其他条件不变,向碱性含砷(V)废水中加入一定量石灰水,测得As(V)去除率在30℃以后随温度升高而降低。可能的原因是__________________ 。
④在初始pH、c[As(V)]相同的模拟废水中加入石灰水,As(V)去除率随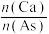 的变化如图2曲线a所示;固定
的变化如图2曲线a所示;固定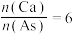 ,往石灰水中添加Fe(Ⅲ)盐,As(V)去除率随
,往石灰水中添加Fe(Ⅲ)盐,As(V)去除率随 的变化如图2曲线b所示。加入Fe(Ⅲ)盐后,As(V)去除率增大的原因是
的变化如图2曲线b所示。加入Fe(Ⅲ)盐后,As(V)去除率增大的原因是____________ 。
已知:As(V)在不同pH条件下的物种分布分数如图1所示。
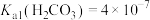 ,
,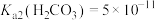 ;
;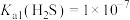 ,
,

(1)硫化法:As(Ⅲ)能与硫化剂(能提供
 )反应生成雌黄(
)反应生成雌黄( )沉淀。HCHO能在硫酸盐还原菌的作用下将
)沉淀。HCHO能在硫酸盐还原菌的作用下将 还原为
还原为 ,同时生成
,同时生成 。
。①沉淀1 mol As(Ⅲ)理论上需消耗HCHO的物质的量为
②
 能与
能与 反应:
反应: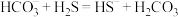 。该反应的平衡常数
。该反应的平衡常数
(2)石灰沉淀法:向含砷(V)废水中添加石灰水,可使砷元素转化为多种砷酸钙盐沉淀。
①向中性废水中加入适量石灰水,使As(V)完全转化为
 沉淀。写出该反应的离子方程式:
沉淀。写出该反应的离子方程式:②向含
 沉淀的悬浊液中通入
沉淀的悬浊液中通入 气体,可得到
气体,可得到 。该转化能实现的原因是
。该转化能实现的原因是③控制其他条件不变,向碱性含砷(V)废水中加入一定量石灰水,测得As(V)去除率在30℃以后随温度升高而降低。可能的原因是
④在初始pH、c[As(V)]相同的模拟废水中加入石灰水,As(V)去除率随
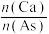 的变化如图2曲线a所示;固定
的变化如图2曲线a所示;固定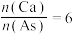 ,往石灰水中添加Fe(Ⅲ)盐,As(V)去除率随
,往石灰水中添加Fe(Ⅲ)盐,As(V)去除率随 的变化如图2曲线b所示。加入Fe(Ⅲ)盐后,As(V)去除率增大的原因是
的变化如图2曲线b所示。加入Fe(Ⅲ)盐后,As(V)去除率增大的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】按要求完成下列问题:
(1)写出下列反应的化学方程式,是离子反应的只需写出离子方程式:
①实验室制备氢氧化铝________ 。
②实验室制备氯气________ 。
(2)配平下列化学方程式
①_____
________ ________
________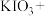 ________
________ ________
________ ________
________ ________
________
②____
________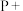 ________
________ ________
________ ________
________ ________
________ ________
________
③____
________ ________
________ ________
________ ________
________ ________
________ ________
________
④________
________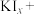 ________
________ ________
________ ________KCl+________
________KCl+________ ________HCl
________HCl
(1)写出下列反应的化学方程式,是离子反应的只需写出离子方程式:
①实验室制备氢氧化铝
②实验室制备氯气
(2)配平下列化学方程式
①
________
 ________
________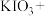 ________
________ ________
________ ________
________ ________
________
②
________
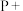 ________
________ ________
________ ________
________ ________
________ ________
________
③
________
 ________
________ ________
________ ________
________ ________
________ ________
________
④
________
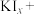 ________
________ ________
________ ________KCl+________
________KCl+________ ________HCl
________HCl
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位置,结构和性质的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
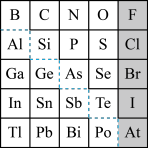
(l)Ge 的最高价氧化物对应水化物的化学式为_____ ,P、S、Cl元素对应的简单离子的还原性由强到弱的顺序为_____ 。(写离子符号)
(2)根据元素周期律,推断:
①阴影部分元素最高价氧化物对应水化物的酸性最强的是_____ 。(写化学式)
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“> ”“< ”或“=” )_____ H2SeO4。
③镓的氯化物与氨水反应的化学方程式为_____
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。:如2A1+4BaO 3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是
3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是____________
a.高温时Al 的活泼性大于Ba b.高温有利于BaO 分解
c.高温时BaO• A12O3比A12O3稳定 d.Ba的沸点比Al 的低
(4)用铝热法还原下列氧化物,制得金属各l mol,消耗铝最少的是________ 。
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4

(l)Ge 的最高价氧化物对应水化物的化学式为
(2)根据元素周期律,推断:
①阴影部分元素最高价氧化物对应水化物的酸性最强的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“> ”“< ”或“=” )
③镓的氯化物与氨水反应的化学方程式为
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。:如2A1+4BaO
 3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是
3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是a.高温时Al 的活泼性大于Ba b.高温有利于BaO 分解
c.高温时BaO• A12O3比A12O3稳定 d.Ba的沸点比Al 的低
(4)用铝热法还原下列氧化物,制得金属各l mol,消耗铝最少的是
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4
您最近一年使用:0次
填空题
|
较难
(0.4)
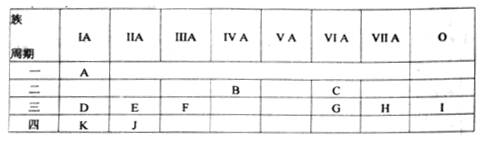
【推荐2】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)______ ,离子半径最小的是____ (写元素符号)。
(2)J的简单离子的结构示意图__________ 。
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)____ 。
(4)比较G、H两元素的最高价氧化物对应水化物的酸性______ (写化学式,下同)。比较C、G两元素的气态氢化物稳定性_________ 。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)
(2)J的简单离子的结构示意图
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)
(4)比较G、H两元素的最高价氧化物对应水化物的酸性
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(I)俄美科学家联合小组宣布合成出114号元素(FI)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中位于第______ 周期,_____ 族,属于金属元素还是非金属元素?____
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式________ 。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为__________ 。
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为___________ 。
(3)元素⑩的单质与⑦的氢化物高温下反应的化学方程式为___________ 。
(III)判断以下叙述正确的是__________ 。
部分短周期元素的原子半径及主要化合价
A. L2+、R2-的核外电子数相等
B. 单质与稀盐酸反应的速率L<Q
C. M与T形成的化合物一定具有两性
D. 氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中位于第
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
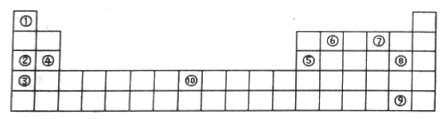
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为
(3)元素⑩的单质与⑦的氢化物高温下反应的化学方程式为
(III)判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A. L2+、R2-的核外电子数相等
B. 单质与稀盐酸反应的速率L<Q
C. M与T形成的化合物一定具有两性
D. 氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】下表列出了7种短周期元素在元素周期表中的相对位置,其中元素①的最低负化合价的绝对值与其原子最外层电子数相等,元素⑤是地壳中含量最多的金属元素。
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是_______ 。
(2)上述7中元素中,非金属性最强的是______ (填元素符号);最高价氧化物对应水化物中,碱性最强的物质的化学式是_______ 。
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是________ 。
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是_______________ 。
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是_______ 。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是_______ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是
(2)上述7中元素中,非金属性最强的是
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】I如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:
(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式________ 。
(2)用电子式表示⑥和⑨形成化合物的过程:________ 。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为________ (用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式________ 。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为(用离子符号表示)________ 。
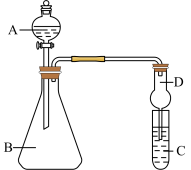
Ⅱ某同学欲利用下图装置验证同主族元素性质递变规律。若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C溶液中现象为________ ,反应离子方程式为________ ,即可证明。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式
(2)用电子式表示⑥和⑨形成化合物的过程:
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式
(5)⑤、⑥、⑩的离子半径由大到小的顺序为(用离子符号表示)
Ⅱ某同学欲利用下图装置验证同主族元素性质递变规律。若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C溶液中现象为

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】2015年8月12日晚,天津滨海新区某公司仓库发生爆炸,事发仓库里存放了大量的硝酸铵、氰化钠(NaCN)、金属钠等危险化学品。回答下列问题:
(1)NaCN的电子式为:_______________________ 。
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:_____________________________ 。
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄漏可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因:______________________________ 。
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式_____________________________ ;
③用硫代硫酸钠中和的离子方程式为CN-+ →A+
→A+ (已配平),A为
(已配平),A为_________ (填化学式)。
(4)CN-中C元素显+2价,N元素显﹣3价,则非金属性N_______ C(填<、=或>),请用简单的实验方法证明(要求说明简单操作、现象和结论):_______________________________________ 。
(5)0.4mol/L的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是_______________________________________
(1)NaCN的电子式为:
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄漏可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因:
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式
③用硫代硫酸钠中和的离子方程式为CN-+
 →A+
→A+ (已配平),A为
(已配平),A为(4)CN-中C元素显+2价,N元素显﹣3价,则非金属性N
(5)0.4mol/L的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】按要求填空:
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式________ ,其单质与NaOH反应的化学方程式为____________________________________________________ 。
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是___________________ ,原子半径由大到小的顺序是__________________ 。
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ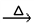 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:_____________ ,______________ ;比较C和D的稳定性的强弱:_____________________ (用化学式表示)。
(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是_______ (填序号),既有离子键又有非极性键的是______ (填序号);既有离子键又有极性键的是______ (填序号)。
(5)下列原子: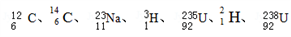 中共有
中共有____ 种元素,__ 种核素。
(6)写出下列物质或微粒的电子式:
①CO2__________ ②KCl_____________ ③H2O2_______________ ④N2_____________ ;
⑤用电子式表示MgCl2的形成过程_________________________________________________ 。
(1)原子核外有3个电子层,其价电子数为7的元素其最高价氧化物对应水化物化学式
(2)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是
(3) A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
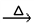 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:(4)①NH4NO3 ②NaF ③CO2 ④K2O2 ⑤NaOH ⑥CH4
以上只含有极性键的是
(5)下列原子:
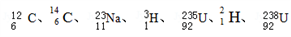 中共有
中共有(6)写出下列物质或微粒的电子式:
①CO2
⑤用电子式表示MgCl2的形成过程
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为________ (填化学式)。
(2)KClO4是助氧化剂,其中含有化学键的类型为________________________ 。
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
________________________________________________________________ 。
(4)NaN3是气体发生剂,受热分解产生N2和Na。取56 g上述产气药剂,分解产生的气体通过碱石灰后的体积为16.8 L(标准状况),该产气药剂中NaN3的质量分数为________ 。
(1)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为
(2)KClO4是助氧化剂,其中含有化学键的类型为
(3)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
(4)NaN3是气体发生剂,受热分解产生N2和Na。取56 g上述产气药剂,分解产生的气体通过碱石灰后的体积为16.8 L(标准状况),该产气药剂中NaN3的质量分数为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】硫代硫酸钠(Na2S2O3)是一种常用的化工原料,常用作除氯剂等。回答下列问题:
(1)硫代硫酸钠中所含的化学键类型为_______________________ 。
(2)硫代硫酸钠在中性或碱性溶液中稳定,在酸性溶液中不稳定。向pH=2的硫酸中滴加Na2S2O3溶液,可观察到的现象是________________ 。
(3)实验测定Na2S2O3溶液呈弱碱性,用离子方程式解释其主要原因:__________ ,25℃时该离子反应的平衡常数值约为__________________
【已知:25℃时K1(H2S2O3)=2.52×10-1mol/L,K2(H2S2O3)=1.02xl0-2mol/L】
(4)实际生产中,一般将Na2S和Na2CO3以物质的量比2∶1配成溶液后加热,将SO2缓缓通入溶液中,即可得到硫代硫酸钠。反应的化学方程式为_______________________ 。
(5)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯需要0.56g硫代硫酸钠。硫代硫酸钠作除氯剂的主要原因是其具有_________ 性,反应的离子方程式为___________________ 。
(1)硫代硫酸钠中所含的化学键类型为
(2)硫代硫酸钠在中性或碱性溶液中稳定,在酸性溶液中不稳定。向pH=2的硫酸中滴加Na2S2O3溶液,可观察到的现象是
(3)实验测定Na2S2O3溶液呈弱碱性,用离子方程式解释其主要原因:
【已知:25℃时K1(H2S2O3)=2.52×10-1mol/L,K2(H2S2O3)=1.02xl0-2mol/L】
(4)实际生产中,一般将Na2S和Na2CO3以物质的量比2∶1配成溶液后加热,将SO2缓缓通入溶液中,即可得到硫代硫酸钠。反应的化学方程式为
(5)在水产养殖上,硫代硫酸钠常用于除去自来水中的氯气,理论上,去除1g的氯需要0.56g硫代硫酸钠。硫代硫酸钠作除氯剂的主要原因是其具有
您最近一年使用:0次



