1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位置,结构和性质的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
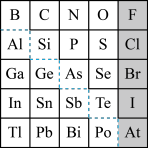
(l)Ge 的最高价氧化物对应水化物的化学式为_____ ,P、S、Cl元素对应的简单离子的还原性由强到弱的顺序为_____ 。(写离子符号)
(2)根据元素周期律,推断:
①阴影部分元素最高价氧化物对应水化物的酸性最强的是_____ 。(写化学式)
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“> ”“< ”或“=” )_____ H2SeO4。
③镓的氯化物与氨水反应的化学方程式为_____
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。:如2A1+4BaO 3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是
3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是____________
a.高温时Al 的活泼性大于Ba b.高温有利于BaO 分解
c.高温时BaO• A12O3比A12O3稳定 d.Ba的沸点比Al 的低
(4)用铝热法还原下列氧化物,制得金属各l mol,消耗铝最少的是________ 。
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4

(l)Ge 的最高价氧化物对应水化物的化学式为
(2)根据元素周期律,推断:
①阴影部分元素最高价氧化物对应水化物的酸性最强的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“> ”“< ”或“=” )
③镓的氯化物与氨水反应的化学方程式为
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。:如2A1+4BaO
 3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是
3Ba↑ +BaO •A12O3,利用上述方法可制取Ba的主要原因是a.高温时Al 的活泼性大于Ba b.高温有利于BaO 分解
c.高温时BaO• A12O3比A12O3稳定 d.Ba的沸点比Al 的低
(4)用铝热法还原下列氧化物,制得金属各l mol,消耗铝最少的是
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4
更新时间:2020-08-07 10:56:59
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】下图是元素周期表的一部分。
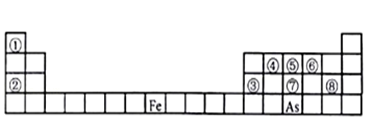
Ⅰ、用化学用语回答下列问题:
(1)由②、⑥两元素形成的强氧化性物质的电子式为_______ ,由①、⑤两元素构成的10电子化合物的形成过程为_______ 。
(2)⑦、⑧的最高价含氧酸的酸性较弱的是_______ 。(化学式表示)
(3)As在元素周期表中位置为__ ;氢化物的沸点:NH3 _______ AsH3(填“>”或“<”)
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_______ ,当消耗75g还原剂时,电子转移了__ mol。
Ⅱ、A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如下图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。
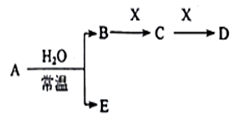
(1)A与水反应的化学方程式为_______ 。
(2)工业上常用CO热还原法冶炼X,写出其化学方程式_______ 。
(3)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式_______ 。
Ⅲ、由①、⑤、⑥、S和Fe五种元素组成的相对分子质量为392的化合物B,B中含有结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
(1)由实验a、b推知B溶液中含有的离子为_______ ;
(2)B的化学式为_______ 。

Ⅰ、用化学用语回答下列问题:
(1)由②、⑥两元素形成的强氧化性物质的电子式为
(2)⑦、⑧的最高价含氧酸的酸性较弱的是
(3)As在元素周期表中位置为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
Ⅱ、A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如下图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。

(1)A与水反应的化学方程式为
(2)工业上常用CO热还原法冶炼X,写出其化学方程式
(3)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式
Ⅲ、由①、⑤、⑥、S和Fe五种元素组成的相对分子质量为392的化合物B,B中含有结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
(1)由实验a、b推知B溶液中含有的离子为
(2)B的化学式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在元素周期表中的位置:___________ ,有关Be性质的推断不正确的是___________ (填序号)。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时, 溶液的
溶液的
(2)已知: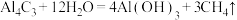 ,写出
,写出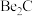 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):___________
(3)基态铝原子的价电子排布式为___________ ,镁铝合金经过高温淬火获得一种储钠材料,用___________ 法测定其晶胞结构如图1所示,图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___________ ,该立方晶胞的晶胞的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为___________ pm。(列出计算式,可不化简)。
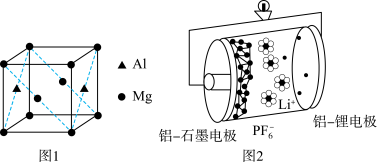
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为: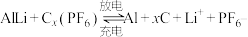 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为___________ ,充电时,应将铝-石墨电极与外接电源的___________ 极相连。
(1)Be元素在元素周期表中的位置:
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时,
 溶液的
溶液的
(2)已知:
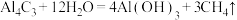 ,写出
,写出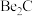 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):(3)基态铝原子的价电子排布式为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为:
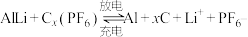 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】按照要求回答下列问题。
(1)有下列物质: 、
、 、
、 、
、 、
、 、
、 、
、 。
。
①上述物质中既含共价键又含离子键的__________ ;属于共价化合物的是__________ ;
② 溶于水时破坏
溶于水时破坏__________ (填“共价键”或“离子键”,下同), 熔化时破坏
熔化时破坏__________ 。
(2)砷在元素周期表中的位置__________ 。原子序数为115的 中子数为
中子数为__________ 。
(3)向 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为__________ 。可证明非金属性:
__________ S(填“>”或“<”)。
(4)短周期元素Y的一种含氧酸化学式为 ,其结构式可表示为
,其结构式可表示为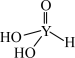 。该酸为
。该酸为__________ 元酸。写出该酸与过量 溶液反应的化学方程式:
溶液反应的化学方程式:__________ 。(用对应元素符号作答。已知信息:氢氧原子结合成的一种原子团“ ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
(1)有下列物质:
 、
、 、
、 、
、 、
、 、
、 、
、 。
。①上述物质中既含共价键又含离子键的
②
 溶于水时破坏
溶于水时破坏 熔化时破坏
熔化时破坏(2)砷在元素周期表中的位置
 中子数为
中子数为(3)向
 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为
(4)短周期元素Y的一种含氧酸化学式为
 ,其结构式可表示为
,其结构式可表示为 。该酸为
。该酸为 溶液反应的化学方程式:
溶液反应的化学方程式: ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
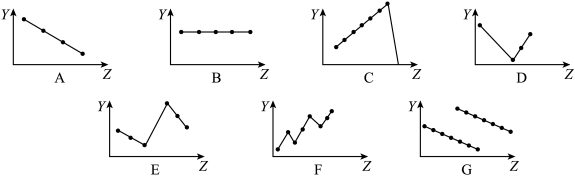
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数_____________ 。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径_______ 。
③第二、三周期主族元素随原子序数递增原子半径的变化___________ 。
(2)已知某单核粒子的结构示意图为:
①当x-y=10时,该粒子为______ (填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_______ 。
(3)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。
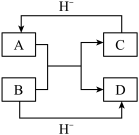
请写出:A的化学式_______ (写一种);D的化学式________ 。
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径
③第二、三周期主族元素随原子序数递增原子半径的变化
(2)已知某单核粒子的结构示意图为:

①当x-y=10时,该粒子为
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是
(3)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。

请写出:A的化学式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】硒的原子序数为34,是硫的同主族元素,硒的单质及其化合物用途非常广泛。
(1)硒位于周期表第___ ,周期___ 族。Se2Cl2常用作分析试剂,其电子式为_____ 。
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是_____ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___ 。用氨水中和亚硒酸后得到亚硒酸铵,再向( NH4)2SeO3溶液中加入Na2S2O3可得到纳米硒,同时生成亚硫酸盐,(NH4)2SeO3与Na2S2O3反应生成纳米硒的离子方程式为______ 。
(1)硒位于周期表第
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】随原子序数递增,八种短周期元素(用字母x表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断回答下列问题:
(1)f在周期表中的位置是__________ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):_______ >__________ ;比较g、h的最高价氧化物对应水化物的酸性强弱:_______ >__________ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_________________ 。
(4)写出e的单质在足量d2中燃烧反应的化学方程式:____________________________ 。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1R溶液的烧杯中逐滴加入1 mol·L-1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化示意图如下:

①写出m点反应的离子方程式:____________________________ 。
②若在R溶液中改加20 mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_______ mol。

根据判断回答下列问题:
(1)f在周期表中的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同):
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:
(4)写出e的单质在足量d2中燃烧反应的化学方程式:
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1R溶液的烧杯中逐滴加入1 mol·L-1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化示意图如下:

①写出m点反应的离子方程式:
②若在R溶液中改加20 mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】按要求填空。
(1)比较大小或强弱
①A.乙酸(CH3COOH)、B.三氟乙酸(CF3COOH)、C.三氯乙酸(CCl3COOH),它们的酸性由强到弱的顺序为_______ (用ABC字母作答,填汉字不给分,下同)。
②A.一氯乙烷(CH2ClCH3)、B.乙烷(CH3CH3)、C.乙醇(CH3CH2OH),它们的沸点由高到低的顺序为_______ 。
③A.丙三醇(CH2OHCHOHCH2OH)、B.丙醇(CH3CH2CH2OH)、C.丙烷(CH3CH2CH3),它们的水溶性由好到差的顺序为_______ 。
④A.SCl2、B.CS2、C.SO2,它们的键角由大到小的顺序为_______ 。
(2) 的空间结构为
的空间结构为_______ ,中心原子Cl的杂化类型为_______ 。
(3)有机物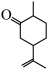 中,有
中,有_______ 个手性碳,1mol该有机物含π键的个数为_______ 。
(4)H2O的热稳定性比H2S好,沸点也比H2S高,原因是_______ 。
(1)比较大小或强弱
①A.乙酸(CH3COOH)、B.三氟乙酸(CF3COOH)、C.三氯乙酸(CCl3COOH),它们的酸性由强到弱的顺序为
②A.一氯乙烷(CH2ClCH3)、B.乙烷(CH3CH3)、C.乙醇(CH3CH2OH),它们的沸点由高到低的顺序为
③A.丙三醇(CH2OHCHOHCH2OH)、B.丙醇(CH3CH2CH2OH)、C.丙烷(CH3CH2CH3),它们的水溶性由好到差的顺序为
④A.SCl2、B.CS2、C.SO2,它们的键角由大到小的顺序为
(2)
 的空间结构为
的空间结构为(3)有机物
 中,有
中,有(4)H2O的热稳定性比H2S好,沸点也比H2S高,原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】硒的原子序数为34,是硫的同主族元素,硒的单质及其化合物用途非常广泛。
(1)硒位于周期表第___ ,周期___ 族。Se2Cl2常用作分析试剂,其电子式为_____ 。
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是_____ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___ 。用氨水中和亚硒酸后得到亚硒酸铵,再向( NH4)2SeO3溶液中加入Na2S2O3可得到纳米硒,同时生成亚硫酸盐,(NH4)2SeO3与Na2S2O3反应生成纳米硒的离子方程式为______ 。
(1)硒位于周期表第
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】海水是资源宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。完成下列填空:
(1)氯离子原子核外有_____ 种不同运动状态的电子、有____ 种不同能量的电子。
(2)溴在周期表中的位置_________ 。
(3)卤素单质及其化合物在许多性质上都存在递变规律,请说明下列递变规律的原因。
① 熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是______________ 。
② 还原性按Cl—、Br—、I—的顺序依次增大,原因是____________ 。
(4)已知X2 (g) + H2 (g) 2HX (g) + Q(X2 表示Cl2、Br2),如图表示上述反应的平衡常数K与温度T的关系。
2HX (g) + Q(X2 表示Cl2、Br2),如图表示上述反应的平衡常数K与温度T的关系。

① Q表示X2 (g)与H2 (g)反应的反应热,Q_____ 0(填“>”、“<”或“=”)。
② 写出曲线b表示的平衡常数K的表达式,K=______ (表达式中写物质的化学式)。
(5)(CN)2是一种与Cl2性质相似的气体,在(CN)2中C显+3价,N显-3价,氮元素显负价的原因_________ ,该分子中每个原子都达到了8电子稳定结构,写出(CN)2的电子式_____ 。
(1)氯离子原子核外有
(2)溴在周期表中的位置
(3)卤素单质及其化合物在许多性质上都存在递变规律,请说明下列递变规律的原因。
① 熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是
② 还原性按Cl—、Br—、I—的顺序依次增大,原因是
(4)已知X2 (g) + H2 (g)
 2HX (g) + Q(X2 表示Cl2、Br2),如图表示上述反应的平衡常数K与温度T的关系。
2HX (g) + Q(X2 表示Cl2、Br2),如图表示上述反应的平衡常数K与温度T的关系。
① Q表示X2 (g)与H2 (g)反应的反应热,Q
② 写出曲线b表示的平衡常数K的表达式,K=
(5)(CN)2是一种与Cl2性质相似的气体,在(CN)2中C显+3价,N显-3价,氮元素显负价的原因
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】现有下列短周期元素的数据(已知Be的原子半径为0.089nm):
(1)⑧号元素在周期表中的位置是______________________________ ;上述元素处于同一主族的有_______________________________ 。(用元素符号表示)
(2)元素①和⑥能形成两种化合物,其中较稳定的化合物与水反应的离子方程式:_______ 。
(3)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等); 和
和 作核反应堆最佳热载体,
作核反应堆最佳热载体, H和
H和 D用作高温堆减速剂。下列说法中正确的是
D用作高温堆减速剂。下列说法中正确的是___________ 。
A. 和
和 属于同种核素
属于同种核素
B. H和
H和 D的化学性质不同
D的化学性质不同
C. H和
H和 D是同种物质
D是同种物质
D.氧化性:Li+<Na+<K+<Rb+<Cs+
E.碱性:Be(OH)2<LiOH<NaOH<KOH
F.半径:K>Na>Li>Li+
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程中的总离子方程式______________ 。反应生成的两种碱继续作用即得到产品。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
(1)⑧号元素在周期表中的位置是
(2)元素①和⑥能形成两种化合物,其中较稳定的化合物与水反应的离子方程式:
(3)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等);
 和
和 作核反应堆最佳热载体,
作核反应堆最佳热载体, H和
H和 D用作高温堆减速剂。下列说法中正确的是
D用作高温堆减速剂。下列说法中正确的是A.
 和
和 属于同种核素
属于同种核素B.
 H和
H和 D的化学性质不同
D的化学性质不同C.
 H和
H和 D是同种物质
D是同种物质D.氧化性:Li+<Na+<K+<Rb+<Cs+
E.碱性:Be(OH)2<LiOH<NaOH<KOH
F.半径:K>Na>Li>Li+
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程中的总离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】填写下列空白:
(1)某元素的气态氢化物的化学式XH4,则其最高价氧化物对应的水化物的化学式为_________ 。
(2)氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则氧元素的相对原子质量为_________________ 。
(3)物质的量相同的H2O和D2O与足量钠反应,放出的气体的质量之比为____________ 。
(4)X2﹣含中子N个,X的质量数为A,则1g X的氢化物中含质子的物质的量是______ mol。
(5)铷和另一种碱金属形成的合金4.6g与足量的水反应后,产生0.2 g氢气,则此合金中另一碱金属可能是:__________ 。
(1)某元素的气态氢化物的化学式XH4,则其最高价氧化物对应的水化物的化学式为
(2)氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则氧元素的相对原子质量为
(3)物质的量相同的H2O和D2O与足量钠反应,放出的气体的质量之比为
(4)X2﹣含中子N个,X的质量数为A,则1g X的氢化物中含质子的物质的量是
(5)铷和另一种碱金属形成的合金4.6g与足量的水反应后,产生0.2 g氢气,则此合金中另一碱金属可能是:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】短周期主族元素 A、B、C、D、E、F 的原子序数依次增大,A 原子核外最外 层电子数是其电子层数的 2 倍,A、B 的核电荷数之比为 3:4。C 与 D 均为金属元素,5.8 g D 的氢氧化物恰好能与 100 mL 2 mol·L-1 盐酸完全反应,D 原子核中质子数和中子数相等。E 与F 相邻,F-的最外层为 8 电子结构。根据上述条件,用化.学.用.语.回答:
(1)D 在周期表中的位置____ ;
(2)B、C 易形成淡黄色化合物,其电子式为____ ,该物质含有的化学键 类型为_____ ;
(3)用电子式表示 DF2 的形成过程____ ;
(4)元素 E、F 中非金属性较强的是____ ,请用一个置换反应证明____ (写化学反应方程式);
(5)原子半径:C____ E;熔点:DB____ CF(填“>”“<”或“=”);
(6)A、B、E 可形成一个三原子分子,且每个原子均达到 8 电子稳定结构,则该分子的 结构式为____ ;含 A元素的化合物在是自然界种类最多的原因是____ 。
(1)D 在周期表中的位置
(2)B、C 易形成淡黄色化合物,其电子式为
(3)用电子式表示 DF2 的形成过程
(4)元素 E、F 中非金属性较强的是
(5)原子半径:C
(6)A、B、E 可形成一个三原子分子,且每个原子均达到 8 电子稳定结构,则该分子的 结构式为
您最近一年使用:0次



