硒的原子序数为34,是硫的同主族元素,硒的单质及其化合物用途非常广泛。
(1)硒位于周期表第___ ,周期___ 族。Se2Cl2常用作分析试剂,其电子式为_____ 。
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是_____ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___ 。用氨水中和亚硒酸后得到亚硒酸铵,再向( NH4)2SeO3溶液中加入Na2S2O3可得到纳米硒,同时生成亚硫酸盐,(NH4)2SeO3与Na2S2O3反应生成纳米硒的离子方程式为______ 。
(1)硒位于周期表第
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
更新时间:2017-10-30 11:04:28
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】实验室只有36.5%,密度为1.2g/cm3的浓盐酸,现需配制100mL 10%密度0.9g/cm3的盐酸,需36.5%的浓盐酸______________ mL。在配制过程中,用到的仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要___________ 。定容时,如果眼睛仰视刻线,配制的溶液的浓度将______________ (填偏高,偏低,无影响),10%的盐酸逐滴加入到纯碱溶液中,反应的离子方程式为_____________ 。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】Ⅰ.化合物 Mg5Al3(OH)19(H2O)4 可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据___________ 。
(2)用离子方程式表示除去固体产物中 Al2O3 的原理___________
(3)已知 MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理_____________ 。
Ⅱ.磁性材料 A(M=296g/mol)是由两种元素组成的化合物,某研究小组按如图流程探 究其组成:
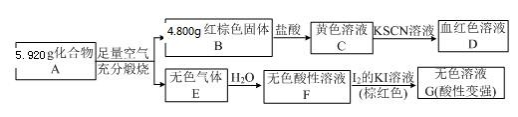
请回答:
(4)A的化学式为_____ 。C 中呈黄色的离子对应元素在元素周期表中的位置为__________ 。
(5)已知化合物 A 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下,该气体对氨气的相对密度为2),该气体分子的电子式为_____ 。写出该反应的离子方程式_________ 。
(6)写出F→G反应的化学方程式____________ 。
 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3(1)写出该化合物作阻燃剂的两条依据
(2)用离子方程式表示除去固体产物中 Al2O3 的原理
(3)已知 MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理
Ⅱ.磁性材料 A(M=296g/mol)是由两种元素组成的化合物,某研究小组按如图流程探 究其组成:

请回答:
(4)A的化学式为
(5)已知化合物 A 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下,该气体对氨气的相对密度为2),该气体分子的电子式为
(6)写出F→G反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】铜及其化合物在生产生活有广泛应用,铜在化合物中的常见化合价有+1、+2.已知 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
(1)工业上可用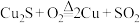 反应制取粗铜,该反应中
反应制取粗铜,该反应中___________ 元素被还原。不考虑杂质的反应,理论上生成1mol的 电子转移的数目为
电子转移的数目为___________
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为___________ 。温度控制在50~60℃的原因除了加快反应速率外,还有___________ 。在 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:___________ 。
(3)现向Cu、 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为___________ 。若将上述混合物用足量的 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为___________ g。若上述混合物中含0.2mol Cu,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为___________ mol。
 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。(1)工业上可用
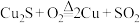 反应制取粗铜,该反应中
反应制取粗铜,该反应中 电子转移的数目为
电子转移的数目为(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:(3)现向Cu、
 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
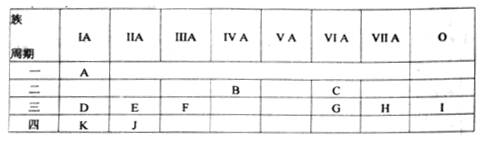
【推荐1】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)______ ,离子半径最小的是____ (写元素符号)。
(2)J的简单离子的结构示意图__________ 。
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)____ 。
(4)比较G、H两元素的最高价氧化物对应水化物的酸性______ (写化学式,下同)。比较C、G两元素的气态氢化物稳定性_________ 。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)
(2)J的简单离子的结构示意图
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)
(4)比较G、H两元素的最高价氧化物对应水化物的酸性
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】下表列出了7种短周期元素在元素周期表中的相对位置,其中元素①的最低负化合价的绝对值与其原子最外层电子数相等,元素⑤是地壳中含量最多的金属元素。
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是_______ 。
(2)上述7中元素中,非金属性最强的是______ (填元素符号);最高价氧化物对应水化物中,碱性最强的物质的化学式是_______ 。
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是________ 。
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是_______________ 。
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是_______ 。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是_______ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是
(2)上述7中元素中,非金属性最强的是
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】现有a~i 9种短周期元素,它们在同期表中的位置如下,请据此回答下列问题:(请用具体的元素符号及化学用语作答)
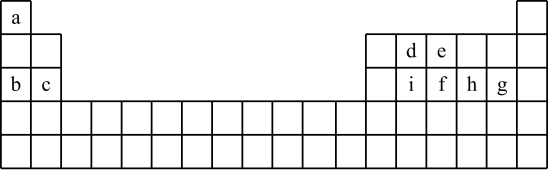
(1)a~i元素中,金属性最强的是________ ,最高价氧化物对应水化物中,酸性最强的物质是___________ 。g所在族的元素形成的氢化物中沸点最低的是____________________ 。
(2)比较b、e、g简单离子半径的大小___________________ (用离子符号作答)。
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式__________________ 、___________________ 。
(4)用一个化学反应方程式表示d的非金属性强于i_______________________________ 。
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是______ (填序号)。
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号_________ ;镓(Ga)与As同周期,最外层有3个电子,Ga与As可以形成一种新型化合物半导体材料,其性能更优越。这种新型化合物化学式为____________________ 。
(6)c与a形成的化合物的电子式为___________ ,用电子式表示a与h形成a2h的过程__________________________________________ 。
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式_________________________________ 。

(1)a~i元素中,金属性最强的是
(2)比较b、e、g简单离子半径的大小
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式
(4)用一个化学反应方程式表示d的非金属性强于i
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号
(6)c与a形成的化合物的电子式为
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.A、D同主族,C、E同主族,D、E、F同周期.A、B的原子最外层电子数之和与C原子的最外层电子数相等.A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子(题中的字母只代表元素代号,与实际元素符号无关).
请回答下列问题:
(1)A~F六种元素原子,原子半径最大的是 (填对应的元素符号).
(2)A与B两种元素组成一种阳离子,该离子符号为 .
(3)C、D两种元素组成的化合物的化学式是 .
(4)E、F两种元素中非金属性较强的是 ,能够证明这一结论的化学事实是 .
请回答下列问题:
(1)A~F六种元素原子,原子半径最大的是 (填对应的元素符号).
(2)A与B两种元素组成一种阳离子,该离子符号为 .
(3)C、D两种元素组成的化合物的化学式是 .
(4)E、F两种元素中非金属性较强的是 ,能够证明这一结论的化学事实是 .
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】I.摩擦剂是牙膏的主体成分,SiO2是一种常见的摩擦剂。
(1)Si在元素周期表中的位置是_______ 。
(2)根据用途推测SiO2在水中的溶解性:_______ (填“易溶”或“难溶”)。
(3)制备SiO2的方法如图:
Na2SiO3溶液 H2SiO3沉淀
H2SiO3沉淀 SiO2
SiO2
①写出反应I的离子方程式_______ 。
②比较酸性强弱:H2SO4_______ H2SiO3(填“>”或“<”)。
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF2)。锡的原子结构示意图如图。

下列说法正确的是_______ (填序号)。
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
II.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
(1)K2FeO4中铁元素的化合价为_______ 。
(2)制备K2FeO4需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于K2FeO4的说法中,不正确 的是_______ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)将K2FeO4与水反应的化学方程式补充完整: 4K2FeO4 + H2O = Fe(OH)3(胶体)+_____ + KOH
______
(5)消毒净化500 m3水,至少需要K2FeO4的质量为_______ kg。
(1)Si在元素周期表中的位置是
(2)根据用途推测SiO2在水中的溶解性:
(3)制备SiO2的方法如图:
Na2SiO3溶液
 H2SiO3沉淀
H2SiO3沉淀 SiO2
SiO2①写出反应I的离子方程式
②比较酸性强弱:H2SO4
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF2)。锡的原子结构示意图如图。

下列说法正确的是
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
II.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
| 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1 L水投放5 mg K2FeO4即可达到卫生标准 |
(2)制备K2FeO4需要在
(3)下列关于K2FeO4的说法中,
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)将K2FeO4与水反应的化学方程式补充完整: 4K2FeO4 + H2O = Fe(OH)3(胶体)+_____ + KOH
(5)消毒净化500 m3水,至少需要K2FeO4的质量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
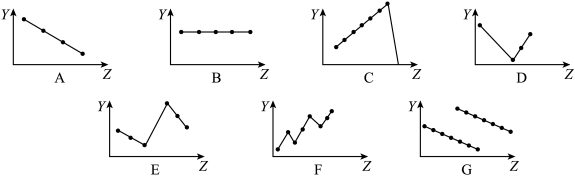
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数_____________ 。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径_______ 。
③第二、三周期主族元素随原子序数递增原子半径的变化___________ 。
(2)已知某单核粒子的结构示意图为:
①当x-y=10时,该粒子为______ (填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_______ 。
(3)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。
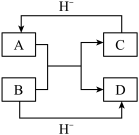
请写出:A的化学式_______ (写一种);D的化学式________ 。
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径
③第二、三周期主族元素随原子序数递增原子半径的变化
(2)已知某单核粒子的结构示意图为:

①当x-y=10时,该粒子为
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是
(3)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。

请写出:A的化学式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】砷(As)及其化合物与生产、生活密切相关,广泛应用在杀虫剂以及药物中。回答下列问题:
(1)砷是第四周期VA族元素。下列关于第VA族元素及其化合物的说法不正确的是_______ (填序号)。
a.沸点:PH3<NH3
b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(2)工业生产中常用“古氏试砷法”检验微量砷,其反应原理为:
①将含砷化合物转化为具有极强还原性的AsH3;
②AsH3与AgNO3溶液反应产生As2O3与另一种固体,该反应的离子方程式为_____________ 。
(3)砷及其化合物几乎都有毒,通常+3价砷化合物毒性强于+5价砷化合物。海产品中含有微量+5价砷化合物,食用海鲜后不能马上进食水果的原因是________________________________ 。
(4)砷酸(H3AsO4)可用于制造杀虫剂、药物。As2O3溶于稀硝酸中可得砷酸,此反应的化学方程式为________________________________ 。
(5)利用单质铁处理水体砷污染的原理为:单质铁在水体中被氧化腐蚀得到水合氧化铁[Fe(OH)3和FeOOH],吸附沉降砷的化合物。在其它条件一定时,调节水样的pH,得到除砷效率曲线如图所示。

①请解释水样酸性较强时,除砷效率较低的原因是_____________________ 。
②国家饮用水标准规定水中砷的含量应低于0.05mg·L-1(1mg=1000μg)。某水样中含砷总浓度为100μg·L-1,若控制水样的pH=6,出水后的砷浓度_________________ (填“能”或“否”)达到饮用水标准。
(1)砷是第四周期VA族元素。下列关于第VA族元素及其化合物的说法不正确的是
a.沸点:PH3<NH3
b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(2)工业生产中常用“古氏试砷法”检验微量砷,其反应原理为:
①将含砷化合物转化为具有极强还原性的AsH3;
②AsH3与AgNO3溶液反应产生As2O3与另一种固体,该反应的离子方程式为
(3)砷及其化合物几乎都有毒,通常+3价砷化合物毒性强于+5价砷化合物。海产品中含有微量+5价砷化合物,食用海鲜后不能马上进食水果的原因是
(4)砷酸(H3AsO4)可用于制造杀虫剂、药物。As2O3溶于稀硝酸中可得砷酸,此反应的化学方程式为
(5)利用单质铁处理水体砷污染的原理为:单质铁在水体中被氧化腐蚀得到水合氧化铁[Fe(OH)3和FeOOH],吸附沉降砷的化合物。在其它条件一定时,调节水样的pH,得到除砷效率曲线如图所示。

①请解释水样酸性较强时,除砷效率较低的原因是
②国家饮用水标准规定水中砷的含量应低于0.05mg·L-1(1mg=1000μg)。某水样中含砷总浓度为100μg·L-1,若控制水样的pH=6,出水后的砷浓度
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.A、D同主族,C、E同主族,D、E、F同周期.A、B的原子最外层电子数之和与C原子的最外层电子数相等.A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子(题中的字母只代表元素代号,与实际元素符号无关).
请回答下列问题:
(1)A~F六种元素原子,原子半径最大的是 (填对应的元素符号).
(2)A与B两种元素组成一种阳离子,该离子符号为 .
(3)C、D两种元素组成的化合物的化学式是 .
(4)E、F两种元素中非金属性较强的是 ,能够证明这一结论的化学事实是 .
请回答下列问题:
(1)A~F六种元素原子,原子半径最大的是 (填对应的元素符号).
(2)A与B两种元素组成一种阳离子,该离子符号为 .
(3)C、D两种元素组成的化合物的化学式是 .
(4)E、F两种元素中非金属性较强的是 ,能够证明这一结论的化学事实是 .
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而引发中毒的事故。
(1)两种日化产品的主要成分中都含有氯元素,该元素在元素周期表中的位置是_______________ 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:________________________ 。
(3)洁厕液的主要成分是盐酸.下列关于卤化氢性质的比较中,错误的是________ 。
A.酸性:
B.稳定性:
C.熔点:
D.还原性:
(4)常温下,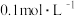 的NaClO溶液的
的NaClO溶液的 ,原因是
,原因是________________________________ (用方程式解释).常温下HClO的电离平衡常数为________ 。洁厕液与84消毒液混合后会生成有毒的氯气,写出该反应的离子方程式:____________________________ 。
(5)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产:
①在碱性条件下,利用NaClO氧化硝酸铁,制得K2FeO4,该反应的离子方程式为___________ 。
②K2FeO4与KOH反应生成 。K2FeO4在水溶液中易水解:
。K2FeO4在水溶液中易水解: ,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用________ 溶液(填序号)。
A.水
B.NH4Cl、2-甲基-2-丙醇
C.Fe(NO3)3、2-甲基-2-丙醇
D.CH3COONa、2-甲基-2-丙醇
(6)消毒效率是单位质量物质得到的电子数,则 与NaClO两种消毒剂的消毒效率之比为
与NaClO两种消毒剂的消毒效率之比为________ 。
(1)两种日化产品的主要成分中都含有氯元素,该元素在元素周期表中的位置是
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:
(3)洁厕液的主要成分是盐酸.下列关于卤化氢性质的比较中,错误的是
A.酸性:

B.稳定性:

C.熔点:

D.还原性:

(4)常温下,
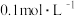 的NaClO溶液的
的NaClO溶液的 ,原因是
,原因是(5)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产:
①在碱性条件下,利用NaClO氧化硝酸铁,制得K2FeO4,该反应的离子方程式为
②K2FeO4与KOH反应生成
 。K2FeO4在水溶液中易水解:
。K2FeO4在水溶液中易水解: ,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用A.水
B.NH4Cl、2-甲基-2-丙醇
C.Fe(NO3)3、2-甲基-2-丙醇
D.CH3COONa、2-甲基-2-丙醇
(6)消毒效率是单位质量物质得到的电子数,则
 与NaClO两种消毒剂的消毒效率之比为
与NaClO两种消毒剂的消毒效率之比为
您最近一年使用:0次



