元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在元素周期表中的位置:___________ ,有关Be性质的推断不正确的是___________ (填序号)。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时, 溶液的
溶液的
(2)已知: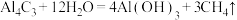 ,写出
,写出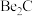 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):___________
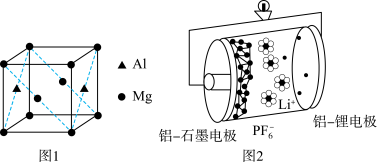
(3)基态铝原子的价电子排布式为___________ ,镁铝合金经过高温淬火获得一种储钠材料,用___________ 法测定其晶胞结构如图1所示,图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___________ ,该立方晶胞的晶胞的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为___________ pm。(列出计算式,可不化简)。
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为: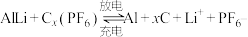 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为___________ ,充电时,应将铝-石墨电极与外接电源的___________ 极相连。
(1)Be元素在元素周期表中的位置:
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时,
 溶液的
溶液的
(2)已知:
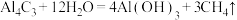 ,写出
,写出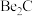 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):(3)基态铝原子的价电子排布式为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为:
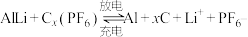 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为
2023·天津河北·一模 查看更多[2]
更新时间:2023-04-08 15:14:56
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】某课外活动小组同学用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应为____________________________________ 。
(2)若开始时开关K与b连接,则B极的电极反应为______ ,总反应的离子方程式为________ 。有关上述实验,下列说法正确的是(填序号)___ 。
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应为______ 。
此时通过阴离子交换膜的离子数______ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②通电开始后,阴极附近溶液pH会增大,请简述原因_______________ 。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应为_____________________ 。

(1)若开始时开关K与a连接,则B极的电极反应为
(2)若开始时开关K与b连接,则B极的电极反应为
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应为
此时通过阴离子交换膜的离子数
②通电开始后,阴极附近溶液pH会增大,请简述原因
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】钠离子电池因其原材料丰富、资源成本低廉及安全环保等突出优点,在电化学规模储能领域和低速电动车领域中具有广阔的应用前景。某钠离子电池结构如图所示,钠离子电池总反应方程式为NaxTMO2+Na1-xC NaTMO2 +C,下列说法不正确的是
NaTMO2 +C,下列说法不正确的是___________
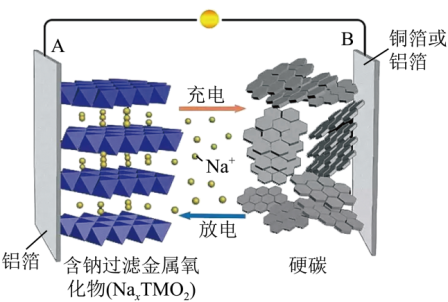
A.充电时,电极B与外接直流电源的负极相连
B.充电时,Na+得电子成为Na嵌入硬碳中
C.放电时,外电路中每转移0.2mole-,理论上硬碳质量增加4.6g
D.放电时,Na+从硬碳中脱嵌,经过电解质溶液嵌入含钠过渡金属氧化物中
E.充电时,阳极反应为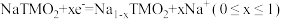
F.放电时,电极A为正极,电极反应式: NaxTMO2+(1- x)Na+ +(1- x)e- = NaTMO2
 NaTMO2 +C,下列说法不正确的是
NaTMO2 +C,下列说法不正确的是
A.充电时,电极B与外接直流电源的负极相连
B.充电时,Na+得电子成为Na嵌入硬碳中
C.放电时,外电路中每转移0.2mole-,理论上硬碳质量增加4.6g
D.放电时,Na+从硬碳中脱嵌,经过电解质溶液嵌入含钠过渡金属氧化物中
E.充电时,阳极反应为
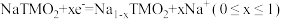
F.放电时,电极A为正极,电极反应式: NaxTMO2+(1- x)Na+ +(1- x)e- = NaTMO2
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】按要求回答下列问题。
(1)有人研究了用电化学方法把 转化为
转化为 ,其原理如图1所示:
,其原理如图1所示:
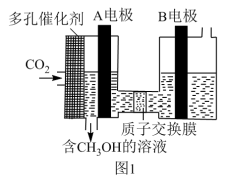
则图中A电极接电源_______ 极。已知B电极为惰性电极,则在水溶液中,该极的电极反应式为_______ 。
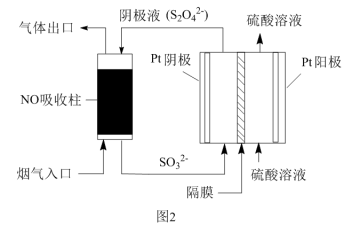
(2)以连二亚硫酸盐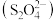 为还原剂脱除烟气中的
为还原剂脱除烟气中的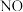 ,并通过电解再生,装置如图2所示。阴极的电极反应式为
,并通过电解再生,装置如图2所示。阴极的电极反应式为_______ ,电解槽中的隔膜为_______ (填“阳”或“阴”)离子交换膜。
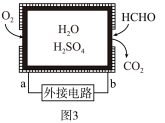
(3)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工作原理如图3所示,b极的电极反应式为_______ ,当电路中转移 电子时,传感器内参加反应的甲醛
电子时,传感器内参加反应的甲醛 为
为_______  。
。
(1)有人研究了用电化学方法把
 转化为
转化为 ,其原理如图1所示:
,其原理如图1所示:
则图中A电极接电源
(2)以连二亚硫酸盐
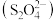 为还原剂脱除烟气中的
为还原剂脱除烟气中的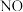 ,并通过电解再生,装置如图2所示。阴极的电极反应式为
,并通过电解再生,装置如图2所示。阴极的电极反应式为
(3)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工作原理如图3所示,b极的电极反应式为
 电子时,传感器内参加反应的甲醛
电子时,传感器内参加反应的甲醛 为
为 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】下表为元素周期表的一部分,请用化学用语回答有关问题:
(1)①和⑧的元素符号是______ 和______ ;
(2)元素⑥形成的氢化物的电子式是______ ;
(3)表中能形成两性氢氧化物的元素是______ (填写元素符号),请写出该元素的氢氧化物与⑨最高价氧化物对应的水化物发生反应的化学方程式_______________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ⑨ | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①和⑧的元素符号是
(2)元素⑥形成的氢化物的电子式是
(3)表中能形成两性氢氧化物的元素是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】下图是元素周期表的一部分。
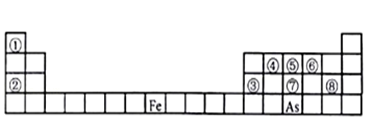
Ⅰ、用化学用语回答下列问题:
(1)由②、⑥两元素形成的强氧化性物质的电子式为_______ ,由①、⑤两元素构成的10电子化合物的形成过程为_______ 。
(2)⑦、⑧的最高价含氧酸的酸性较弱的是_______ 。(化学式表示)
(3)As在元素周期表中位置为__ ;氢化物的沸点:NH3 _______ AsH3(填“>”或“<”)
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_______ ,当消耗75g还原剂时,电子转移了__ mol。
Ⅱ、A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如下图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。
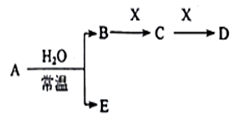
(1)A与水反应的化学方程式为_______ 。
(2)工业上常用CO热还原法冶炼X,写出其化学方程式_______ 。
(3)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式_______ 。
Ⅲ、由①、⑤、⑥、S和Fe五种元素组成的相对分子质量为392的化合物B,B中含有结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
(1)由实验a、b推知B溶液中含有的离子为_______ ;
(2)B的化学式为_______ 。

Ⅰ、用化学用语回答下列问题:
(1)由②、⑥两元素形成的强氧化性物质的电子式为
(2)⑦、⑧的最高价含氧酸的酸性较弱的是
(3)As在元素周期表中位置为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
Ⅱ、A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如下图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。

(1)A与水反应的化学方程式为
(2)工业上常用CO热还原法冶炼X,写出其化学方程式
(3)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式
Ⅲ、由①、⑤、⑥、S和Fe五种元素组成的相对分子质量为392的化合物B,B中含有结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
(1)由实验a、b推知B溶液中含有的离子为
(2)B的化学式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】下表列出了7种短周期元素在元素周期表中的相对位置,其中元素①的最低负化合价的绝对值与其原子最外层电子数相等,元素⑤是地壳中含量最多的金属元素。
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是_______ 。
(2)上述7中元素中,非金属性最强的是______ (填元素符号);最高价氧化物对应水化物中,碱性最强的物质的化学式是_______ 。
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是________ 。
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是_______________ 。
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是_______ 。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是_______ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是
(2)上述7中元素中,非金属性最强的是
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】关于物质结构与性质的内在联系,请回答下列问题:
(1)已知Se与O同族,基态Se原子价层电子的运动状态有______ 种,基态O原子的电子排布式不能表示为1s22s22p 2p
2p ,因为这违背了
,因为这违背了______ (填选项)。
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l) SO2++SO
SO2++SO 。SO2+中的σ键和π键数目之比为
。SO2+中的σ键和π键数目之比为______ ,SO2的空间构型为______ 。
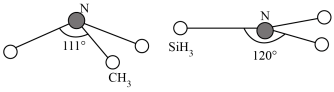
(3)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3(平面形)的结构如图所示,则二者中N的杂化方式分别为______ 。更易形成配合物的是______ 。______ 。______ g•cm-3(用含NA、a、b的式子表示)。
(1)已知Se与O同族,基态Se原子价层电子的运动状态有
 2p
2p ,因为这违背了
,因为这违背了A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l)
 SO2++SO
SO2++SO 。SO2+中的σ键和π键数目之比为
。SO2+中的σ键和π键数目之比为(3)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3(平面形)的结构如图所示,则二者中N的杂化方式分别为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】金属锡及其化合物在生产和科研中应用广泛。回答下列问题:
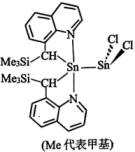
(1)某种含锡的有机金属化合物的结构如图所示。已知烷基配位体以C、N整合形式键合于Sn原子。_______ ,在周期表中的位置为_______ ,C、Si、Cl电负性由大到小的顺序为_______ 。
②该化合物中共有_______ 种杂化方式;提供电子对形成配位键的原子是_______ 。
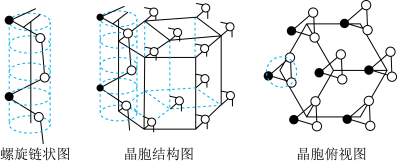
(2)一种含锡的多元金属硫化物的晶胞结构为四方晶系,已知金属原子均呈四面体配位,晶胞棱边夹角均为90°,其结构可看作是由两个立方体A、B上下堆叠而成。如图,甲为A的体对角线投影图,乙为B的沿y轴方向的投影图。A中Fe、Sn位置互换即为B。_______ ,晶胞中Sn的配位数与Cu的配位数之比为_______ 。
②立方体A、B棱长均为a pm,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。晶胞中部分原子的分数坐标为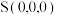 、
、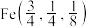 ,则晶胞中Sn原子的分数坐标为
,则晶胞中Sn原子的分数坐标为_______ ;晶胞中Sn原子和Cu原子间的最短距离为_______ pm。
(1)某种含锡的有机金属化合物的结构如图所示。已知烷基配位体以C、N整合形式键合于Sn原子。
②该化合物中共有
(2)一种含锡的多元金属硫化物的晶胞结构为四方晶系,已知金属原子均呈四面体配位,晶胞棱边夹角均为90°,其结构可看作是由两个立方体A、B上下堆叠而成。如图,甲为A的体对角线投影图,乙为B的沿y轴方向的投影图。A中Fe、Sn位置互换即为B。

②立方体A、B棱长均为a pm,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。晶胞中部分原子的分数坐标为
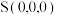 、
、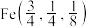 ,则晶胞中Sn原子的分数坐标为
,则晶胞中Sn原子的分数坐标为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的价电子排布式为___ 。
(2)磷的一种同素异形体——白磷(P4)的空间构型为___ ,其键角为__ ,推测其在CS2中的溶解度___ (填“大于”或“小于”)在水中的溶解度。
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:___ 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为___ 、__ ,A的中心原子杂化轨道类型为___ 。

(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是__ (填元素符号)。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:__ 。
(1)基态P原子的价电子排布式为
(2)磷的一种同素异形体——白磷(P4)的空间构型为
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为

(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:
| 物质 | BN | AlN | GaN |
| 熔点/℃ | 3000 | 2200 | 1700 |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】根据元素周期表回答下列问题:
(1)写出元素Cu的基态原子的电子排布式:____________________ 。
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有________ 对。此元素A原子与O的第一电离能的相对大小为:A________ O(填“<”“>”或“=”)。
(3)元素C形成的最高价氧化物中含有________ 个π键。C和Cl形成化合物的电子式为_____________ ,此化合物中C的杂化方式为________ 。
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是________ ,假设晶胞的边长为d cm、密度为ρ g·cm-3,则元素钒的相对原子质量为_____________ (NA为阿伏伽德罗常数)。

(1)写出元素Cu的基态原子的电子排布式:
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有
(3)元素C形成的最高价氧化物中含有
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O] 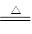 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
(1)铁元素在元素周期表中的位置为________ ,其价层电子排布图为________ 。
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为________ 。“摩尔盐”的分解产物中属于非极性分子的化合物是________ 。
(3)NH3的沸点比N2O的沸点________ (填“高”或“低”),其主要原因是________ 。
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为________ ,与CN—互为等电子体的单质的分子式为_________ 。HCN分子中σ键和π键的个数之比为________ 。
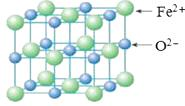
(5)FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为________ ,若该晶胞边长为acm,则该晶胞密度为________ g/cm3。
 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题: (1)铁元素在元素周期表中的位置为
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为
(3)NH3的沸点比N2O的沸点
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为
(5)FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)B元素的基态原子的价电子排布图为_____ ,第二周期中第一电离比B小的元素为______ 。
(2)三氟化硼常用作有机反应的催化剂,其分子的立体构型为______ ,中心原子的杂化类型为________ 。
(3)B的一种天然矿藏化学式为Na2[B4O5(OH)4]·8H2O,其阴离子结构单元是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,结构式如图1,该阴离子含配位键,请在下图中用“→”标出其中的配位键。该阴离子可相互结合形成链状结构,其可能的原因是___________ 。

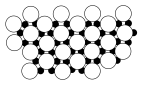
(4)科学家发现硼化镁在39K时有超导性,理想的硼化镁晶体是镁原子和硼原子是分层排布,即一层镁一层硼相间排列。下图是该晶体微观结构中取出的部分原子沿z轴方向的投影(白球是镁,黑球是硼)。则硼化镁的化学式为___________ 。
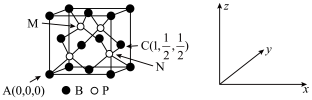
(5)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的___ (选填“立方体”“正四面体”或“正八面体”)空隙。建立如图所示坐标系,可得晶胞中A、C处原子的分数坐标,则M,N处的P原子分数坐标分别为_________ ,_________ ,若晶胞中硼原子和磷原子之间的最近核间距为apm,则晶胞边长为___________ cm。
(1)B元素的基态原子的价电子排布图为
(2)三氟化硼常用作有机反应的催化剂,其分子的立体构型为
(3)B的一种天然矿藏化学式为Na2[B4O5(OH)4]·8H2O,其阴离子结构单元是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,结构式如图1,该阴离子含配位键,请在下图中用“→”标出其中的配位键。该阴离子可相互结合形成链状结构,其可能的原因是

(4)科学家发现硼化镁在39K时有超导性,理想的硼化镁晶体是镁原子和硼原子是分层排布,即一层镁一层硼相间排列。下图是该晶体微观结构中取出的部分原子沿z轴方向的投影(白球是镁,黑球是硼)。则硼化镁的化学式为

(5)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的

您最近一年使用:0次



