回答下列问题:
(1)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为_______ 。SiCl4可发生水解反应,机理如下:
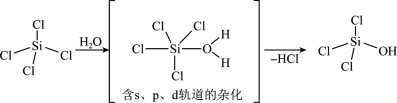
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为_______ (填标号)。
(2)四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
请回答下列问题:
①元素Z位于周期表中第_______ 周期_______ 族;
②X、Y两元素的氢化物中,水溶液呈碱性的是_______ (写化学式)
③Y和Z的氢化物中,较稳定的是_______ (填化学式)。
④Y的最高价氧化物对应水化物的化学式为_______ 。
(1)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
| X | Y | |
| Z | W |
①元素Z位于周期表中第
②X、Y两元素的氢化物中,水溶液呈碱性的是
③Y和Z的氢化物中,较稳定的是
④Y的最高价氧化物对应水化物的化学式为
更新时间:2023/03/27 23:35:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,根据表中8种元素,用元素符号等化学用语填空。
(1)①~⑧元素中,金属性最强的是_________ (写元素符号)。
(2)①~⑧元素中,画出最稳定的元素的原子结构示意图_________ 。
(3)①~⑧元素中,最高价氧化物水化物酸性最强的物质是__________ (写化学式)。
(4)②、③、⑥所形成的简单离子,其半径由大到小的顺序是_________ (写离子符号)
| ⅠA族 | ⅡA族 | ⅢA族 | ⅣA族 | ⅤA族 | ⅥA族 | ⅦA族 | 0族 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①~⑧元素中,金属性最强的是
(2)①~⑧元素中,画出最稳定的元素的原子结构示意图
(3)①~⑧元素中,最高价氧化物水化物酸性最强的物质是
(4)②、③、⑥所形成的简单离子,其半径由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分, 表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)写出下列序号所代表的元素符号③_____ ;⑩______
(2)写出⑥的一种用途_________________ ;常温下可与表中_______ 单质反应(填化学式)
(3)元素④的原子结构示意图为________________________ ;
(4)⑤和⑨形成的化合物的化学式为:_____________ ;向该化合物的水溶液里逐滴滴入苛性钠溶液,现象为__________________________________________________ .
(5)②⑤⑦⑧的原子半径由大到小的顺序是__________________________ (用元素符号表示)
(6)将①⑤同时投入到水中,发生反应的化学方程式有:______________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑧ | ⑩ | ||||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑦ | ⑨ | ||
| 4 | ② | ④ |
(1)写出下列序号所代表的元素符号③
(2)写出⑥的一种用途
(3)元素④的原子结构示意图为
(4)⑤和⑨形成的化合物的化学式为:
(5)②⑤⑦⑧的原子半径由大到小的顺序是
(6)将①⑤同时投入到水中,发生反应的化学方程式有:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分。根据表中的9种元素,用元素符号或化学式填空:
(1)在①~⑨元素中,金属性最强的金属元素是________ 。
(2)在①~⑨元素中,最高价氧化物的水化物呈两性的元素是________ 。
(3)④、⑥、⑦、⑨所形成的单核离子中,半径最大的是________ (离子)。
(4)⑦和⑨可形成________ (填“离子”或“共价”)化合物。
(5)①可与氧原子形成两种常见氧化物,其中一种氧化物的原子组成为1:1,则其电子式________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在①~⑨元素中,最高价氧化物的水化物呈两性的元素是
(3)④、⑥、⑦、⑨所形成的单核离子中,半径最大的是
(4)⑦和⑨可形成
(5)①可与氧原子形成两种常见氧化物,其中一种氧化物的原子组成为1:1,则其电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】观察下列A、B、C、D、E五种粒子的结构示意图,回答有关问题。
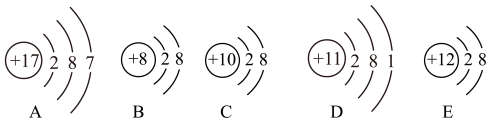
(1)图中离子属于金属元素离子的是________ (填离子符号),与图中非金属原子相对应的离子的结构示意图是____________ 。
(2)图中电子层结构相同的是__________ (填序号,下同),性质最稳定的是________ ,最容易失去电子的是________ ,最容易得到电子的是_________ 。
(3)图中可直接相互结合形成的化合物的化学式是_______ ,可经过得失电子后再相互结合形成的化合物的化学式是___________ 。

(1)图中离子属于金属元素离子的是
(2)图中电子层结构相同的是
(3)图中可直接相互结合形成的化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】A、B、C、D4 种元素的原子序数均小于20,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数是次外层的3倍;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1) 由此可知元素A、B、C、D分别为_____ 、_______ 、_________ 、________ 。
(2) 上述元素种任意三种组成的化合物中,既含离子键又含共价键的化合物的化学式为_________ 、_________ 、________ 。(至少写三种)
(3) 四种元素两两组合,能组成共价化合物的化学式有_______ 、_________ 、_________ 。(至少写三种)
(1) 由此可知元素A、B、C、D分别为
(2) 上述元素种任意三种组成的化合物中,既含离子键又含共价键的化合物的化学式为
(3) 四种元素两两组合,能组成共价化合物的化学式有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识,回答问题:
Ⅰ.在第三周期元素及其单质和化合物中,氧化性最强的单质是__________ ,还原性最强的单质是__________ ;最高价氧化物对应的水化物中,最强的酸是__________ ,最强的碱是_________ ,形成的两性氢氧化物是__________ ;化学性质最稳定的元素是__________ 。
Ⅱ.(1)A元素原子的核电荷数为8,其原子核内的质子数为__________ ,该元素原子的二价阴离子的核外电子数为_________ ,中子数是8的核素表示为__________ 。
(2)B元素原子的一价阳离子的核外有10个电子,质量数为23,该元素原子的原子核内中子数为__________ 。
(3)A、B形成1:1型化合物的相对分子质量是__________ 。
Ⅰ.在第三周期元素及其单质和化合物中,氧化性最强的单质是
Ⅱ.(1)A元素原子的核电荷数为8,其原子核内的质子数为
(2)B元素原子的一价阳离子的核外有10个电子,质量数为23,该元素原子的原子核内中子数为
(3)A、B形成1:1型化合物的相对分子质量是
您最近一年使用:0次
【推荐1】第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
(1)基态Se原子的价层电子轨道表示式为______ ,O3分子内的共价键类型为______ (填“极性共价键”或“非极性共价键”)。
(2)水丰富而独特的性质与其结构密切相关。
①下列事实可用“水分子间存在氢键”解释的是______ (填标号)。
a.冰的密度比水的小
b.水的沸点比硫化氢的沸点高
c.水的热稳定性比硫化氢强
d.水分子为极性分子
②酸溶于水可形成 ,
, 的电子式为
的电子式为______ 。判断 和
和 的键角大小;
的键角大小;
______ (填“>”或“<”) 。
。
(3)硫元素形成的化合物 广泛应用于医药、印染等行业,隔绝空气加热后可分解生成
广泛应用于医药、印染等行业,隔绝空气加热后可分解生成 、
、 、
、 、
、 及
及 。
。 中心原子
中心原子 的轨道杂化类型为
的轨道杂化类型为______ , 极易溶于水的原因是
极易溶于水的原因是____________ (任答一点)。
(4) 的空间结枃为
的空间结枃为______ 。
(1)基态Se原子的价层电子轨道表示式为
(2)水丰富而独特的性质与其结构密切相关。
①下列事实可用“水分子间存在氢键”解释的是
a.冰的密度比水的小
b.水的沸点比硫化氢的沸点高
c.水的热稳定性比硫化氢强
d.水分子为极性分子
②酸溶于水可形成
 ,
, 的电子式为
的电子式为 和
和 的键角大小;
的键角大小;
 。
。(3)硫元素形成的化合物
 广泛应用于医药、印染等行业,隔绝空气加热后可分解生成
广泛应用于医药、印染等行业,隔绝空气加热后可分解生成 、
、 、
、 、
、 及
及 。
。 中心原子
中心原子 的轨道杂化类型为
的轨道杂化类型为 极易溶于水的原因是
极易溶于水的原因是(4)
 的空间结枃为
的空间结枃为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为________ 个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为________ 。 的沸点比
的沸点比 高,原因是
高,原因是__________________________ 。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________ 杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为_____________________________________ 。
(1)氧元素基态原子核外未成对电子数为
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是(3)H+可与H2O形成H3O+,H3O+中O原子采用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】人体中含量位于前6名的元素依次是:氧、碳、X、氮、钙、磷。根据要求用以上元素完成下列填空:
(1)X是_______ (写元素符号,下同)。能量最高的亚层电子云呈球形的元素有________ 。
(2)形成化合物种类最多的元素的最简氢化物的电子式为_________ ;该分子为非极性分子的原因是________________________________ 。
(3)能证明C、N、O非金属性递变规律的事实是____________ 。
a.最高价氧化物对应水化物的酸性 b.单质与H2反应的难易程度
c.NO2、CO2和C3N4中元素的化合价 d.气态氢化物的稳定性
(4)氮元素的另一种气态氢化物肼可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为_____________ 。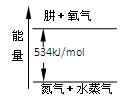
(1)X是
(2)形成化合物种类最多的元素的最简氢化物的电子式为
(3)能证明C、N、O非金属性递变规律的事实是
a.最高价氧化物对应水化物的酸性 b.单质与H2反应的难易程度
c.NO2、CO2和C3N4中元素的化合价 d.气态氢化物的稳定性
(4)氮元素的另一种气态氢化物肼可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的。肼燃烧时的能量变化如图所示,则该反应的热化学方程式为

您最近一年使用:0次