题型:单选题
难度:0.85
引用次数:1804
题号:18565944
下列热化学方程式正确的是
| 选项 | 已知条件 | 热化学方程式 |
| A | H2的燃烧热为a kJ∙mol−1 | H2(g)+Cl2(g) 2HCl(g) ΔH=−a kJ∙mol−1 2HCl(g) ΔH=−a kJ∙mol−1 |
| B | 1molSO2、0.5molO2完全反应后,放出热量98.3kJ | 2SO2(g)+O2(g)  2SO3(g) ΔH=−98.3 kJ∙mol−1 2SO3(g) ΔH=−98.3 kJ∙mol−1 |
| C | H+(aq)+OH-(aq)=H2O(l) ΔH=−57.3 kJ∙mol−1 | H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=−114.6 kJ∙mol−1 |
| D | 31g白磷比31g红磷能量多bkJ | P4(白磷,s) = 4P(红磷,s) ΔH=−4b kJ∙mol−1 |
| A.A | B.B | C.C | D.D |
更新时间:2023-03-30 18:25:18
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l) △H=−57.3 kJ∙mol−1,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的△H |
| B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量。则Fe(s)+S(s)=FeS(s) △H=−95.6 kJ∙mol−1 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=−38.6 kJ∙mol−1 2NH3(g) △H=−38.6 kJ∙mol−1 |
| D.相同条件下,在两个相同的恒容密闭容器中,2molN2和6molH2反应放出的热量是1molN2和3molH2反应放出的热量的2倍 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】某些微粒间相互作用的数据如下表所示:
根据表中数据,下列说法不正确 的是
微粒间相互作用 | 化学键 | 分子间作用力 | ||||||
|
|
|
|
|
|
| HCl | |
键能/范德华力强度 ( | 463 | 568 | 366 | 157 | 497 | 28.1 | 18.8 | 21.1 |
| A.上表的微粒间相互作用中有5种极性共价键,2种氢键 |
| B.键长:H-F<H-Br,但仅用上表数据无法比较两者与H-Cl的键长大小 |
C. 的 的 |
D.用上表数据可比较 与 与 的沸点高低 的沸点高低 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】如图所示,下列热化学方程式正确的是
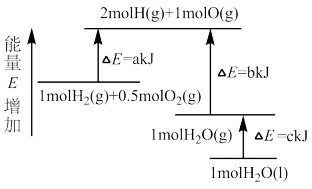

A. 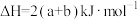 |
B.  |
C.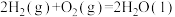 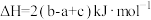 |
D.  |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】符合如图所示的化学反应的热化学方程式是
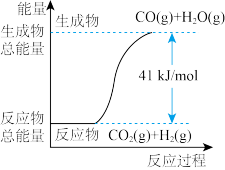

| A.CO+H2O=CO2+H2ΔH=+41 kJ·mol-1 |
| B.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol-1 |
| C.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41 kJ·mol-1 |
| D.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=-41 kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法或表示方法正确的是
| A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含1molCH3COOH与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
| D.由C(石墨)=C(金刚石) △H=+1.9kJ/mol可知,石墨比金刚石稳定 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关反应热的说法正确的是
| A.在化学反应过程中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量 |
| B.甲烷标准燃烧热△H=-890kJ/mol,则:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890kJ/mol |
| C.已知常温常压下HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol,则有H2SO4+Ba(OH)2=BaSO4+2H2O △H=-114.6kJ/mol |
| D.已知S(s)+O2(g) =SO2(g) △H=-Q1kJ/mol,S(g)+O2(g) =SO2(g) △H=-Q2kJ/mol,则Q1<Q2 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则下列热化学方程式中正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=+890kJ•mol-1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-222.5kJ•mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ•mol-1 |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=+222.5kJ•mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】1mol碳在氧气中完全燃烧生成气体,放出393kJ的热量,下列热化学方程式表示正确的是
| A.C (s) +1/2O2 (g) = CO(g) ΔH=-393kJ·molˉ1 |
| B.C + O2 = CO2 ΔH=-393kJ·molˉ1 |
| C.C (s) + O2 (g)=CO2 (g) ΔH=+393kJ·molˉ1 |
| D.C(s)+O2(g)=CO2(g) ΔH=-393kJ·molˉ1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列有关热化学方程式的叙述正确的是
| A.已知C(石墨,s)=C(金刚石,s) ΔH >0,则金刚石比石墨稳定 |
| B.已知S(g)+O2(g)=SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2,则ΔH1>ΔH2 |
| C.已知甲烷的燃烧热为890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=2CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol |
| D.已知中和热为ΔH=-57.3 kJ/mol,则含0.5 mol浓硫酸和足量稀NaOH溶液反应的放出57.3 kJ的热量 |
您最近半年使用:0次






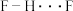
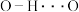
 )
)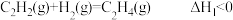
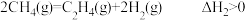
 、
、 、
、 由大到小的顺序是
由大到小的顺序是
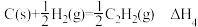

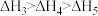
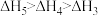


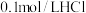 与某强碱稀溶液中和放出的热量随反应物的用量改变而改变,但中和反应反应热不变
与某强碱稀溶液中和放出的热量随反应物的用量改变而改变,但中和反应反应热不变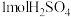 与
与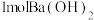 反应生成
反应生成 沉淀时放出的热叫做中和热
沉淀时放出的热叫做中和热

