写出下列反应的热化学方程式:
(1)1 mol C2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1 366.8 kJ热量:___________ 。
(2)1 mol C(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量:___________ 。
(3)1.7 g NH3(g)发生催化氧化反应生成气态产物,放出22.67 kJ的热量:___________ 。
(4)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,写出表示硫的燃烧热的热化学方程式:___________ 。
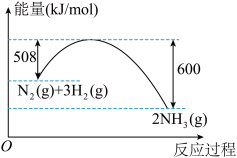
(5)如图是298 K、101 kPa时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为___________ 。
(1)1 mol C2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1 366.8 kJ热量:
(2)1 mol C(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量:
(3)1.7 g NH3(g)发生催化氧化反应生成气态产物,放出22.67 kJ的热量:
(4)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,写出表示硫的燃烧热的热化学方程式:
(5)如图是298 K、101 kPa时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为

更新时间:2023-04-04 14:54:30
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】化学反应中常伴随着能量变化。
I.将Al条打磨后,插入6 mol/L盐酸中。
(1)如果Al条不打磨,开始一段时间没有气泡冒出,用离子方程式说明其原因___________ 。
(2)该反应的能量变化可用下图中的___________ 表示(填序号)。___________ 。t2~t3速率变化的主要原因是___________ 。
(4)铝与某些金属氧化物在高热条件下发生的反应,同时放出巨大的热,铁路工人经常用铝热剂焊接铁轨,写出化学方程式___________ 。
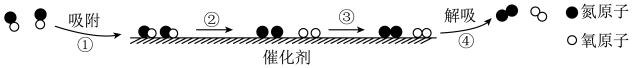
Ⅱ. 利用固体表面催化工艺进行NO分解的过程如下图所示。___________ 键断裂,此过程___________ (放出或者吸收)能量。
I.将Al条打磨后,插入6 mol/L盐酸中。
(1)如果Al条不打磨,开始一段时间没有气泡冒出,用离子方程式说明其原因
(2)该反应的能量变化可用下图中的


(4)铝与某些金属氧化物在高热条件下发生的反应,同时放出巨大的热,铁路工人经常用铝热剂焊接铁轨,写出化学方程式
Ⅱ. 利用固体表面催化工艺进行NO分解的过程如下图所示。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.化学反应伴随能量变化,获取化学反应中的能量有多条途径。
(1)下列反应中,属于放热反应且是氧化还原反应的是_______(填字母).
(2)如图为反应 的能量变化示意图。
的能量变化示意图。
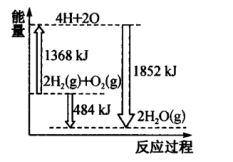
①由 和
和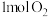 变成
变成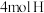 、
、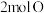 需要
需要_______ (“放出”或“吸收”)能量。
② 和
和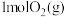 反应生成
反应生成 ,共放出
,共放出_______  能量。
能量。
Ⅱ.燃料电池在工作时,从负极连续通入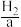 、
、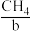 、
、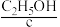 等燃料,从正极连续通入
等燃料,从正极连续通入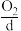 ,以
,以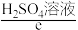 或
或 溶液为电解质溶液,发生反应生成
溶液为电解质溶液,发生反应生成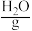 、
、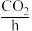 或
或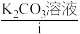 等,同时产生电能,目前已研制成功
等,同时产生电能,目前已研制成功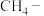 空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。
空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。
(3)在上述画横线的九种物质中,属于电解质的是_______ (填序号,下同);属于非电解质的是_______ 。
(4)用 和
和 组合形成的质子交换膜燃料电池的结构如图所示:
组合形成的质子交换膜燃料电池的结构如图所示:
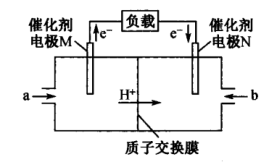
①电极M是_______ (填“正极”或“负极”),电极N的电极反应式为_______ 。
②若该燃料电池消耗 (标准状况下)
(标准状况下) ,则理论上电路中转移
,则理论上电路中转移_______  电子。
电子。
(1)下列反应中,属于放热反应且是氧化还原反应的是_______(填字母).
A. 与 与 反应 反应 | B. 的燃烧反应 的燃烧反应 | C.高温煅烧 | D.C与 反应 反应 |
 的能量变化示意图。
的能量变化示意图。
①由
 和
和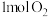 变成
变成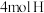 、
、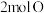 需要
需要②
 和
和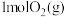 反应生成
反应生成 ,共放出
,共放出 能量。
能量。Ⅱ.燃料电池在工作时,从负极连续通入
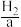 、
、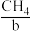 、
、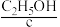 等燃料,从正极连续通入
等燃料,从正极连续通入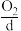 ,以
,以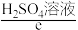 或
或 溶液为电解质溶液,发生反应生成
溶液为电解质溶液,发生反应生成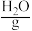 、
、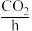 或
或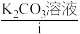 等,同时产生电能,目前已研制成功
等,同时产生电能,目前已研制成功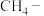 空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。
空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。(3)在上述画横线的九种物质中,属于电解质的是
(4)用
 和
和 组合形成的质子交换膜燃料电池的结构如图所示:
组合形成的质子交换膜燃料电池的结构如图所示:
①电极M是
②若该燃料电池消耗
 (标准状况下)
(标准状况下) ,则理论上电路中转移
,则理论上电路中转移 电子。
电子。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氢气是理想的能源,可由天然气和水反应制备,其主要反应为 ,反应过程中能量变化如图1所示:
,反应过程中能量变化如图1所示:
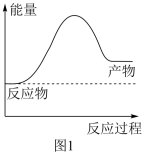
(1)该反应是___________ (填“吸热”或“放热”)反应。
(2)某温度下,在 恒容密闭容器中充入
恒容密闭容器中充入 和
和 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图2所示。
的物质的量变化如图2所示。
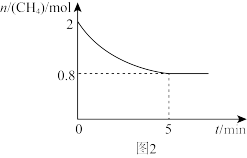
① 前,该反应的正反应速率
前,该反应的正反应速率___________ (填“大于”、“小于”或“等于”)逆反应速率,逆反应速率不断___________ (填“增大”或“减小”)。
②下列能说明该反应已达到化学平衡状态的是___________ (填字母)。
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内, 键断裂的同时有
键断裂的同时有 键断裂
键断裂
③ 内,以
内,以 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为___________  ,
, 时,混合气体中
时,混合气体中 的体积分数为
的体积分数为___________  (精确到
(精确到 )。
)。
④若要加快化学反应速率,可采用的方法是___________ (填“升高”或“降低”)温度。
 ,反应过程中能量变化如图1所示:
,反应过程中能量变化如图1所示:
(1)该反应是
(2)某温度下,在
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图2所示。
的物质的量变化如图2所示。
①
 前,该反应的正反应速率
前,该反应的正反应速率②下列能说明该反应已达到化学平衡状态的是
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内,
 键断裂的同时有
键断裂的同时有 键断裂
键断裂③
 内,以
内,以 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为 ,
, 时,混合气体中
时,混合气体中 的体积分数为
的体积分数为 (精确到
(精确到 )。
)。④若要加快化学反应速率,可采用的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出温度为298K时,下列反应的热化学方程式:
(1)3molNO2(g)与1molH2O(l)反应生成HNO3(aq)和NO(g),放热138kJ。________________
(2)用CO还原1molFe2O3,放热24.8kJ。______________
(3)1molHgO(s)分解为液态汞和氧气,吸热90.7kJ。_________________
(1)3molNO2(g)与1molH2O(l)反应生成HNO3(aq)和NO(g),放热138kJ。
(2)用CO还原1molFe2O3,放热24.8kJ。
(3)1molHgO(s)分解为液态汞和氧气,吸热90.7kJ。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列反应的热化学方程式:
(1)N2和H2反应生成34g NH3,放出92kJ热量____________________ 。
(2)1molCH4(g)在O2中完全燃烧生成CO2和H2O(g),放出890.3kJ热量________ 。
(1)N2和H2反应生成34g NH3,放出92kJ热量
(2)1molCH4(g)在O2中完全燃烧生成CO2和H2O(g),放出890.3kJ热量
您最近一年使用:0次



