有关硫和氯及其化合物性质的比较,错误的是
| A.半径:S>Cl | B.非金属性:S<Cl |
| C.酸性:H2SO4>HClO4 | D.稳定性:H2S<HCl |
2023·上海崇明·二模 查看更多[2]
更新时间:2023-04-06 23:39:07
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列正确的是( )。
| A.碱性:Al(OH)3>NaOH |
| B.原子半径:Cl>S |
| C.第一电离能:Mg>Al |
| D.沸点:H2S>H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关性质的比较,不正确的是
| A.酸性强弱:HI>HBr>HCl | B.非金属性:O>S>Se |
| C.还原性强弱:Cl->Br->I- | D.酸性强弱:HClO4>H2SO4>H3PO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列氢化物中,用单质直接化合制取最容易的是
| A.HF | B.HCl | C.HBr | D.HI |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述不正确的是
| A.Na、Mg、Al元素最高化合价依次升高 |
| B.Li、Na、K元素的金属性依次增强 |
| C.P、S、Cl元素最高价氧化物对应的水化物酸性依次增强 |
| D.N、O、F原子的半径依次增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列说法中正确的组合是
①任何原子的核内均含质子和中子
②周期表中第16纵行所有元素的化合价都有+6价
③科学家在周期表中金属与非金属分界线处找到了半导体材料
④随着原子序数递增,碱金属元素的单质的密度依次增大
⑤带相反电荷离子之间的静电吸引叫做离子键
⑥同主族两种元素原子的核外电子数的差值可能为36
⑦同一周期的甲、乙两种元素,甲位于第IIA族,序数为x,乙位于第IIIA族,则乙的序数可能为x+10
⑧卤素单质和水反应的通式为:X2+H2O=HXO+HX
⑨Na2O和Na2O2中阴阳离子个数比都是1:2
①任何原子的核内均含质子和中子
②周期表中第16纵行所有元素的化合价都有+6价
③科学家在周期表中金属与非金属分界线处找到了半导体材料
④随着原子序数递增,碱金属元素的单质的密度依次增大
⑤带相反电荷离子之间的静电吸引叫做离子键
⑥同主族两种元素原子的核外电子数的差值可能为36
⑦同一周期的甲、乙两种元素,甲位于第IIA族,序数为x,乙位于第IIIA族,则乙的序数可能为x+10
⑧卤素单质和水反应的通式为:X2+H2O=HXO+HX
⑨Na2O和Na2O2中阴阳离子个数比都是1:2
| A.2项 | B.3项 | C.4项 | D.6项 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】用下列实验装置进行相应实验,下列有关说法正确的是
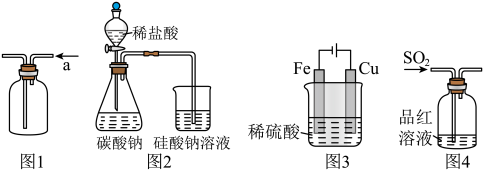

| A.用图1所示装置从a口进气收集纯净的CH2=CH2 |
| B.用图2所示装置中的实验现象能证明非金属性:Cl>C>Si |
| C.用图3所示装置可比较Fe、Cu的金属活动性 |
| D.用图4所示装置可以验证SO2的漂白性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】关于卤素(用X表示)的下列叙述中正确的是( )
| A.卤素单质与水反应均可用X2+H2O=HXO+HX表示 |
| B.由于Cl的非金属性比Br强,故盐酸的酸性比氢溴酸的酸性强 |
| C.卤素单质的密度从F2→I2随相对分子质量增大而增大 |
| D.卤素原子半径越小,对应的氢化物越不稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】某元素的+2价阳离子核外共有18个电子,则关于此元素的叙述正确的是
| A.原子半径比钾的原子半径大 | B.氯化物难溶于水 |
| C.离子半径比氯离子半径大 | D.碳酸盐难溶于水 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】W、X、Y、Z是原子序数依次增大的短周期主族元素,W、X、Z组成的一种化合物与蒸馏水按体积比3∶1混合后可用于杀灭新型冠状病毒,Y的一种单质在空气中含量最高。下列有关说法错误的是
A.简单离子的半径: |
B.简单氢化物的沸点: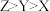 |
C.最高价氧化物对应水化物的酸性: |
| D.W、Y、Z既能形成共价化合物又能形成离子化合物 |
您最近一年使用:0次




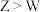

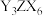 。下列说法正确的是
。下列说法正确的是


