下列对一些实验事实的理论解释,错误的是
| 选项 | 实验事实 | 理论解释 |
| A | 金属的导热性好 | 遍布晶体的自由电子受热加速运动 |
| B | 酸性: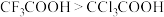 | 氟的电负性大于氯的电负性,F-C的极性大于C1-C的极性,使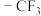 的极性大于 的极性大于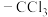 的极性,导致 的极性,导致 的羧基中的羟基的极性更大,更易电离出 的羧基中的羟基的极性更大,更易电离出 |
| C | 聚四氟乙烯的化学稳定性高于聚乙烯 | C-F的键能比C-H的键能大,键能越大,化学性质越稳定 |
| D | 对羟基苯甲醛(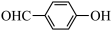 )比邻羟基苯甲醛( )比邻羟基苯甲醛(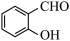 )的沸点低 )的沸点低 | 对羟基苯甲醛形成分子内氢键,邻羟基苯甲醛形成分子间氢键 |
| A.A | B.B | C.C | D.D |
更新时间:2023-04-15 14:51:42
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】以尿素 为原料制得的某化合物的结构如图所示,下列说法错误的是
为原料制得的某化合物的结构如图所示,下列说法错误的是
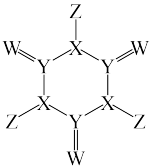
 为原料制得的某化合物的结构如图所示,下列说法错误的是
为原料制得的某化合物的结构如图所示,下列说法错误的是
A.电负性: |
B. 与 与 形成的分子都是极性分子 形成的分子都是极性分子 |
C.原子半径: |
D. 元素的简单气态氢化物中,沸点最高的是 元素的简单气态氢化物中,沸点最高的是 的气态氢化物 的气态氢化物 |
您最近半年使用:0次
【推荐2】下列各项叙述中,正确的是
| A.N、P、As的电负性随原子序数的增大而增大 |
| B.价电子排布为3d54s2的元素位于第四周期VA族,是p区元素 |
| C.2p和3p轨道形状均为哑铃形,能量也相等 |
D.氮原子的最外层电子排布图: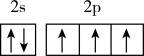 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.Na2O2和 NaOH 所含化学键类型完全相同 |
| B.CH4是含极性键的非极性分子 |
| C.CO2溶于水和干冰升华都只有分子间作用力改变 |
| D.NH3比 PH3稳定是因为 NH3分子间存在氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】羟胺 是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成
是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成 和
和 ,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
已知: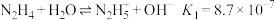 ;
;
 。
。
下列有关说法正确的是
 是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成
是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成 和
和 ,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。已知:
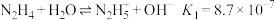 ;
; 。
。下列有关说法正确的是
| A.羟胺的碱性比氨强 |
B.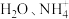 与 与 的VSEPR模型相同 的VSEPR模型相同 |
| C.羟胺极易溶于水主要原因是形成分子内氢键 |
D. 大小: 大小: |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】冰晶胞中水分子的空间排列方式与金刚石晶胞类似。下列有关冰晶胞说法正确的是
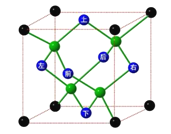

| A.冰分子间的氢键具有方向性和饱和性,是σ键 |
| B.每个冰晶胞平均含有4个水分子 |
| C.实验测得冰中氢键的作用力为18.5 kJ/mol,而冰的熔化热为5.0 kJ/mol,这说明冰熔化成水,氢键部分被破坏 |
| D.晶体冰与金刚石晶体硬度都很大,且都是原子晶体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中正确的是
A. 的酸性大于 的酸性大于 是因为 是因为 的极性大于 的极性大于 的极性,使 的极性,使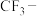 的极性大于 的极性大于 |
B.甲烷分子中心原子采取 杂化,键角107° 杂化,键角107° |
C. 是非极性分子,空间构型为直线形 是非极性分子,空间构型为直线形 |
D.氨气溶于水显碱性,大部分 与 与 以氢键(用“…”表示)结合形成 以氢键(用“…”表示)结合形成 分子。根据氨水的性质可推知 分子。根据氨水的性质可推知 的结构式为 的结构式为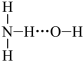 |
您最近半年使用:0次

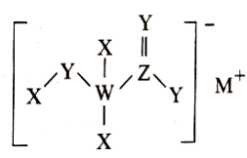
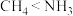
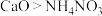
 内的
内的 键破坏
键破坏 稳定性强于
稳定性强于 的原因是
的原因是

