前四周期元素W、X、Y、Z的原子序数依次增大,且都不在同一周期。X的价电子排布式为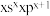 ,基态Y的最高能级的单电子数是W的3倍,Z与W中的单电子数和最外层电子数均相同,但两者族序数不同。下列说法正确的是
,基态Y的最高能级的单电子数是W的3倍,Z与W中的单电子数和最外层电子数均相同,但两者族序数不同。下列说法正确的是
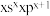 ,基态Y的最高能级的单电子数是W的3倍,Z与W中的单电子数和最外层电子数均相同,但两者族序数不同。下列说法正确的是
,基态Y的最高能级的单电子数是W的3倍,Z与W中的单电子数和最外层电子数均相同,但两者族序数不同。下列说法正确的是A.电负性比较: |
| B.Y元素的第一电离能高于其相邻元素 |
| C.Z元素在周期表中的位置可能为第四周期ⅥB族 |
| D.X的简单氢化物比Y的简单氢化物键角小 |
更新时间:2023-04-21 14:08:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】前20号主族元素W、X、Y、Z的原子序数依次增加。W的最外层电子数是内层电子数的3倍,W、X、Z最外层电子数之和为10;W与Y同族。下列说法不正确的是
| A.简单离子半径 X > W | B.W的氢化物沸点大于Y的氢化物沸点 |
| C.Z的氧化物中含离子键 | D.最高价氧化物对应水化物的碱性 Z > X |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 元素原子
元素原子 层电子数是
层电子数是 层电子数的4倍,
层电子数的4倍, 元素原子
元素原子 层电子数是
层电子数是 层电子数的
层电子数的 ,则
,则 、
、 两元素形成的稳定化合物的摩尔质量(
两元素形成的稳定化合物的摩尔质量( )可能为( )
)可能为( )
 元素原子
元素原子 层电子数是
层电子数是 层电子数的4倍,
层电子数的4倍, 元素原子
元素原子 层电子数是
层电子数是 层电子数的
层电子数的 ,则
,则 、
、 两元素形成的稳定化合物的摩尔质量(
两元素形成的稳定化合物的摩尔质量( )可能为( )
)可能为( )| A.40 | B.48 | C.58 | D.72 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】以下有关元素性质的说法正确的是
A.①  ,K,Rb ② ,K,Rb ②  ,P,As ③O,S,Se ④ ,P,As ③O,S,Se ④  ,P,Cl, 元素的电负性依次递增的是④ ,P,Cl, 元素的电负性依次递增的是④ |
| B.某元素的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,该元素一定在第三周期第IIA族 |
C.下列原子中,①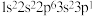 ② ② 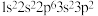 ③ ③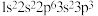 ④ ④ 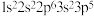 对应的第一电离能最大的是④ 对应的第一电离能最大的是④ |
D.以下原子中,①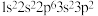 ② ② 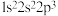 ③ ③ 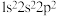 ④ ④ 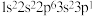 半径最大的是① 半径最大的是① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素X、Y、Z、W的原子序数依次增大,用表中信息判断下列说法正确的是
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | 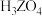 | |||
 溶液对应的pH(25℃) 溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
| A.元素的电负性:W<Z |
| B.简单离子半径:W<Y |
| C.元素的第一电离能:Z<W |
| D.X原子核外有7种不同运动状态的电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法中错误的是
| A.根据对角线规则,铍和铝的性质具有相似性 |
B.在H3O+、 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.P4和CH4都是正四面体分子且都含有非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】物质的结构决定其性质。下列实例与解释不相符的是
| 选项 | 实例 | 解释 |
| A |  比 比 酸性强 酸性强 |  的电负性比 的电负性比 的电负性强,吸电子能力强,使羟基的极性增强,更容易电离 的电负性强,吸电子能力强,使羟基的极性增强,更容易电离 |
| B |  的沸点高于 的沸点高于 |  的非金属性强于 的非金属性强于 |
| C |  比 比 的稳定性高 的稳定性高 |  键的键能比 键的键能比 键的键能大 键的键能大 |
| D |  在 在 中的溶解度大于在 中的溶解度大于在 中的溶解度 中的溶解度 | 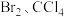 为非极性分子, 为非极性分子, 为极性分子 为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法中,能用键能的大小作为主要依据来解释的是
| A.常温常压下,氧单质呈气态,而硫单质呈固态 |
| B.醋酸、硝酸是挥发性酸,而硫酸是难挥发性酸 |
| C.Ne、Ar一般较难发生化学反应 |
| D.空气中氮气的化学性质比氧气稳定 |
您最近一年使用:0次
【推荐2】下列事实不能通过比较 和
和 的电负性解释的是
的电负性解释的是
A.键角: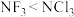 | B.键能: |
C.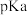 :三氟乙酸<三氯乙酸 :三氟乙酸<三氯乙酸 | D.分子极性: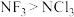 |
您最近一年使用:0次

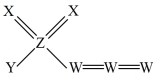
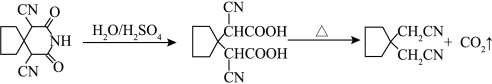
 分子的空间填充模型为
分子的空间填充模型为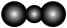
 分子中碳原子有2种杂化方式
分子中碳原子有2种杂化方式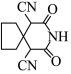 分子中有2个手性碳原子
分子中有2个手性碳原子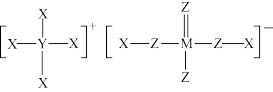

 是等电子体
是等电子体 结构
结构

