为探究某液态化合物X(仅含三种短周期元素)的组成和性质,某学习小组进行了如图实验:
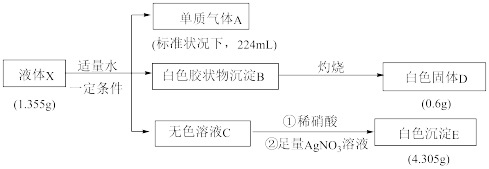
已知:白色固体D是光导纤维的主要成分。请回答:
(1)组成X的三种元素的名称是______ 。
(2)由白色固体D制备的光导纤维作通讯材料时,遇强碱性溶液易造成断路,请用离子方程式解释其原因______ 。
(3)写出液体X与适量水在一定条件下反应的化学方程式______ 。
(4)设计实验检验单质气体A______ 。

已知:白色固体D是光导纤维的主要成分。请回答:
(1)组成X的三种元素的名称是
(2)由白色固体D制备的光导纤维作通讯材料时,遇强碱性溶液易造成断路,请用离子方程式解释其原因
(3)写出液体X与适量水在一定条件下反应的化学方程式
(4)设计实验检验单质气体A
22-23高一下·浙江·期中 查看更多[3]
(已下线)【2023】【高一下】【期中考】【西子实验】【高中化学】【张太顺收集】(已下线)【2023】【高一下】【期中考】【9+1】【高中化学】【霍钰涵收集】浙江省9+1高中联盟2022-2023学年高一下学期4月期中化学试题
更新时间:2023-04-21 19:56:37
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】金属铝在酸性或碱性溶液中均可与 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:

请回答下列问题:
(1)实验室制备气体D的化学反应方程式为___________ ;
(2)气体D和F反应可生成盐,检验该盐中阳离子的方法是___________ ;
(3)向B溶液中通入过量的CO2,该反应的离子方程式是___________ ;
(4)除去气体C中的杂质气体E的化学方法是___________ (用化学方程式表示);
(5)Al与 在酸性条件下反应,Al与被还原的
在酸性条件下反应,Al与被还原的 的物质的量之比是
的物质的量之比是 ___________ ;
(6)在100 mL 0.5 mol/L 的A溶液中,加入100 mL NaOH溶液,得到1.56 g沉淀,所需NaOH溶液的物质的量浓度为___________ , ___________ 。
 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:
请回答下列问题:
(1)实验室制备气体D的化学反应方程式为
(2)气体D和F反应可生成盐,检验该盐中阳离子的方法是
(3)向B溶液中通入过量的CO2,该反应的离子方程式是
(4)除去气体C中的杂质气体E的化学方法是
(5)Al与
 在酸性条件下反应,Al与被还原的
在酸性条件下反应,Al与被还原的 的物质的量之比是
的物质的量之比是 (6)在100 mL 0.5 mol/L 的A溶液中,加入100 mL NaOH溶液,得到1.56 g沉淀,所需NaOH溶液的物质的量浓度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图的转化关系中,A、C、D是常见的气体单质,D气体在常温下呈黄绿色。F气体极易溶于水,且液态常作制冷剂,B的焰色反应为黄色。图中的部分反应产物或反应物已略去。

(1)写出G的化学式:______________ 。
(2)写出F的电子式:_______________ 。
(3)写出D单质和E溶液反应的离子方程式:_______________________ 。
(4)写出电解B溶液的化学方程式:_____________________________ 。

(1)写出G的化学式:
(2)写出F的电子式:
(3)写出D单质和E溶液反应的离子方程式:
(4)写出电解B溶液的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质.

(1)写出A、B、E、F的化学式:A________ ,B________ ,E________ ,F________ .
(2)写出反应①②③的化学方程式:
①______________________________________ ;
②______________________________________ ;
③______________________________________ 。

(1)写出A、B、E、F的化学式:A
(2)写出反应①②③的化学方程式:
①
②
③
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】镓是我国战略储备金属之一,在电子通信、新能源、芯片、军工等领域有着重要应用。某废渣粉煤灰主要含有Al2O3、SiO2,还有少量的Fe2O3、Ga2O3,一种从中提取镓的工艺流程如图:

样已知:①碱浸液中铝、镓元素分别以AlO 、GaO
、GaO 形式存在;
形式存在;
②常温下Al(OH)3(s)+OH-(aq) AlO
AlO (aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(1)粉煤灰需“球磨”至40目筛子(孔径为0.425mm的漏筛)漏出再焙烧,目的是_____ 。
(2)“焙烧”时碳酸钠与SiO2反应的化学方程式为_____ 。
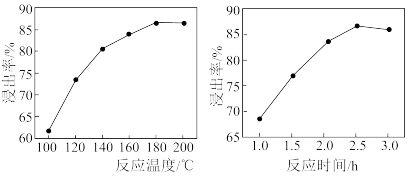
(3)“碱浸”时镓的浸出率随温度、时间变化如图所示,反应适宜的温度为_____ ,时间为____ 。
(4)“沉铝”时,物质X是_____ (填名称),过程中若要使铝元素在常温下恰好沉淀完全(含Al物质浓度恰好为10-5mol/L),计算此时溶液的c(OH-)=_____ (写出计算过程)。
(5)写出解析过程中GaO 被H2SO4解析为Ga3+的离子方程式:
被H2SO4解析为Ga3+的离子方程式:_____ 。

样已知:①碱浸液中铝、镓元素分别以AlO
 、GaO
、GaO 形式存在;
形式存在;②常温下Al(OH)3(s)+OH-(aq)
 AlO
AlO (aq)+2H2O(l),平衡常数K=100.63。回答下列问题:
(aq)+2H2O(l),平衡常数K=100.63。回答下列问题:(1)粉煤灰需“球磨”至40目筛子(孔径为0.425mm的漏筛)漏出再焙烧,目的是
(2)“焙烧”时碳酸钠与SiO2反应的化学方程式为
(3)“碱浸”时镓的浸出率随温度、时间变化如图所示,反应适宜的温度为

(4)“沉铝”时,物质X是
(5)写出解析过程中GaO
 被H2SO4解析为Ga3+的离子方程式:
被H2SO4解析为Ga3+的离子方程式:
您最近一年使用:0次
【推荐2】钌(Ru)是一种极其昂贵的稀有贵金属,广泛应用于电子、航空航天、石油化工、有机合成等领域。钉的矿产资源很少,因此从含钌废渣中回收钉尤为重要。某含钌的废渣主要成分为Ru、Pb、SiO2,回收钌的工艺流程如下:
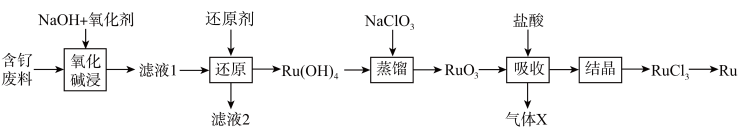
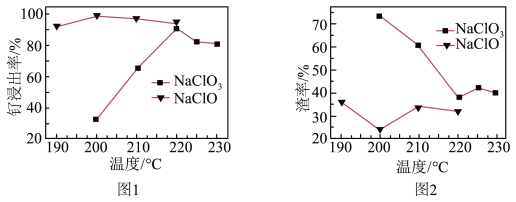
(1)“氧化碱浸”时,两种氧化剂在不同温度下对钌浸出率和渣率的影响分别如图1、图2所示,则适宜选择的氧化剂为___________ (填化学式);最佳反应温度为___________ 。
(2)滤液1中溶质的主要成分包括Na2RuO4、Na2SiO3、Na2PbO2等,均为可溶性盐。SiO2在氧化碱浸中发生反应的离子方程式为___________ 。
(3)“蒸馏”过程中氧化剂与还原剂的物质的量之比为___________ 。
(4)“转化”过程发生反应的化学方程式为___________ 。
(5)滤液1中含有铅等重金属元素,Na2S2O3可用于治疗铅等重金属离子中毒。现测定实验室某Na2S2O3产品纯度如下:称取0.80 g粗产品,用容量瓶配成250.00 mL溶液,取25.00 mL上述溶液置于锥形瓶中,用0.0250 mol·L-1的碘溶液与之反应(2 +I2=
+I2= +2I-),消耗碘溶液的体积为6.00 mL,则该产品中Na2S2O3的质量分数为
+2I-),消耗碘溶液的体积为6.00 mL,则该产品中Na2S2O3的质量分数为___________ 。(写出计算过程)

(1)“氧化碱浸”时,两种氧化剂在不同温度下对钌浸出率和渣率的影响分别如图1、图2所示,则适宜选择的氧化剂为

(2)滤液1中溶质的主要成分包括Na2RuO4、Na2SiO3、Na2PbO2等,均为可溶性盐。SiO2在氧化碱浸中发生反应的离子方程式为
(3)“蒸馏”过程中氧化剂与还原剂的物质的量之比为
(4)“转化”过程发生反应的化学方程式为
(5)滤液1中含有铅等重金属元素,Na2S2O3可用于治疗铅等重金属离子中毒。现测定实验室某Na2S2O3产品纯度如下:称取0.80 g粗产品,用容量瓶配成250.00 mL溶液,取25.00 mL上述溶液置于锥形瓶中,用0.0250 mol·L-1的碘溶液与之反应(2
 +I2=
+I2= +2I-),消耗碘溶液的体积为6.00 mL,则该产品中Na2S2O3的质量分数为
+2I-),消耗碘溶液的体积为6.00 mL,则该产品中Na2S2O3的质量分数为
您最近一年使用:0次
【推荐3】以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体FeSO4•7H2O的工艺流程如图:

(1)硫铁矿的主要成分FeS2中铁元素化合价为_____ ,由滤液得到绿矾晶体的操作是______ 。
(2)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式______ 。
(3)烟气中的SO2会污染环境,可用足量氢氧化钠溶液吸收,写出该反应的离子方程式______ 。
(4)写出检验滤液中阴离子的方法______ 。
(5)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是______ (写化学式)。
(6)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO +15Fe2++16H+。写出过程II反应的离子方程式
+15Fe2++16H+。写出过程II反应的离子方程式______ 。

(1)硫铁矿的主要成分FeS2中铁元素化合价为
(2)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式
(3)烟气中的SO2会污染环境,可用足量氢氧化钠溶液吸收,写出该反应的离子方程式
(4)写出检验滤液中阴离子的方法
(5)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是
(6)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO
 +15Fe2++16H+。写出过程II反应的离子方程式
+15Fe2++16H+。写出过程II反应的离子方程式
您最近一年使用:0次
【推荐1】为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的试验装置,按要求回答下列问题。
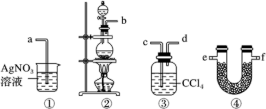
(1)请根据甲同学的意图,连接相应的装置,接口顺序:b接___________ ,___________ 接___________ ,___________ 接a。
(2)U形管中所盛试剂的化学式为___________ ②中反应的离子方程式___________
(3)乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某个装置之后再加装置⑤。你认为装置⑤应加在___________ 之后(填装置序号),瓶中可以放入___________ 。

(4)丙同学看到甲同学设计的装置后提出无需多加装置⑤,只需将原烧杯中AgNO3溶液换成其他溶液。你认为可将溶液换成___________ ,如果观察到___________ 的现象,则证明制Cl2时有HCl挥发出。

(1)请根据甲同学的意图,连接相应的装置,接口顺序:b接
(2)U形管中所盛试剂的化学式为
(3)乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某个装置之后再加装置⑤。你认为装置⑤应加在

(4)丙同学看到甲同学设计的装置后提出无需多加装置⑤,只需将原烧杯中AgNO3溶液换成其他溶液。你认为可将溶液换成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原反应是一类重要的化学反应,广泛存在于工农业生产、科学技术和日常生活中。
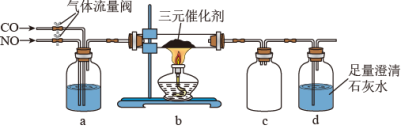
(1)汽车尾气系统中,有毒气体CO和NO在三元催化剂作用下生成无毒气体,某课外化学兴趣小组用如下装置模拟该转化过程。下列说法错误的是_______。
(2)某化工厂基于“绿色化学”理念设计了如下治污工艺流程,下列说法错误的是_______。

(3)某混合气体中可能含有 、
、 、
、 、NO、
、NO、 中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。
中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。
(4)氢化钠(NaH)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是_______ ;被氧化与被还原元素的物质的量之比为:_______ ;
(5)汽车剧烈碰撞时,安全气囊中发生反应: 。该反应中氧化产物与还原产物的质量比为
。该反应中氧化产物与还原产物的质量比为_______ ;若氧化产物比还原产物多19.6 g,则反应生成的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(6)高铁酸钠( ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式_______ 。
(1)汽车尾气系统中,有毒气体CO和NO在三元催化剂作用下生成无毒气体,某课外化学兴趣小组用如下装置模拟该转化过程。下列说法错误的是_______。

| A.a装置中试剂为浓硫酸,起干燥、观察流速及混合气体的作用 |
B.b装置的硬质玻璃管中发生反应 |
| C.c装置为安全瓶,能防止d装置中的澄清石灰水倒吸 |
D.d装置既可检验气体 ,又可吸收实验中的有害尾气 ,又可吸收实验中的有害尾气 |

A.该流程可用于吸收 |
B.由 转化为 转化为 的过程中,氧化剂和还原剂的物质的量之比为2∶1 的过程中,氧化剂和还原剂的物质的量之比为2∶1 |
C.该过程的总反应为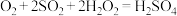 |
D. 可用做该反应过程的催化剂 可用做该反应过程的催化剂 |
 、
、 、
、 、NO、
、NO、 中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。
中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。A.肯定有 和 和 | B.肯定有NO |
C.肯定没有 和 和 | D.可能有 和 和 |
 ,该反应中氧化剂是
,该反应中氧化剂是(5)汽车剧烈碰撞时,安全气囊中发生反应:
 。该反应中氧化产物与还原产物的质量比为
。该反应中氧化产物与还原产物的质量比为 在标准状况下的体积为
在标准状况下的体积为(6)高铁酸钠(
 ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】请回答下列问题
(1)浓硫酸与木炭在加热条件下的化学方程式为___________ 。
(2)试用上述各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号)___________ →___________ →___________ →___________ 。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是___________ ,C瓶溶液的作用是___________ 。
(4)装置②中所加的固体药品是___________ ,确定装置②在整套装置中位置的理由是___________ 。
(5)装置③中所盛的溶液可验证的产物是___________ 。
| 编号 | ① | ② |
| 装置 | 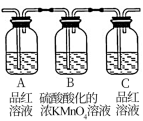 |  |
| 编号 | ③ | ④ |
| 装置 | 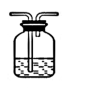 | 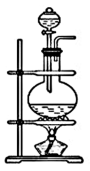 |
(2)试用上述各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号)
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是
(4)装置②中所加的固体药品是
(5)装置③中所盛的溶液可验证的产物是
您最近一年使用:0次
【推荐1】碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如图:

Sr(OH)2在水中的溶解度
(1)元素Sr位于元素周期表第五周期第______ 族。
(2)菱锶矿、焦炭混合粉碎的目的是______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_____ ,进行煅烧反应的立窑衬里应选择_____ (填“石英砂砖”或“碱性耐火砖”)。
(4)“浸取”中用热水浸取而不用冷水的原因是_____ ;滤渣1含有焦炭、Ca(OH)2和______ 。
(5)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO•yFe2O3)中Sr与Fe的质量比为0.13,则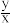 为
为_____ (取整数)。

Sr(OH)2在水中的溶解度
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
(4)“浸取”中用热水浸取而不用冷水的原因是
(5)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO•yFe2O3)中Sr与Fe的质量比为0.13,则
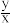 为
为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组同学欲探究 的性质,过程如下:
的性质,过程如下:
①向5%的 溶液中滴加少量酸性KI溶液;
溶液中滴加少量酸性KI溶液;
②向5%的 溶液中滴加少量酸性
溶液中滴加少量酸性 溶液。
溶液。
(1) 中氧元素的化合价为
中氧元素的化合价为__________ 。
(2)实验①选择KI的原因是KI具有__________ (填“氧化性”或“还原性”),在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝。
(3)实验②的目的是验证 有还原性,该实验中,得出结论的依据是:酸性
有还原性,该实验中,得出结论的依据是:酸性 溶液颜色变浅或褪色,
溶液颜色变浅或褪色,___________________ 。
(4)以上实验可得出的结论是_____________________________ 。
 的性质,过程如下:
的性质,过程如下:①向5%的
 溶液中滴加少量酸性KI溶液;
溶液中滴加少量酸性KI溶液;②向5%的
 溶液中滴加少量酸性
溶液中滴加少量酸性 溶液。
溶液。(1)
 中氧元素的化合价为
中氧元素的化合价为(2)实验①选择KI的原因是KI具有
(3)实验②的目的是验证
 有还原性,该实验中,得出结论的依据是:酸性
有还原性,该实验中,得出结论的依据是:酸性 溶液颜色变浅或褪色,
溶液颜色变浅或褪色,(4)以上实验可得出的结论是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
I.指出下列粒子中带下划线元素的化合价:
(1)Na2O2_______ NH3 _______ Ca(ClO)2 _______
II.现有下列8种物质:
①Cl2 ②钠 ③H2O ④CO2 ⑤ H2SO4 ⑥Fe(OH)3胶体 ⑦ C12H22O11(蔗糖) ⑧NaCl溶液
(2)把上述各物质按物质的分类方法填写在表格的空白处(填物质编号):
(3)写出②与③反应的化学方程式_______ ;
(4)写出⑤与Ba(OH)2溶液反应的离子方程式 _______ 。
I.指出下列粒子中带下划线元素的化合价:
(1)Na2O2
II.现有下列8种物质:
①Cl2 ②钠 ③H2O ④CO2 ⑤ H2SO4 ⑥Fe(OH)3胶体 ⑦ C12H22O11(蔗糖) ⑧NaCl溶液
(2)把上述各物质按物质的分类方法填写在表格的空白处(填物质编号):
| 分类标准 | 电解质 | 非电解质 |
| 属于该类的物质 |
(4)写出⑤与Ba(OH)2溶液反应的
您最近一年使用:0次



