硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。请回答下列问题:
(1)Si元素位于元素周期表_______ ,在 中,硅原子和氧原子以
中,硅原子和氧原子以_______ (选填“极性共价键”、“非极性共价键”、“离子键”)连接形成立体网状结构,所以 硬度大。
硬度大。
(2)国家速滑馆用到建筑黏合剂和防火剂硅酸钠,硅酸钠可由 溶解在
溶解在 溶液中反应来制备,反应的离子方程式为
溶液中反应来制备,反应的离子方程式为_______ 。
(3)生产磨砂玻璃时可以用 溶蚀玻璃,是因为
溶蚀玻璃,是因为 溶液可与
溶液可与 反应,其化学反应方程式为
反应,其化学反应方程式为_______ 。
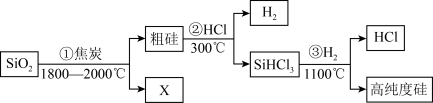
(4)由 制备高纯度硅的工业流程如图所示,
制备高纯度硅的工业流程如图所示, 为
为_______ ,可以循环使用的物质为_______ 。
(1)Si元素位于元素周期表
 中,硅原子和氧原子以
中,硅原子和氧原子以 硬度大。
硬度大。(2)国家速滑馆用到建筑黏合剂和防火剂硅酸钠,硅酸钠可由
 溶解在
溶解在 溶液中反应来制备,反应的离子方程式为
溶液中反应来制备,反应的离子方程式为(3)生产磨砂玻璃时可以用
 溶蚀玻璃,是因为
溶蚀玻璃,是因为 溶液可与
溶液可与 反应,其化学反应方程式为
反应,其化学反应方程式为(4)由
 制备高纯度硅的工业流程如图所示,
制备高纯度硅的工业流程如图所示, 为
为
更新时间:2023/04/23 06:45:02
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是黏土和___ ;
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___ ;乘务员使用的无线通话机的芯片材料是___ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为___ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶,地漏和洗手盆下水口都是纳米硅胶的高科技产品, 向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式为___ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是黏土和
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶,地漏和洗手盆下水口都是纳米硅胶的高科技产品, 向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是_______ (填化学式,下同),光导纤维的主要成分是_______ 。
(2)形成酸雨的原理之一如下图所示:
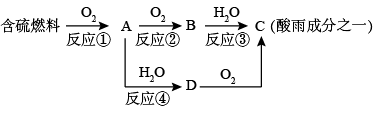
回答下列问题:
①酸雨的pH_______ (填“>”“<”或“=”)5.6。
②氨的催化氧化方程式_______ 。
③铵盐与强碱反应的离子方程式_______
(3)二氧化氮溶于水的化学方程式_______ ,
(4)试管①中反应的化学方程式是_______ 。
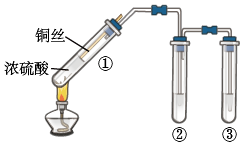
(5)浓硝酸与铜反应的化学方程式为_______ 。
(1)可用于制作计算机芯片和太阳能电池的是
(2)形成酸雨的原理之一如下图所示:

回答下列问题:
①酸雨的pH
②氨的催化氧化方程式
③铵盐与强碱反应的离子方程式
(3)二氧化氮溶于水的化学方程式
(4)试管①中反应的化学方程式是

(5)浓硝酸与铜反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)写出纯碱的化学式:____ 。
(2)写出一氯甲烷的结构式:_____ 。
(3)面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸,请用化学知识解释其现象___ 。
(4)写出工业制粗硅的化学方程式:___ 。
(2)写出一氯甲烷的结构式:
(3)面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸,请用化学知识解释其现象
(4)写出工业制粗硅的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硅单质及其化合物应用范围很广,请回答下列问题:
制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
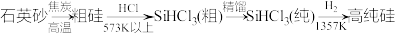
(1)写出由纯SiHCl3制备高纯硅的化学反应方程式___________ ;
(2)整个制备过程必须严格控制无水无氧,SiHCl3遇水剧烈反应生成H2SiO3,HCl和另一种物质,写出配平的化学反应方程式___________ ; H2还原SiHCl3过程中若混入O2,可能引起的后果是___________ 。
制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
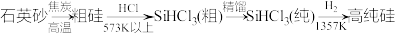
(1)写出由纯SiHCl3制备高纯硅的化学反应方程式
(2)整个制备过程必须严格控制无水无氧,SiHCl3遇水剧烈反应生成H2SiO3,HCl和另一种物质,写出配平的化学反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括________ 、水泥和玻璃。
(2) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是________ (用化学方程式表示)。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是________(填字母)。
(4)硅单质可作为硅半导体材料。三氯甲硅烷( )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:________ 。
②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式________ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是________ 。
(5)新型陶瓷材料氮化硅( )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下: 。若生成标准状况下33.6LCO时,反应过程中转移的电子数为
。若生成标准状况下33.6LCO时,反应过程中转移的电子数为________  。
。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是________(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
(4)硅单质可作为硅半导体材料。三氯甲硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图: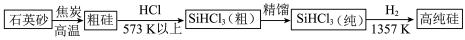
②整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是(5)新型陶瓷材料氮化硅(
 )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下: 。若生成标准状况下33.6LCO时,反应过程中转移的电子数为
。若生成标准状况下33.6LCO时,反应过程中转移的电子数为 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)①写出石英主要成分的化学式:___________ ;②写出正丁烷的结构简式:___________ 。
(2)写出碳与浓硫酸加热条件下反应的化学方程式:___________ 。
(2)写出碳与浓硫酸加热条件下反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学用语是学习化学的基本工具,请用化学用语填空:
(1)相对分子质量最小的氧化物的化学式是_______ 。
(2)地壳中含量居前两位的元素所形成化合物的化学式为_______ 。
(3)氯化钠是由_______ 和_______ 构成;
(4)标出氧化钙中钙元素的化合价_______ 。
(5)写出硝酸钾的化学式_______ 。
(1)相对分子质量最小的氧化物的化学式是
(2)地壳中含量居前两位的元素所形成化合物的化学式为
(3)氯化钠是由
(4)标出氧化钙中钙元素的化合价
(5)写出硝酸钾的化学式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)SiO2在自然界中广泛存在,它是制备现代通讯材料_______ (写该材料名称)的主要原料;以SiO2为原料,在工业上制备粗硅的化学方程式为_______ 。
(2)在一定体积的18 mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积_______ (填“大于”“小于”或“等于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_______ 。
(3)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是_______ (用化学方程式表示)。储运浓硝酸时通常用铁罐或铝罐,则原因是_______ 。硝酸是一种易挥发性的酸,用蘸浓硝酸和蘸浓氨水的玻璃棒靠近会产生大量白烟,白烟的成分是_______ 。
(1)SiO2在自然界中广泛存在,它是制备现代通讯材料
(2)在一定体积的18 mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积
(3)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是___________(填字母)。
(2)SiO2与氢氧化钠溶液反应的化学方程式为___________ 。
(3)氮化硅是一种性能优良的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,根据以上描述,推测氮化硅可能有哪些用途:___________ (填字母)。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作电线
(4)工业上常利用反应2C+SiO2 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___________ (填化学式,下同),氧化剂是___________ 。
(1)下列物质不属于硅酸盐的是___________(填字母)。
| A.陶瓷 | B.玻璃 | C.水晶 | D.生石灰 |
(3)氮化硅是一种性能优良的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,根据以上描述,推测氮化硅可能有哪些用途:
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作电线
(4)工业上常利用反应2C+SiO2
 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:非金属元素在生产生活中扮演着重要角色。石英、焦炭在高温的氮气流中发生反应: 。
。
(1)该反应的还原剂是_______ ,反应所涉及的元素中,非金属性最强的是_______ ;硅元素在元素周期表中的位置_________________ ,N2的电子式是________________ 。
(2)氮化硅(Si3N4)是一种性能优异的无机非金属材料,Si3N4中氮元素的化合价为_____ ;SiO2是一种酸性氧化物,与NaOH溶液反应的离子方程式为_____________ 。
 。
。(1)该反应的还原剂是
(2)氮化硅(Si3N4)是一种性能优异的无机非金属材料,Si3N4中氮元素的化合价为
您最近一年使用:0次

 溶液(试管口用浸有NaOH溶液的棉团塞住),可观察到的现象是
溶液(试管口用浸有NaOH溶液的棉团塞住),可观察到的现象是 溶于水发生反应的离子方程式是
溶于水发生反应的离子方程式是

