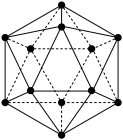
硼普遍存在于蔬菜水果中,是维持骨骼健康和钙、磷、镁正常代谢所需要的微量元素之一。晶体硼的基本结构单元是由硼原子组成的正二十面体(如图),其中含有20个等边三角形和一定数目的顶角,每个顶角上各有1个硼原子。请观察图形后回答:这个基本结构单元由______ 个硼原子组成,键角是______ ,共含有______ 个B-B键。

2023高三·全国·专题练习 查看更多[1]
(已下线)04 常考题空4 晶体化学式及粒子数确定 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-04-25 15:07:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.硒—钴—镧La 三元整流剂在导电玻璃中应用广泛,且三种元素形成的单质及其化合物均有重要的应用。请回答下列问题:
(1)钴位于元素周期表中_____ (填“s”、“p”、“d”或“ds”)区,与钴位于同一周期且含有相同未成对电子数的元素有_____ 种。
(2)元素Se 、O、N 的第一电离能由大到小的顺序_____ 。
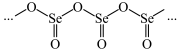
硒的某种氧化物为链状聚合结构如图所示,该氧化物的化学式为_____ 。
(3)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用图表示。
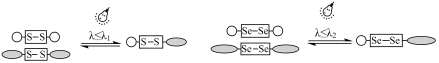
已知光的波长与键能成反比,则图中实现光响应的波长: λ1_________ λ 2 (填“>”、“<”或“=”),其原因是_____ 。
Ⅱ.
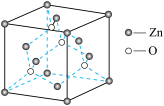
(4)ZnO 的晶胞结构如下图,则 Zn2+的配位数为_____ ;已知晶胞参数为 a cm,该晶体的密度为_____ g cm-3(写出计算式,阿伏加德罗常数的值为 NA)。
(1)钴位于元素周期表中
(2)元素Se 、O、N 的第一电离能由大到小的顺序
硒的某种氧化物为链状聚合结构如图所示,该氧化物的化学式为

(3)二硒键和二硫键是重要的光响应动态共价键,其光响应原理可用图表示。

已知光的波长与键能成反比,则图中实现光响应的波长: λ1
Ⅱ.
(4)ZnO 的晶胞结构如下图,则 Zn2+的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
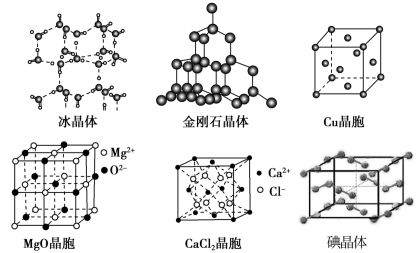
【推荐2】如图为几种晶体或晶胞的结构示意图。
(1)金刚石属于___________ 晶体,其中每个碳原子与___________ 个碳原子距离最近且相等;碘晶体属于___________ 晶体,每个碘晶胞中实际占有___________ 个碘分子,碘晶体熔化过程中克服的作用力为___________ 。
(2)这些晶体中,微粒之间以共价键结合而形成的是___________ 。
(3)冰、金刚石、MgO、碘单质四种晶体的熔点由高到低的顺序为________________________ 。
(4)NaCl晶胞与MgO晶胞结构相同,NaCl晶体的熔点___________ (填“大于”或“小于”)MgO晶体的熔点,原因是____________________________________________ 。
(5)假设碘晶胞中立方体的边长为acm,阿伏加德罗常数的值为 ,则碘晶体的密度为
,则碘晶体的密度为___________  。
。
(1)金刚石属于
(2)这些晶体中,微粒之间以共价键结合而形成的是
(3)冰、金刚石、MgO、碘单质四种晶体的熔点由高到低的顺序为
(4)NaCl晶胞与MgO晶胞结构相同,NaCl晶体的熔点
(5)假设碘晶胞中立方体的边长为acm,阿伏加德罗常数的值为
 ,则碘晶体的密度为
,则碘晶体的密度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的价层电子轨道表示式为___________ 。
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下: ,加入
,加入 的目的是
的目的是___________ 。
(3) 的电子式为
的电子式为___________ 。在25℃和101kPa时,Na与 反应生成1mol
反应生成1mol 放热510.9kJ,写出该反应的热化学方程式:
放热510.9kJ,写出该反应的热化学方程式:___________ 。 可作供氧剂,写出
可作供氧剂,写出 与CO2反应的化学方程式
与CO2反应的化学方程式___________ 。若有1mol 参加反应则转移电子的物质的量为
参加反应则转移电子的物质的量为___________ mol。
(4)采用空气和Na为原料可直接制备 。空气与熔融金属Na反应前需依次通过
。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(5)向酸性KMnO4溶液中加入 粉末,观察到溶液褪色,发生如下反应: ______MnO
粉末,观察到溶液褪色,发生如下反应: ______MnO +_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:
+_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:___________ ,该反应说明 具有
具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为___________ 。

(7)天然碱的主要成分为 ,1mol
,1mol 经充分加热得到
经充分加热得到 的质量为
的质量为___________ g。
(1)基态Na原子的价层电子轨道表示式为
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下:
 ,加入
,加入 的目的是
的目的是(3)
 的电子式为
的电子式为 反应生成1mol
反应生成1mol 放热510.9kJ,写出该反应的热化学方程式:
放热510.9kJ,写出该反应的热化学方程式: 可作供氧剂,写出
可作供氧剂,写出 与CO2反应的化学方程式
与CO2反应的化学方程式 参加反应则转移电子的物质的量为
参加反应则转移电子的物质的量为(4)采用空气和Na为原料可直接制备
 。空气与熔融金属Na反应前需依次通过
。空气与熔融金属Na反应前需依次通过a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(5)向酸性KMnO4溶液中加入
 粉末,观察到溶液褪色,发生如下反应: ______MnO
粉末,观察到溶液褪色,发生如下反应: ______MnO +_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:
+_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式: 具有
具有(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为

(7)天然碱的主要成分为
 ,1mol
,1mol 经充分加热得到
经充分加热得到 的质量为
的质量为
您最近一年使用:0次



