如图所示,天然气(主要成分CH4)烧水是一种生活中常见现象。

(1)天然气燃烧过程中放出热量,请从化学键角度解释原因:___________ 。
(2)水从液态变成气态过程中___________ (填“吸收”或“放出”)热量。
(3)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
当H2(g)和O2(g)化合生成 2 mol H2O (g) 时,放出___________ kJ的能量。
(4)用微观示意图表示①、②过程中水发生的变化。示例:水分子表示为 。
。
①水从液态变为气态的微观过程示意图__________
②水分解的微观过程示意图__________

(1)天然气燃烧过程中放出热量,请从化学键角度解释原因:
(2)水从液态变成气态过程中
(3)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
| 化学键 | H-H | O=O | H-O |
| 键能/kJ•mol-1 | 436 | 498 | 463 |
(4)用微观示意图表示①、②过程中水发生的变化。示例:水分子表示为
 。
。①水从液态变为气态的微观过程示意图
更新时间:2023-04-28 21:55:01
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空
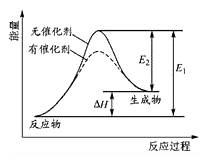
(1)某反应的反应过程中能量变化如图所示,回答下列问题:
E逆反应的活化能___ E反应的活化能(填“大于”或“小于”)
(2)50mL 0.50mol/L盐酸与50mL 0.55mo/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
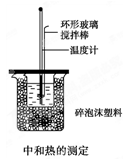
①烧杯间填满碎泡沫塑料作用是________
②实验中改用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量_________ (填“相等“或“不相等”)
(1)某反应的反应过程中能量变化如图所示,回答下列问题:
E逆反应的活化能

(2)50mL 0.50mol/L盐酸与50mL 0.55mo/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:

①烧杯间填满碎泡沫塑料作用是
②实验中改用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】火力发电的原理:首先通过化石燃料___________ ,使___________ ,加热水使之___________ 以推动蒸汽轮机,然后带动发电机发电。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料: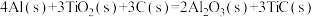
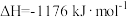 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为___________ 。
(4)肼可作为火箭发动机的燃料,与氧化剂 反应生成N2和水蒸气。
反应生成N2和水蒸气。
已知:①
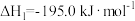
②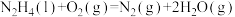
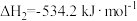
③
 ?
?
根据①与②的数据,计算 =
=___________ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:
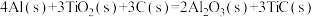
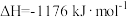 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(4)肼可作为火箭发动机的燃料,与氧化剂
 反应生成N2和水蒸气。
反应生成N2和水蒸气。已知:①

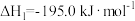
②
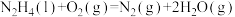
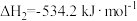
③

 ?
?根据①与②的数据,计算
 =
=
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学反应中常伴随着能量变化。将Mg条打磨后,插入6 mol/L盐酸中。
(1)Mg与盐酸反应的离子方程式是___________ 。
(2)该反应的能量变化可用下图中的___________ 表示(填序号)。
(3)H2的产生速率随时间的变化如图所示。
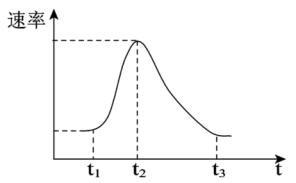
t1~t2速率变化的主要原因是___________ 。
t2~t3速率变化的主要原因是___________ 。
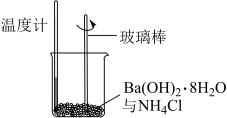
(4)实验表明:如图的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是___________ (填“吸热”或“放热”)反应。
(1)Mg与盐酸反应的离子方程式是
(2)该反应的能量变化可用下图中的
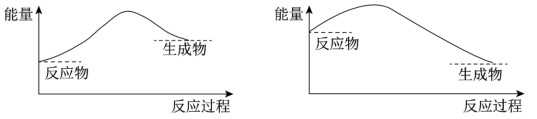
a b
(3)H2的产生速率随时间的变化如图所示。

t1~t2速率变化的主要原因是
t2~t3速率变化的主要原因是
(4)实验表明:如图的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是

您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)已知:2mol 与足量
与足量 充分燃烧生成液态水时放出572kJ热量。
充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的_______ (填字母)表示。

②写出 燃烧生成液态水的热化学反应方程式:
燃烧生成液态水的热化学反应方程式:_______ 。
(4)表中是部分共价键的键能。
根据表中的数据写出工业合成氨的热化学反应方程式:_______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)已知:2mol
 与足量
与足量 充分燃烧生成液态水时放出572kJ热量。
充分燃烧生成液态水时放出572kJ热量。①该反应的能量变化可用图中的

②写出
 燃烧生成液态水的热化学反应方程式:
燃烧生成液态水的热化学反应方程式:(4)表中是部分共价键的键能。
| 共价键 |  |  |  |
键能( ) ) | 436 | 946 | 391 |
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】已知下热化学方程式:
①H2(g)+1/2O2(g)= H2O(l) ⊿H1= —285.8 kJ/mol
②H2(g)+1/2O2(g)= H2O(g) ⊿H2= —241.8kJ/mol
③C(s)+1/2O2(g) = CO(g) ⊿H3= —110.5kJ/mol
④C(s)+ O2(g) = CO2(g) ⊿H4= —393.5kJ/mol
回答下列问题:
(1)比较⊿H1,⊿H2,⊿H3,⊿H4的大小_______________
(2)上述反应中属于放热的是_______
(3)H2的燃烧热为________________ ,C的燃烧热为_______________
(4)燃烧10g H2生成液态水,放出的热量为_________________________
(5)CO的燃烧热为_________ ,其热化学方程式为__________________
(6)分别燃烧1mol C,H2,CO;充分燃烧后它们放出的热量分别为Q1,Q2,Q3
试比较Q1,Q2,Q3的大小___________________________
①H2(g)+1/2O2(g)= H2O(l) ⊿H1= —285.8 kJ/mol
②H2(g)+1/2O2(g)= H2O(g) ⊿H2= —241.8kJ/mol
③C(s)+1/2O2(g) = CO(g) ⊿H3= —110.5kJ/mol
④C(s)+ O2(g) = CO2(g) ⊿H4= —393.5kJ/mol
回答下列问题:
(1)比较⊿H1,⊿H2,⊿H3,⊿H4的大小
(2)上述反应中属于放热的是
(3)H2的燃烧热为
(4)燃烧10g H2生成液态水,放出的热量为
(5)CO的燃烧热为
(6)分别燃烧1mol C,H2,CO;充分燃烧后它们放出的热量分别为Q1,Q2,Q3
试比较Q1,Q2,Q3的大小
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列各题:
(1)已知1.2 g C不完全燃烧生成CO时放出11.05 kJ的热量,要计算该反应的反应热,首先要写出反应的___ ,然后按其中的化学计量数用所给的数据计算出相应的热量,写出反应热的数值、___ 和___ 。
(2)已知C(s)+O2(g)=CO2(g) ΔH=-393.15 kJ·mol-1。求100 g C完全燃烧放出多少热量,可先计算出100 g C的___ 是多少,然后乘碳的燃烧热来求算;也可以直接按热化学方程式来列___ 计算。
(3)已知2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1。求氢气的燃烧热时,要算出___ H2完全燃烧放出的热量,这就是氢气的燃烧热。
(4)已知物质的键能数据,求反应热,要先写出___ ,然后按公式________ 求算。
(5)由已知相关几个反应的热化学方程式,求某个反应的反应热,要应用___ 定律来求。首先确定_________________ ,明确反应热的加减方向,然后对各个热化学方程式进行适当的调整和组合,就能求算出所求反应的反应热。
(1)已知1.2 g C不完全燃烧生成CO时放出11.05 kJ的热量,要计算该反应的反应热,首先要写出反应的
(2)已知C(s)+O2(g)=CO2(g) ΔH=-393.15 kJ·mol-1。求100 g C完全燃烧放出多少热量,可先计算出100 g C的
(3)已知2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1。求氢气的燃烧热时,要算出
(4)已知物质的键能数据,求反应热,要先写出
(5)由已知相关几个反应的热化学方程式,求某个反应的反应热,要应用
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】2009年“六·五”世界环境日,中国主题是“减少污染——行动起来”,这向世界传达了建设环境友好型社会的理念。已知反应:
①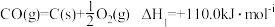
②2CO(g)+O2(g)=2CO2(g) ∆H2=-566.0kJ/mol
请回答下列问题:
(1)反应①的熵变∆S______ (填“>”或“<”)0。
(2)有人建议,汽车尾气中的CO可用催化加热分解的方法来消除(反应①),这一方案在理论上是否可行?______ (填“可行”或“不可行”)。
(3)反应②中的∆H2是不是CO的燃烧热?______ (填“是”或“不是”)。
(4)煤炭的充分燃烧也是建设环境友好型社会的一个重要方面,12 g C(s)完全燃烧生成CO2(g)时,放出的热量为______ kJ(依据反应①、②计算)。
①
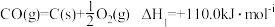
②2CO(g)+O2(g)=2CO2(g) ∆H2=-566.0kJ/mol
请回答下列问题:
(1)反应①的熵变∆S
(2)有人建议,汽车尾气中的CO可用催化加热分解的方法来消除(反应①),这一方案在理论上是否可行?
(3)反应②中的∆H2是不是CO的燃烧热?
(4)煤炭的充分燃烧也是建设环境友好型社会的一个重要方面,12 g C(s)完全燃烧生成CO2(g)时,放出的热量为
您最近半年使用:0次



