回答下列问题:
(1)已知C(s,石墨)=C(s,金刚石),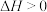 ;则稳定性:金刚石
;则稳定性:金刚石_________ (填“>”或“<”)石墨。
(2)已知: ;
; ,则
,则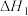
_________ (填“>”或“<”)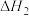 。
。
(3)在25℃、 下,
下, 气态甲醇(
气态甲醇( )完全燃烧放热
)完全燃烧放热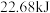 。则表示气态甲醇燃烧热的热化学方程式为
。则表示气态甲醇燃烧热的热化学方程式为__________________ 。
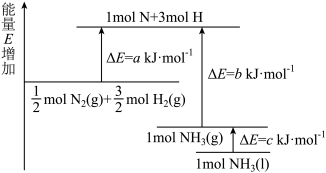
(4)合成氨反应的能量变化如图所示,则反应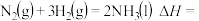
_________ .
(5)几种化学键的键能如下表所示:
①由两种单质化合形成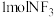 ,焓变
,焓变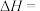
_________  。
。
②工业上由 与
与 制备
制备 :
: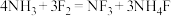 。该反应中氧化剂与还原剂物质的量之比为
。该反应中氧化剂与还原剂物质的量之比为_________ 。
③比较热稳定性:
_________  。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)
(6)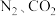 与
与 体系中存在如图1所示物质转变关系,已知
体系中存在如图1所示物质转变关系,已知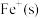 与中间产物
与中间产物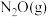 反应过程中的能量变化如图2所示。下列说法正确的是_________。
反应过程中的能量变化如图2所示。下列说法正确的是_________。
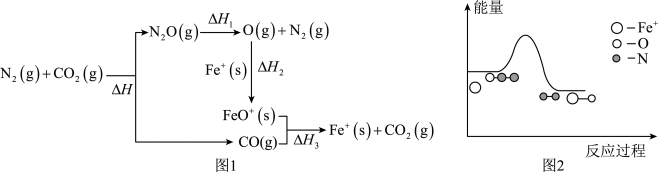
(1)已知C(s,石墨)=C(s,金刚石),
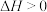 ;则稳定性:金刚石
;则稳定性:金刚石(2)已知:
 ;
; ,则
,则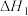
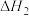 。
。(3)在25℃、
 下,
下, 气态甲醇(
气态甲醇( )完全燃烧放热
)完全燃烧放热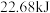 。则表示气态甲醇燃烧热的热化学方程式为
。则表示气态甲醇燃烧热的热化学方程式为(4)合成氨反应的能量变化如图所示,则反应
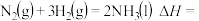

(5)几种化学键的键能如下表所示:
化学键 |
|
|
|
|
键能/ | 941.6 | 154.8 | 283.0 | 200.0 |
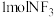 ,焓变
,焓变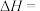
 。
。②工业上由
 与
与 制备
制备 :
: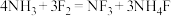 。该反应中氧化剂与还原剂物质的量之比为
。该反应中氧化剂与还原剂物质的量之比为③比较热稳定性:

 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)(6)
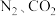 与
与 体系中存在如图1所示物质转变关系,已知
体系中存在如图1所示物质转变关系,已知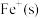 与中间产物
与中间产物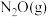 反应过程中的能量变化如图2所示。下列说法正确的是_________。
反应过程中的能量变化如图2所示。下列说法正确的是_________。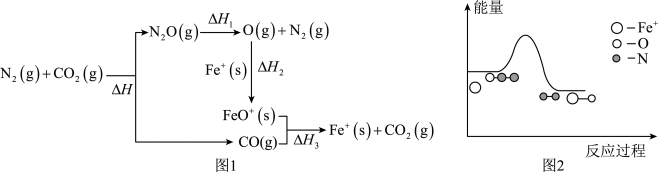
A.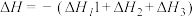 |
B. 在反应中作催化剂,能降低反应的活化能和焓变 在反应中作催化剂,能降低反应的活化能和焓变 |
C.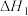 和 和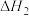 均小于0 均小于0 |
D.由图2可知,反应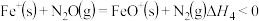 |
更新时间:2023-04-20 06:27:23
|
相似题推荐
【推荐1】回答下列问题:
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g) =CO2(g) △H= - 393.51 kJ/mol
B(s)+O2(g)=CO2(g) △H= - 395.41 kJ/mol
则两种同素异形体中较稳定的是(填"A"或"B")___________________ 。
(2)工业上用H2和Cl2反应制HCl,各键能数据为:H – H:436 kJ/mol;Cl-Cl:243 kJ/mol;H-Cl:431 kJ/mol,该反应的热化学方程式是_____________________ 。
(3)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,已知l gCH4气体与O2气体反应生成CO气体和H2气体放2.25 kJ热量。
①写出相应热化学方程式______________ 。
②用甲烷制备合成气还可以发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2= +216kJ/mol。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。若x=0.2时,反应①放出的能量为____ kJ;若x=____ 时, 反应①与②放出(或吸收)的总能量为0。
(4)一定温度下,将3 mol A气体和l mol B气体通入一容积固定为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为
xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为_________ ; x为___________ 。可以作为达到平衡状态的标志是______________ 。
A.单位时间内生成n mol B的同时生成3n molA
B.混合气体的压强不变
C.混合气体的颜色不再改变(C为有色气体)
D.混合气体的密度不变
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g) =CO2(g) △H= - 393.51 kJ/mol
B(s)+O2(g)=CO2(g) △H= - 395.41 kJ/mol
则两种同素异形体中较稳定的是(填"A"或"B")
(2)工业上用H2和Cl2反应制HCl,各键能数据为:H – H:436 kJ/mol;Cl-Cl:243 kJ/mol;H-Cl:431 kJ/mol,该反应的热化学方程式是
(3)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,已知l gCH4气体与O2气体反应生成CO气体和H2气体放2.25 kJ热量。
①写出相应热化学方程式
②用甲烷制备合成气还可以发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2= +216kJ/mol。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。若x=0.2时,反应①放出的能量为
(4)一定温度下,将3 mol A气体和l mol B气体通入一容积固定为2 L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为
xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为A.单位时间内生成n mol B的同时生成3n molA
B.混合气体的压强不变
C.混合气体的颜色不再改变(C为有色气体)
D.混合气体的密度不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题
(1)用CH4催化还原NOx可以消除氮氧化物的污染,例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1= - 574kJ/mol
CH4(g)+4NO(g)=2N2(g)+ CO2(g)+2H2O(g) △H2
若1molCH4还原NO2制N2,整个过程中放出的热量为867kJ,则△H2=_______
(2)根据盖斯提出的“不管化学过程是一步完成或几步完成这个总过程的热效应是相等的”观点来计算反应热。已知:
C(石墨,s)+O2(g)=CO2(g) △H1= -393.5kJ/mol
C(金刚石,s)+O2(g)=CO2(g) △H2= -395.0kJ/mol
则石墨转化为金刚石的热化学方程式为_______ ;相同状况下,能量状态较低的是_______ ;石墨的稳定性比金刚石_______ (填“高”或“低”)
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1;
CH3OH(g)+H2O(g) △H1;
②CO(g)+2H2(g) CH3OH(g) △H2;
CH3OH(g) △H2;
③CO2(g)+H2(g) CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;
回答下列问题:
已知反应①中的相关的化学键键能(“C O”表示CO的化学键)数据见表:由此计算△H2=
O”表示CO的化学键)数据见表:由此计算△H2=_______ kJ·mol-1,已知△H1=-58kJ·mol-1,则△H3=_______ kJ·mol-1 )
(1)用CH4催化还原NOx可以消除氮氧化物的污染,例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1= - 574kJ/mol
CH4(g)+4NO(g)=2N2(g)+ CO2(g)+2H2O(g) △H2
若1molCH4还原NO2制N2,整个过程中放出的热量为867kJ,则△H2=
(2)根据盖斯提出的“不管化学过程是一步完成或几步完成这个总过程的热效应是相等的”观点来计算反应热。已知:
C(石墨,s)+O2(g)=CO2(g) △H1= -393.5kJ/mol
C(金刚石,s)+O2(g)=CO2(g) △H2= -395.0kJ/mol
则石墨转化为金刚石的热化学方程式为
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1;
CH3OH(g)+H2O(g) △H1; ②CO(g)+2H2(g)
 CH3OH(g) △H2;
CH3OH(g) △H2;③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;回答下列问题:
| 化学键 | H-H | C-O | C O O | H-O | C-H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
已知反应①中的相关的化学键键能(“C
 O”表示CO的化学键)数据见表:由此计算△H2=
O”表示CO的化学键)数据见表:由此计算△H2=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答或解释下列问题:
(1)已知:P4(白磷,s) =4P(红磷,s) ΔH=-a kJ·mol-1(a>0),则稳定性:白磷_______ 红磷(填“大于”或“小于”)。
(2)在常温常压下,1 g 氢气在足量氯气中完全燃烧生成氯化氢气体,放出91.5 kJ 的热量。写出相应的热化学方程式为____________ ;
(3)将浓氨水滴入到固体氢氧化钠中,可以快速制备氨气,用平衡移动原理解释原因:____________ ;
(4)常温下,用0.1mol·L-1 NaOH溶液分别滴定20.00 mL 0.1mol/L HCl溶液和20.00 mL0.1 mol/L CH3COOH溶液,得到2条滴定曲线如图所示:
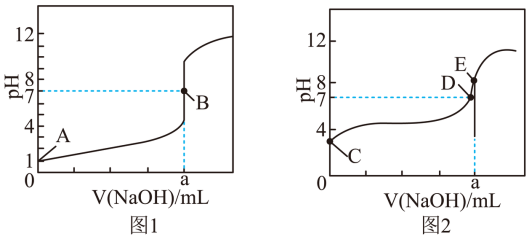
①由A、C点判断,滴定HCl溶液的曲线是__________ (填“图1”或“图2”)。
②a=________ mL。
③D点对应离子浓度由大到小的顺序为____________ 。
(1)已知:P4(白磷,s) =4P(红磷,s) ΔH=-a kJ·mol-1(a>0),则稳定性:白磷
(2)在常温常压下,1 g 氢气在足量氯气中完全燃烧生成氯化氢气体,放出91.5 kJ 的热量。写出相应的热化学方程式为
(3)将浓氨水滴入到固体氢氧化钠中,可以快速制备氨气,用平衡移动原理解释原因:
(4)常温下,用0.1mol·L-1 NaOH溶液分别滴定20.00 mL 0.1mol/L HCl溶液和20.00 mL0.1 mol/L CH3COOH溶液,得到2条滴定曲线如图所示:

①由A、C点判断,滴定HCl溶液的曲线是
②a=
③D点对应离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】环氧乙烷是重要的杀菌剂和工业合成原料。
Ⅰ.乙烯氧化法制环氧乙烷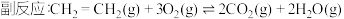

(1)主反应的各基元反应活化能如下:
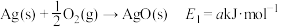 慢
慢
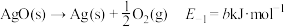 慢
慢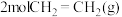 和
和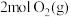 ,达到平衡时
,达到平衡时 的转化率为
的转化率为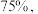
 的选择性为
的选择性为 ,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数
,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数
______ (保留2位有效数字)。已知:环氧乙烷选择性
Ⅱ.电化学合成环氧乙烷
某电化学合成环氧乙烷同时处理酸性含铬废水的原理如图。______ 离子交换膜(填“阴”或“阳”),电极M反应为______ 。
(4)酸性废水质量每增大 ,制得环氧乙烷
,制得环氧乙烷______ g。
Ⅲ.环氧乙烷制乙二醇
水与环氧乙烷分别在酸性和碱性介质中制乙二醇(MEG)的反应机理如下图,同时生成副产物(DEG)。
酸性条件: 的作用是
的作用是______ ,中间体1结构简式______ ,DEG结构简式______ 。
Ⅰ.乙烯氧化法制环氧乙烷


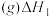
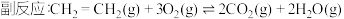

(1)主反应的各基元反应活化能如下:
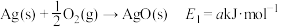 慢
慢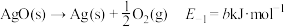 慢
慢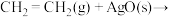

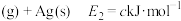 快
快

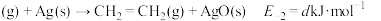 快
快

 (用含a,b,c,d的代数式表示),增大乙烯浓度
(用含a,b,c,d的代数式表示),增大乙烯浓度 的生成速率
的生成速率
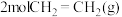 和
和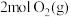 ,达到平衡时
,达到平衡时 的转化率为
的转化率为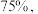
 的选择性为
的选择性为 ,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数
,则平衡时用各组分的物质的量分数表示主反应的化学平衡常数

Ⅱ.电化学合成环氧乙烷
某电化学合成环氧乙烷同时处理酸性含铬废水的原理如图。
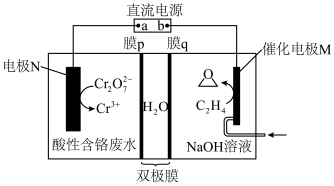
(4)酸性废水质量每增大
 ,制得环氧乙烷
,制得环氧乙烷Ⅲ.环氧乙烷制乙二醇
水与环氧乙烷分别在酸性和碱性介质中制乙二醇(MEG)的反应机理如下图,同时生成副产物(DEG)。
酸性条件:
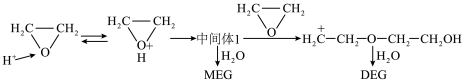

 的作用是
的作用是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】碳族、氮族元素及其化合物在生产、生活和环境保护中应用广泛。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H1=- 890.3 kJ/mol
2H2(g)+O2(g)=2H2O(1) △H2=-571.6 kJ/mol
C(s)+O2(g)=CO2(g) △H3=- 393.5 kJ/mol
C(s)+2H2(g)=CH4(g) △H=_______ kJ/mol。
(2) CH4制备合成气的原理是CH4(g)+CO2(g) 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
①下列叙述不能表示该反应在恒温恒容条件下达到平衡状态的是________ 。
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中CO2、CO的物质的量的比值不再发生变化
d.混合气体的平均相对分子质量不再发生变化
②若1 g CH4(g)完全反应吸收热量为15.5 kJ。在恒容密闭容器中充入1 mol CH4和1 mol CO2在一定条件下反应,体系吸收热量随着时间变化如图所示。在该条件下,甲烷的最大转化率(a)为_________ 。

(3)在密闭容器中只发生反应:2NO+H2=N2+2H2O,其反应速率与浓度关系式为v=kcm(NO)·cn(H2)。(k为常数,只与温度有关,m、n为反应级数,取正整数),在某温度下测得有关数据如表所示。
总反应分两步进行:第i步,2NO+H2=N2+H2O2(很慢);
第ii 步,H2O2+H2=2H2O (很快)。在上述温度下,当c(NO)=c(H2)=0.50 mol/L 时v=____ mol/(L·min )。
(4)在2 L恒容密闭容器中充入3 mol NO(g)和3 mol CO(g),发生反应: 2NO(g)+2CO(g) N2(g)+2CO2(g),在一定温度下达到平衡,测得平衡体系中c(N2)=0.5 mol/L。则该条件下平衡常数K值为
N2(g)+2CO2(g),在一定温度下达到平衡,测得平衡体系中c(N2)=0.5 mol/L。则该条件下平衡常数K值为_______ 。反应前,后容器内气体压强之比为____________ 。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H1=- 890.3 kJ/mol
2H2(g)+O2(g)=2H2O(1) △H2=-571.6 kJ/mol
C(s)+O2(g)=CO2(g) △H3=- 393.5 kJ/mol
C(s)+2H2(g)=CH4(g) △H=
(2) CH4制备合成气的原理是CH4(g)+CO2(g)
 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。①下列叙述不能表示该反应在恒温恒容条件下达到平衡状态的是
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中CO2、CO的物质的量的比值不再发生变化
d.混合气体的平均相对分子质量不再发生变化
②若1 g CH4(g)完全反应吸收热量为15.5 kJ。在恒容密闭容器中充入1 mol CH4和1 mol CO2在一定条件下反应,体系吸收热量随着时间变化如图所示。在该条件下,甲烷的最大转化率(a)为

(3)在密闭容器中只发生反应:2NO+H2=N2+2H2O,其反应速率与浓度关系式为v=kcm(NO)·cn(H2)。(k为常数,只与温度有关,m、n为反应级数,取正整数),在某温度下测得有关数据如表所示。
序数 | c(NO)/(mol/L) | c(H2)/(mol/L) | v/mol/(L·min ) |
I | 0.10 | 0.10 | 0.414 |
Ⅱ | 0.20 | 0.20 | 3.312 |
Ⅲ | 0.10 | 0.20 | 0.828 |
总反应分两步进行:第i步,2NO+H2=N2+H2O2(很慢);
第ii 步,H2O2+H2=2H2O (很快)。在上述温度下,当c(NO)=c(H2)=0.50 mol/L 时v=
(4)在2 L恒容密闭容器中充入3 mol NO(g)和3 mol CO(g),发生反应: 2NO(g)+2CO(g)
 N2(g)+2CO2(g),在一定温度下达到平衡,测得平衡体系中c(N2)=0.5 mol/L。则该条件下平衡常数K值为
N2(g)+2CO2(g),在一定温度下达到平衡,测得平衡体系中c(N2)=0.5 mol/L。则该条件下平衡常数K值为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】CO2的固定、利用有利于缓解温室效应和人类的可持续发展。
(1)我国科研人员发现,320℃左右时,在新型纳米催化剂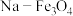 和
和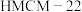 的表面可以将CO2和H2转化为烷烃X,其过程如图所示。
的表面可以将CO2和H2转化为烷烃X,其过程如图所示。
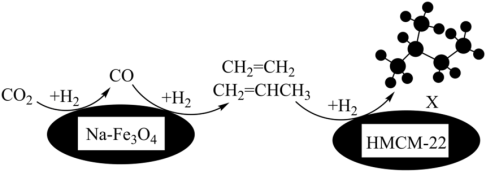
①用系统命名法命名X:_______ 。
②已知: △H = 41 kJ/mol
△H = 41 kJ/mol
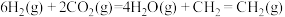 △H = -128 kJ/mol
△H = -128 kJ/mol
写出 气体转化为乙烯的热化学方程式:
气体转化为乙烯的热化学方程式:_______ 。
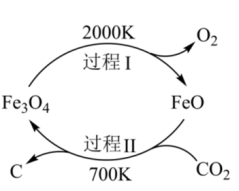
(2)利用太阳能光解Fe3O4,制备的FeO用于还原CO2合成炭黑,可实现资源的再利用。其转化关系如图所示。过程Ⅱ反应的化学方程式是_______
(3)在酸性电解质溶液中,以太阳能电池作电源,惰性材料作电极,可将CO2转化为乙烯。实验装置如图所示。

①若电解过程中生成3.36 L (标准状况下) O2,则电路中转移的电子至少_______ mol。
②生成乙烯的电极反应式是_______ 。
(1)我国科研人员发现,320℃左右时,在新型纳米催化剂
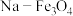 和
和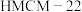 的表面可以将CO2和H2转化为烷烃X,其过程如图所示。
的表面可以将CO2和H2转化为烷烃X,其过程如图所示。
①用系统命名法命名X:
②已知:
 △H = 41 kJ/mol
△H = 41 kJ/mol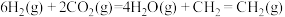 △H = -128 kJ/mol
△H = -128 kJ/mol写出
 气体转化为乙烯的热化学方程式:
气体转化为乙烯的热化学方程式:(2)利用太阳能光解Fe3O4,制备的FeO用于还原CO2合成炭黑,可实现资源的再利用。其转化关系如图所示。过程Ⅱ反应的化学方程式是

(3)在酸性电解质溶液中,以太阳能电池作电源,惰性材料作电极,可将CO2转化为乙烯。实验装置如图所示。

①若电解过程中生成3.36 L (标准状况下) O2,则电路中转移的电子至少
②生成乙烯的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化碳催化加氢制甲醇,不仅有利于减少温室气体二氧化碳,而且还可以获得大量的重要有机化工原料甲醇。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) 平衡常数K该反应一般认为通过如下步骤来实现:
CH3OH(g)+H2O(g) 平衡常数K该反应一般认为通过如下步骤来实现:
i.CO2(g) + H2(g) CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1
CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1
ii.CO(g) + 2H2(g) CH3OH(g) △H =-90 kJ/mol 平衡常数K2
CH3OH(g) △H =-90 kJ/mol 平衡常数K2
则总反应的△H=___________ kJ/mol;平衡常数K=___________ (用K1、K2表示)。
(2)碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。
已知25℃,100kPa时:I.1mol葡萄糖[C6H12O6(s)]完全燃烧生成CO2(g)和H2O(l),放出2804kJ热量。Ⅱ.CO(g)+ O2(g)=CO2(g) ΔH=-283kJ·mol-1。回答问题:
O2(g)=CO2(g) ΔH=-283kJ·mol-1。回答问题:
①25℃时,CO2(g)与H2O(l)经光合作用生成葡萄糖[C6H12O6(s)]和O2(g)的热化学方程式为_______ 。
②25℃,100kPa时,气态分子断开1mol化学键的所需的能量称为键能。已知O=O、C≡O键的键能分别为495kJ·mol-1、799kJ·mol-1,CO2(g)分子中碳氧键的键能为___________ kJ·mol-1。
(3)高炉炼铁的一个反应如下: CO(g)+FeO(s) CO2(g)+Fe(s) △H>0已知1100℃时K=0.263。
CO2(g)+Fe(s) △H>0已知1100℃时K=0.263。
①温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值___________ (填“增大”“减小”或“不变”下同),平衡常数K的变化是___________ 。如果温度不变,在原平衡体系中继续加入一定量CO,达新平衡时,CO的体积分数和原平衡相比___________ 。
②1100℃时,若测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应___________ (填“已经”或“没有”)处于化学平衡状态,此时化学反应速率是v(正)___________ (填“大于”“小于”或“等于”)v(逆)。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) 平衡常数K该反应一般认为通过如下步骤来实现:
CH3OH(g)+H2O(g) 平衡常数K该反应一般认为通过如下步骤来实现:i.CO2(g) + H2(g)
 CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1
CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1ii.CO(g) + 2H2(g)
 CH3OH(g) △H =-90 kJ/mol 平衡常数K2
CH3OH(g) △H =-90 kJ/mol 平衡常数K2则总反应的△H=
(2)碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。
已知25℃,100kPa时:I.1mol葡萄糖[C6H12O6(s)]完全燃烧生成CO2(g)和H2O(l),放出2804kJ热量。Ⅱ.CO(g)+
 O2(g)=CO2(g) ΔH=-283kJ·mol-1。回答问题:
O2(g)=CO2(g) ΔH=-283kJ·mol-1。回答问题:①25℃时,CO2(g)与H2O(l)经光合作用生成葡萄糖[C6H12O6(s)]和O2(g)的热化学方程式为
②25℃,100kPa时,气态分子断开1mol化学键的所需的能量称为键能。已知O=O、C≡O键的键能分别为495kJ·mol-1、799kJ·mol-1,CO2(g)分子中碳氧键的键能为
(3)高炉炼铁的一个反应如下: CO(g)+FeO(s)
 CO2(g)+Fe(s) △H>0已知1100℃时K=0.263。
CO2(g)+Fe(s) △H>0已知1100℃时K=0.263。①温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值
②1100℃时,若测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
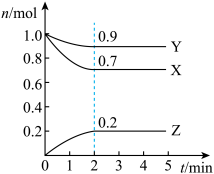
(1)由图中所给数据进行分析,该反应的化学方程式为__________ 。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
0~50s内的平均反应速率 v(N2) = __________ ,250s时,H2的转化率为____________ 。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中___ (填“吸收”或“放出”)的能量为____ , 反应达到(2)中的平衡状态时,对应的能量变化的数值为____ kJ。
(4)反应达平衡时容器内混合气体的平均相对分子质量比起始时____ (填增大、减小或不变),混合气体密度比起始时______ (填增大、减小或不变)。
(5)为加快反应速率,可以采取的措施是_______
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH3

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。
 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中(4)反应达平衡时容器内混合气体的平均相对分子质量比起始时
(5)为加快反应速率,可以采取的措施是
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH3
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】(1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1mol氮气中的化学键需要吸收946kJ能量;破坏0.5mol氢气中的 键需要吸收218kJ能量;形成氨分子中1mol
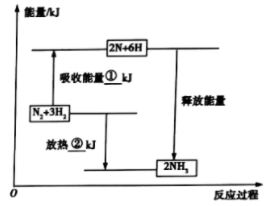
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
①______ kJ,②_____ kJ。
(2)由A、B、C、D四种金属按如表所示装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为_______________ 。
②装置乙中正极的电极反应式为_______________ 。
③装置丙中溶液的pH_________ (填“变大”“变小”或“不变”)
④四种金属的活动性由强到弱的顺序是____________ 。
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: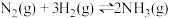 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
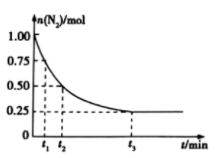
从开始反应到 min,氮气的平均反应速率为
min,氮气的平均反应速率为_________ 。
 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。①

(2)由A、B、C、D四种金属按如表所示装置进行实验。
| 装置 | 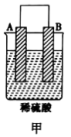 | 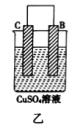 | 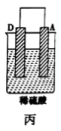 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol
 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: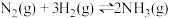 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
 min,氮气的平均反应速率为
min,氮气的平均反应速率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应的热效应是人类获取和利用能量的重要途径。回答下列问题:
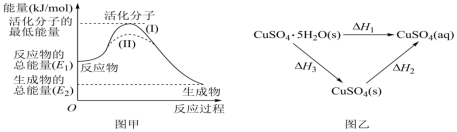
(1)图甲表示某反应的能量变化关系,其ΔH=___________ (用含E1、E2的代数式表示),图乙表示物质的转化路径,则ΔH3=___________ 。(用ΔH1,ΔH2表示)
(2)已知反应:S(g)+O2(g)=SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2,比较ΔH1___________ ΔH2(填“>”“<”或“=”)。
(3)在10℃,101kPa时,0.5mol氢气在氧气中完全燃烧,放出QkJ的热量,则表示该反应的热化学方程式为___________ 。
(4)已知相关共价键的键能数据如下表:。
则C2H6(g) C2H4(g)+H2(g)的ΔH=___________(填字母)。
C2H4(g)+H2(g)的ΔH=___________(填字母)。

(1)图甲表示某反应的能量变化关系,其ΔH=
(2)已知反应:S(g)+O2(g)=SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2,比较ΔH1
(3)在10℃,101kPa时,0.5mol氢气在氧气中完全燃烧,放出QkJ的热量,则表示该反应的热化学方程式为
(4)已知相关共价键的键能数据如下表:。
| 共价键 | H-H | C-H | C-C | C=C |
| 键能/kJ·mol-1 | 436 | 413 | 344 | 614 |
 C2H4(g)+H2(g)的ΔH=___________(填字母)。
C2H4(g)+H2(g)的ΔH=___________(填字母)。| A.+120kJ·mol-1 | B.+46kJ·mol-1 | C.-120kJ·mol-1 | D.-46kJ·mol-1 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.50 mol/L盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL 0.55 mol/L NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)为什么所用NaOH溶液要稍过量_______ 。
(2)倒入NaOH溶液的正确操作是_______ (填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是_______(填序号)。
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol/L的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为_______ 。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生进行实验并通过实验数据计算,该实验测得中和热的数值为57.3 KJ/moL。写出中和热的热化学反应方程式:_______ 。
(6)大烧杯上如不盖硬纸板,求得的中和热ΔH_______ (填‘偏大’‘偏小’‘无影响’)

①用量筒量取50 mL 0.50 mol/L盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL 0.55 mol/L NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)为什么所用NaOH溶液要稍过量
(2)倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是_______(填序号)。
| A.用温度计小心搅拌 |
| B.揭开硬纸片用玻璃棒搅拌 |
| C.轻轻地振荡烧杯 |
| D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动 |
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生进行实验并通过实验数据计算,该实验测得中和热的数值为57.3 KJ/moL。写出中和热的热化学反应方程式:
(6)大烧杯上如不盖硬纸板,求得的中和热ΔH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)═2LiH(s)△H=﹣182kJ•mol﹣1;
②2H2(g)+O2(g)═2H2O(1)△H═﹣572kJ•mol﹣1;
③4Li(s)+O2(g)═2Li2O(s)△H═﹣1196kJ•mol﹣1。
(1)写出LiH在O2中燃烧的热化学方程式__________________ 。
Ⅱ.中和热是指酸跟碱发生中和反应生成1mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
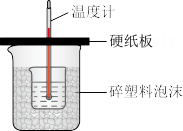
(2)从实验装置上看,图中尚缺少的一种玻璃用品是_____ ,烧杯间填满碎塑料泡沫的作用是_____ 。
(3)大烧杯上如不盖硬纸板,则求得的中和热数值_____ (填“偏大”、“偏小’、“无影响”)。
(4)实验中改用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所求中和热的数值会_____ (填“相等”或“不相等”),理由是_____ 。
(5)设50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H1,25mL 0.5mol/L的浓硫酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H2,50mL 0.5mol/L的醋酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H3,则△H1、△H2、△H3的关系是____ (用“>”“<”或“=”连接)。
①2Li(s)+H2(g)═2LiH(s)△H=﹣182kJ•mol﹣1;
②2H2(g)+O2(g)═2H2O(1)△H═﹣572kJ•mol﹣1;
③4Li(s)+O2(g)═2Li2O(s)△H═﹣1196kJ•mol﹣1。
(1)写出LiH在O2中燃烧的热化学方程式
Ⅱ.中和热是指酸跟碱发生中和反应生成1mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:

(2)从实验装置上看,图中尚缺少的一种玻璃用品是
(3)大烧杯上如不盖硬纸板,则求得的中和热数值
(4)实验中改用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所求中和热的数值会
(5)设50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H1,25mL 0.5mol/L的浓硫酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H2,50mL 0.5mol/L的醋酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H3,则△H1、△H2、△H3的关系是
您最近一年使用:0次






