某小组同学用如下图所示装置进行铜与浓硫酸的反应,并探究产物的性质(气密性已检验、夹持装置已略去)。
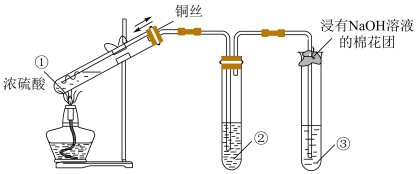
(1)试管①中反应的化学方程式是___________ ;浓硫酸表现出的性质是___________ 、___________ 。
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是___________ ;若试管②中的试剂为酸性 溶液,实验时②中溶液褪色,则说明①中生成的气体具有
溶液,实验时②中溶液褪色,则说明①中生成的气体具有___________ 性;若试管②中的试剂为 溶液,实验中观察到的现象是
溶液,实验中观察到的现象是___________ ,从化合价和物质性质的角度分析该反应发生的原因___________ 。
(3)试管③中的试剂为 溶液,其作用是吸收尾气,反应的离子方程式是
溶液,其作用是吸收尾气,反应的离子方程式是___________ 。
(4)为确认试管①中含铜物质的生成,小组同学需要进行的实验操作 是___________ 。

(1)试管①中反应的化学方程式是
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是
 溶液,实验时②中溶液褪色,则说明①中生成的气体具有
溶液,实验时②中溶液褪色,则说明①中生成的气体具有 溶液,实验中观察到的现象是
溶液,实验中观察到的现象是(3)试管③中的试剂为
 溶液,其作用是吸收尾气,反应的离子方程式是
溶液,其作用是吸收尾气,反应的离子方程式是(4)为确认试管①中含铜物质的生成,小组同学需要进行的实验
更新时间:2023-05-10 09:09:10
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】如下图所示是实验室制取SO2并验证SO2某些性质的装置图。请回答:
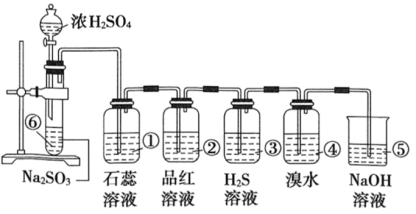
(1)⑥中发生反应的化学方程式为:_______ 。
(2)①中的实验现象为_______ ,此实验证明SO2是_______ 氧化物。
(3)②中的品红溶液_______ ,证明SO2有_______ 性。
(4)③中的实验现象是_______ ,证明SO2有_______ 性。
(5)④中的实验现象是_______ ,证明SO2有_______ 性。
(6)⑤的作用是_______ ,反应的化学方程式为______________ 。

(1)⑥中发生反应的化学方程式为:
(2)①中的实验现象为
(3)②中的品红溶液
(4)③中的实验现象是
(5)④中的实验现象是
(6)⑤的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,X元素的最外层电子数是次外层电子数的三倍。
(1)写出实验室制取W2的离子方程式___________ ;
(2)某小组设计如图所示的实验装置图(图中夹持和加热装置略去),分别研究YX2和W2 的性质。

①分别通入YX2和W2 时,在装置A中观察到的现象是否相同(填“相同”或“不相同”)______ 。装置D中装的是五氧化二钒,当通入YX2时,打开K放入适量的氧气,在D装置中发生化学反应方程式为____ ,
②若装置B中装有5.0 mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程式为___________ 。
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入适量(填字母)___,可以看到白色沉淀产生。
(1)写出实验室制取W2的离子方程式
(2)某小组设计如图所示的实验装置图(图中夹持和加热装置略去),分别研究YX2和W2 的性质。

①分别通入YX2和W2 时,在装置A中观察到的现象是否相同(填“相同”或“不相同”)
②若装置B中装有5.0 mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程式为
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入适量(填字母)___,可以看到白色沉淀产生。
| A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。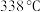 ,酒精灯可加热至
,酒精灯可加热至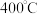 以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的
以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的 。
。
(1)试管①中反应的化学方程式是_______ 。
(2)加热一段时间后,试管①中产生了白雾,⑤⑥⑦中溶液均褪色。
ⅰ.试管⑤⑥⑦中的现象,分别说明 的性质:⑤
的性质:⑤_______ ,⑥_______ ,⑦_______ (填字母,下同)。
a.漂白性 b.氧化性 c.还原性 d.酸性氧化物的通性
ⅱ.下列叙述不正确的是_______ 。
a.上下移动铜丝可控制生成 的量
的量
b.上述实验结束后,发现①中试管内有少量白色固体出现,为确认白色固体为另一反应产物 ,可向试管①中加水,观察颜色
,可向试管①中加水,观察颜色
c.反应结束后,从导管②口向装置中通入空气,可使装置中残留气体完全被吸收,避免污染空气
d.导管②的作用为平衡气压
(3)若实验中换为铜片,取一定质量的铜片和一定体积的 的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释
的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释___ 。

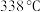 ,酒精灯可加热至
,酒精灯可加热至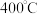 以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的
以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的 。
。(1)试管①中反应的化学方程式是
(2)加热一段时间后,试管①中产生了白雾,⑤⑥⑦中溶液均褪色。
ⅰ.试管⑤⑥⑦中的现象,分别说明
 的性质:⑤
的性质:⑤a.漂白性 b.氧化性 c.还原性 d.酸性氧化物的通性
ⅱ.下列叙述不正确的是
a.上下移动铜丝可控制生成
 的量
的量b.上述实验结束后,发现①中试管内有少量白色固体出现,为确认白色固体为另一反应产物
 ,可向试管①中加水,观察颜色
,可向试管①中加水,观察颜色c.反应结束后,从导管②口向装置中通入空气,可使装置中残留气体完全被吸收,避免污染空气
d.导管②的作用为平衡气压
(3)若实验中换为铜片,取一定质量的铜片和一定体积的
 的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释
的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。

根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
(1)写出SO2与FeCl3溶液反应的离子方程式:_______ ;
(2)C装置中所盛装的FeCl3溶液为5mL,物质的量浓度为1.0mol·L-1,欲使其完全被SO2还原,则至少需要Na2SO3固体_______ g;
(3)该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO 。该做法
。该做法_______ (填“合理”或“不合理”),理由是_______ 。
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有_______(填序号)。
Ⅱ.探究SO2和Na2O2的反应
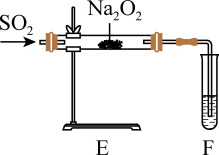
(5)将实验Ⅰ中制备的SO2直接通入E中,将带火星的木条靠近F的试管口,发现木条复燃,据此现象甲同学认为SO2和CO2性质相似,其产物应为Na2SO3和O2,但是乙同学不赞同,他认为木条复燃可能是SO2中含有水蒸气的原因,请用化学方程式来解释乙的观点_______ 。
(6)乙同学认为反应生成的是另外一种盐Na2SO4,因为SO2具有_______ 性。
(7)丙同学认为两种盐都有,取E中完全反应后所得的固体进行如下操作:

根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
(1)写出SO2与FeCl3溶液反应的离子方程式:
(2)C装置中所盛装的FeCl3溶液为5mL,物质的量浓度为1.0mol·L-1,欲使其完全被SO2还原,则至少需要Na2SO3固体
(3)该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO
 。该做法
。该做法(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有_______(填序号)。
| A.酸性KMnO4溶液 | B.浓硫酸 | C.NaCl溶液 | D.碘水 |
Ⅱ.探究SO2和Na2O2的反应

(5)将实验Ⅰ中制备的SO2直接通入E中,将带火星的木条靠近F的试管口,发现木条复燃,据此现象甲同学认为SO2和CO2性质相似,其产物应为Na2SO3和O2,但是乙同学不赞同,他认为木条复燃可能是SO2中含有水蒸气的原因,请用化学方程式来解释乙的观点
(6)乙同学认为反应生成的是另外一种盐Na2SO4,因为SO2具有
(7)丙同学认为两种盐都有,取E中完全反应后所得的固体进行如下操作:
| 操作 | 现象 | 结论 | |
| i | 取agE中固体溶于水,加入足量BaCl2溶液 | 有白色沉淀产生 | |
| ii | 将浊液过滤,然后向沉淀中加入过量 | 丙同学假设成立 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的转化关系如图1所示(反应条件与部分反应的生成物略去)。
(1)D的化学式为_______ ,Y的电子式为_______ 。
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为________ 。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为_______ 。
(4)气体F和气体 在通常条件下同时通入盛有
在通常条件下同时通入盛有 溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?
溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?______ (填“是”或“否”),理由是_______ 。 ②(体积比)
②(体积比) ③
③ 充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为
充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为_______ (用①②③表示)。
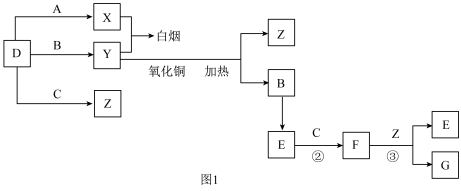
(1)D的化学式为
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)气体F和气体
 在通常条件下同时通入盛有
在通常条件下同时通入盛有 溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?
溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?
 ②(体积比)
②(体积比) ③
③ 充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为
充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室可用如下装置 略去部分夹持仪器
略去部分夹持仪器 制取
制取 并验证其性质.
并验证其性质.
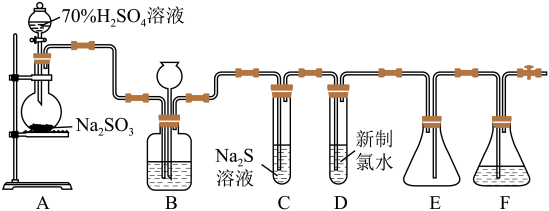
(1)盛装亚硫酸钠的仪器名称为__________ 若将亚硫酸钠改为铜片制取二氧化硫,还缺少的玻璃仪器是________ ,用铜片制取二氧化硫的化学方程式_______ .
(2)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择____  填代号
填代号 .
.
a. 饱和 溶液 b. 饱和
溶液 b. 饱和 溶液
溶液
c. 饱和 溶液 d. 饱和NaHSO3溶液
溶液 d. 饱和NaHSO3溶液
(3)验证二氧化硫的氧化性的装置是______ ,现象为_______________ .
(4)为验证二氧化硫的还原性,充分反应后,取该试管中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀.
溶液,产生白色沉淀.
上述方案合理的是方案________  填“I”、“Ⅱ”或“Ⅲ”
填“I”、“Ⅱ”或“Ⅲ” ;若将试管D中新制氯水改为酸性高锰酸钾溶液,则发生反应的离子方程式为
;若将试管D中新制氯水改为酸性高锰酸钾溶液,则发生反应的离子方程式为____________________ .
(5)装置F的作用是___________________ 
 略去部分夹持仪器
略去部分夹持仪器 制取
制取 并验证其性质.
并验证其性质.
(1)盛装亚硫酸钠的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择 填代号
填代号 .
.a. 饱和
 溶液 b. 饱和
溶液 b. 饱和 溶液
溶液 c. 饱和
 溶液 d. 饱和NaHSO3溶液
溶液 d. 饱和NaHSO3溶液 (3)验证二氧化硫的氧化性的装置是
(4)为验证二氧化硫的还原性,充分反应后,取该试管中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成; 方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀.
溶液,产生白色沉淀.上述方案合理的是方案
 填“I”、“Ⅱ”或“Ⅲ”
填“I”、“Ⅱ”或“Ⅲ” ;若将试管D中新制氯水改为酸性高锰酸钾溶液,则发生反应的离子方程式为
;若将试管D中新制氯水改为酸性高锰酸钾溶液,则发生反应的离子方程式为(5)装置F的作用是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe 及少量Au、Pt 的合金,并设计出由合金制备硫酸铜和硫酸铝晶体的路线:
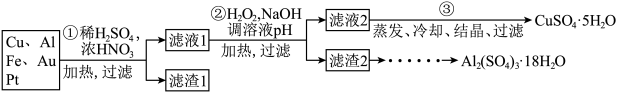
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式___________________ ,得到滤渣1的主要成分为_________ 。
(2)第②步加H2O2的作用是做氧化剂,将溶液中的Fe2+离子氧化为Fe3+,写出该反应的离子方程式_______________________________ ,用H2O2做氧化的优点是__________________ 。
(3)滤渣2的主要成分中Al(OH)3和Fe(OH)3在生产中如何分离两种沉淀,写出反应的离子方程式:_____________________________________________ 。

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式
(2)第②步加H2O2的作用是做氧化剂,将溶液中的Fe2+离子氧化为Fe3+,写出该反应的离子方程式
(3)滤渣2的主要成分中Al(OH)3和Fe(OH)3在生产中如何分离两种沉淀,写出反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行相关实验。
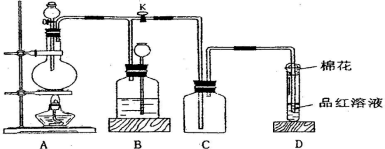
请回答:
⑴ 装置 A 中发生的化学反应方程式为_________ 。
⑵ 装置 D 中试管口放置的棉花中应浸一种液体,这种液体最好是下列哪种_________ , 其作用是_________ 。
a.NaOH 溶液 b.NaCl 溶液 c.H2O d.NH4Cl 溶液
⑶ 装置 B 的作用是贮存多余的气体。当 D 处有明显的现象后,关闭旋塞 K 并移去酒精灯,但由于余热的作用,A 处仍有气体产生,此时 B 中现象是_________ 。B 中应放置的液体是(填字母)_________ 。
a.水 b.酸性 KMnO4 溶液 c.饱和 NaHSO3 溶液 d.浓溴水
⑷ 实验中,取一定质量的铜片和一定体积 18 mol·L—1 的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是______ 。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的物质是_________ (填字母)。
a.BaCl2 溶液 b.锌粉 c.紫色石蕊试液 d.滴有酚酞的 NaOH 溶液

请回答:
⑴ 装置 A 中发生的化学反应方程式为
⑵ 装置 D 中试管口放置的棉花中应浸一种液体,这种液体最好是下列哪种
a.NaOH 溶液 b.NaCl 溶液 c.H2O d.NH4Cl 溶液
⑶ 装置 B 的作用是贮存多余的气体。当 D 处有明显的现象后,关闭旋塞 K 并移去酒精灯,但由于余热的作用,A 处仍有气体产生,此时 B 中现象是
a.水 b.酸性 KMnO4 溶液 c.饱和 NaHSO3 溶液 d.浓溴水
⑷ 实验中,取一定质量的铜片和一定体积 18 mol·L—1 的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的物质是
a.BaCl2 溶液 b.锌粉 c.紫色石蕊试液 d.滴有酚酞的 NaOH 溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是化工行业广泛应用的基础原料,某化学兴趣小组为探究浓硫酸所具有的一些特殊性质,进行如下有关实验。
(1)实验一:浓硫酸与铜反应

①装置A中发生反应的化学方程式为_______________________________________ 。当反应转移0.2mol电子时,被还原的硫酸为_____________ mol。
②装置B的作用是贮存多余的气体。B中应放置的溶液是_____________ 。
A.水 B.酸性 溶液 C.浓溴水 D.饱和
溶液 C.浓溴水 D.饱和 溶液
溶液
(2)实验二:浓硫酸与碳反应,并验证反应生成的气体产物
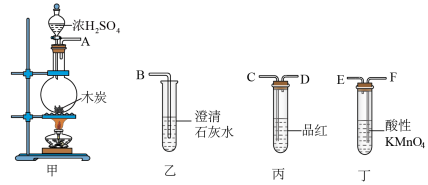
①冯同学认为按照甲、丙、丁、乙的装置顺序,即可验证产物为 和
和 ,那么丁中酸性
,那么丁中酸性 溶液的作用是
溶液的作用是______________________ 。
②陈同学认为丙装置要使用两次才能确保检验气体产物的准确性,如按该同学所说,气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A-_____ -B;能说明气体产物中有 的实验现象是
的实验现象是_______________ 。
(1)实验一:浓硫酸与铜反应

①装置A中发生反应的化学方程式为
②装置B的作用是贮存多余的气体。B中应放置的溶液是
A.水 B.酸性
 溶液 C.浓溴水 D.饱和
溶液 C.浓溴水 D.饱和 溶液
溶液(2)实验二:浓硫酸与碳反应,并验证反应生成的气体产物

①冯同学认为按照甲、丙、丁、乙的装置顺序,即可验证产物为
 和
和 ,那么丁中酸性
,那么丁中酸性 溶液的作用是
溶液的作用是②陈同学认为丙装置要使用两次才能确保检验气体产物的准确性,如按该同学所说,气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A-
 的实验现象是
的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】在古代中国,稀硫酸被称为“绿矾油”。炼丹家孤刚子在其所著《黄帝九鼎神丹经诀》卷九中就记载着“炼石胆取精华法”,即干馏石胆(胆矾)而获得硫酸。
Ⅰ.目前工业上主要采用接触法制备硫酸,其流程如下:

(1)黄铁矿中硫元素的化合价为___________ ,将二氧化硫转化为三氧化硫的化学反应方程式为___________ 。
Ⅱ.硫酸的性质:某化学兴趣小组为了探究足量铁质材料(碳素钢 )和浓硫酸反应的产物,利用下列装置进行了实验探究活动。
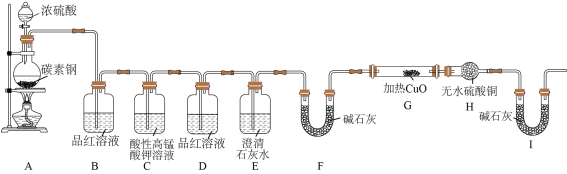
(2)A装置中用于添加浓硫酸的仪器名称为___________ ;请写出碳参与反应的化学方程式___________ 。
(3)实验开始后,观察到装置B和装置C中溶液均褪色。两者褪色原理是否相同?___________ (填“相同”或“不同”)。
(4)若D装置中溶液不褪色,E装置中溶液变浑浊,说明有___________ (填化学式)气体生成。实验过程中观察到___________ 现象时,说明反应产物中还有H2生成。
(5)装置I中碱石灰的作用___________ 。
Ⅰ.目前工业上主要采用接触法制备硫酸,其流程如下:

(1)黄铁矿中硫元素的化合价为
Ⅱ.硫酸的性质:某化学兴趣小组为了探究足量铁质材料(

(2)A装置中用于添加浓硫酸的仪器名称为
(3)实验开始后,观察到装置B和装置C中溶液均褪色。两者褪色原理是否相同?
(4)若D装置中溶液不褪色,E装置中溶液变浑浊,说明有
(5)装置I中碱石灰的作用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组学习了亚铁盐的性质后,欲探究FeSO4溶液分别与Na2CO3溶液、NaHCO3溶液的反应。已知:Fe(OH)2和FeCO3均为白色沉淀,不存在Fe(HCO3)2。实验操作及现象记录如下:
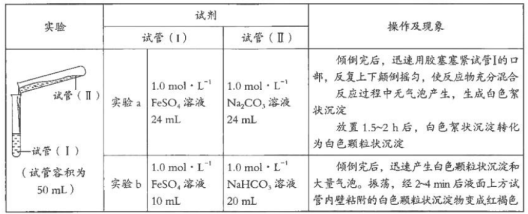
(1)甲同学认为实验a中白色颗粒状沉淀是FeCO3,写出该反应的离子方程式:_________________________ ;他为了证实自己的观点,进行实验:取少量白色颗粒状沉淀,加入__________ ,发现产生大量气泡。
(2)乙同学推测实验a的白色颗粒状沉淀中还可能含有Fe(OH)2,他将实验a中两种溶液体积均改为15mL后再进行实验,证实了他的推测。能证明Fe(OH)2存在的实验现象是___________________________ 。
(3)实验b中白色颗粒状沉淀主要成分也为FeCO3,写出生成FeCO3的离子方程式:_____________________________ 。
(4)实验b中液面上方试管内壁粘附的白色颗粒状沉淀物变为红褐色,主要原因是潮湿的FeCO3被氧气氧化,写出该反应的化学方程式:_________________ 。
(5)乙同学反思,实验a中含有Fe(OH)2,实验b中几乎不含有Fe(OH)2,对比分析出现差异的原因是_____________________________ 。

(1)甲同学认为实验a中白色颗粒状沉淀是FeCO3,写出该反应的离子方程式:
(2)乙同学推测实验a的白色颗粒状沉淀中还可能含有Fe(OH)2,他将实验a中两种溶液体积均改为15mL后再进行实验,证实了他的推测。能证明Fe(OH)2存在的实验现象是
(3)实验b中白色颗粒状沉淀主要成分也为FeCO3,写出生成FeCO3的离子方程式:
(4)实验b中液面上方试管内壁粘附的白色颗粒状沉淀物变为红褐色,主要原因是潮湿的FeCO3被氧气氧化,写出该反应的化学方程式:
(5)乙同学反思,实验a中含有Fe(OH)2,实验b中几乎不含有Fe(OH)2,对比分析出现差异的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是当今世界最重要的化工产品之一。
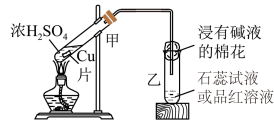
(1)图中甲试管内发生反应的化学方程式___________ ,该反应体现了浓硫酸的性质为___________ 。
(2)图中乙试管中若放紫色石蕊试液遇见SO2的现象___________ ,该变化体现了SO2的性质为___________ 。
(3)图中乙试管中若放品红试液遇见SO2的现象___________ ,该变化体现了SO2的性质为___________ 。
(4)当铜片与浓硫酸充分反应后,试管内并未出现蓝色溶液,而是看到白色固体,请写出检验白色固体的方法___________ 。

(1)图中甲试管内发生反应的化学方程式
(2)图中乙试管中若放紫色石蕊试液遇见SO2的现象
(3)图中乙试管中若放品红试液遇见SO2的现象
(4)当铜片与浓硫酸充分反应后,试管内并未出现蓝色溶液,而是看到白色固体,请写出检验白色固体的方法
您最近一年使用:0次



