下表是元素周期表的一部分。
(1) 和
和 互为
互为___________ ,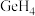 分子的空间结构为
分子的空间结构为___________ 。
(2) 为
为___________ (填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为___________ 。
(3)能作为氯、溴、碘元素非金属性递变规律的判断依据是___________。
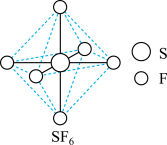
(4) 分子的空间结构为正八面体形,如图所示。
分子的空间结构为正八面体形,如图所示。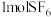 中含有
中含有___________ 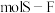 键,它的一氯代物
键,它的一氯代物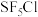 有
有___________ 种。
(5)研究发现,给小鼠喂食适量硒酸钠 可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | H | ||||||
| 二 | C | O | F | ||||
| 三 | Na | Si | S | Cl | |||
| 四 | Ca | Ge | Se | Br |
 和
和 互为
互为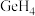 分子的空间结构为
分子的空间结构为(2)
 为
为(3)能作为氯、溴、碘元素非金属性递变规律的判断依据是___________。
A. , , , , 的熔点 的熔点 | B. , , , , 的氧化性 的氧化性 |
C. 、 、 、 、 的热稳定性 的热稳定性 | D. 、 、 、 、 的酸性 的酸性 |
 分子的空间结构为正八面体形,如图所示。
分子的空间结构为正八面体形,如图所示。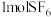 中含有
中含有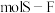 键,它的一氯代物
键,它的一氯代物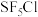 有
有
(5)研究发现,给小鼠喂食适量硒酸钠
 可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
更新时间:2023/04/23 23:43:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题。
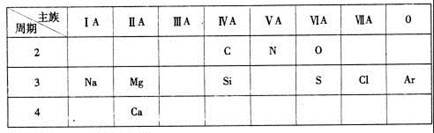
(1)第3周期中金属性最强的元素是_______ (填元素名称);
(2)S原子结构示意图为_______ ;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是_______ (填化学式);
(4)C、N和O原子半径由小到大的顺序的是_______ ;
(5)第3周期中气态氢化物最稳定的是_______ ;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是_______ ,常用于制造_______ (填一种高性能的现代通讯材料的名称);
(7)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为_______
(8)N元素形成的一种氢化物的化学式是_______ ,俗话说“雷雨发庄稼”,请写出二氧化氮溶于水的反应为:_______ 。

(1)第3周期中金属性最强的元素是
(2)S原子结构示意图为
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是
(4)C、N和O原子半径由小到大的顺序的是
(5)第3周期中气态氢化物最稳定的是
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是
(7)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为
(8)N元素形成的一种氢化物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表和元素周期律是学习化学的重要工具,可以帮助我们推测元素及其化合物的结构和性质,对工农业生产具有一定的指导意义。下表是元素周期表的部分片段(2、3周期)
(1)9种元素中,原子半径最小的是______ ,化学性质最不活泼的是____ 。
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是_______ 。
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:______ 和______ 。
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式_______________ 。
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
请你根据上表得出实验结论:_________ ;若比较⑥与⑧的单质的活泼性,请写出实验方案___________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑤ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑥ | ⑧ | ⑨ |
(1)9种元素中,原子半径最小的是
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
| 实验步骤 | 实验现象 |
| A、将一小块单质①放入滴有酚酞溶液的冷水中 | 剧烈反应,①浮于水面上,熔成小球,四处游动,发出“嘶嘶”声.随之消失,溶液变成红色 |
| B、将单质②投入冷水中,观察现象,再将水加热 | 开始无现象,加热后有气体产生 |
| C.将单质②投入稀盐酸中 | 迅速产生大量无色气体 |
| D.将单质③投入稀盐酸中 | 反应不十分剧烈,产生无色气体 |
请你根据上表得出实验结论:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、硫黄等,新品种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂等,用于食品生产中能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为___________ ;普通玻璃的主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化学方程式为___________ 。
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。
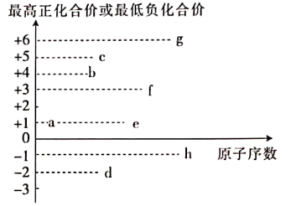
①由a、c、d三种元素形成的离子化合物的化学式为___________ 。
②图中所示元素中金属性最强的是___________ (填元素符号),工业上得到该元素的单质的原理为___________ (填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________ (用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________ (填化学式)。
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为___________ 。
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。

①由a、c、d三种元素形成的离子化合物的化学式为
②图中所示元素中金属性最强的是
③e、f、g元素的简单离子半径由大到小的顺序为
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】半胱氨酸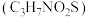 是人体细胞正常活动的必需氨基酸之一。
是人体细胞正常活动的必需氨基酸之一。
(1)组成半胱氨酸的元素中,位于元素周期表第三周期的是_______ 。
(2)非金属性N强于C。
①事实依据: 的酸性比
的酸性比
_______ (填“强”或“弱”)。
②从原子结构角度解释:N和C位于同一周期,原子核外电子层数相同,_______ ,原子半径N小于C,得电子能力N强于C。
(3)半胱氨酸分子中的硫原子被硒(Se)原子取代后称为硒代半胱氨酸,硒代半胱氨酸分子是潜在的抗癌分子药物。Se与O、S在元素周期表中位于同一主族。下列推测正确的是_______ (填字母)。
a.Se的最低化合价为 价
价
b.原子半径:
c.将 通入
通入 溶液中,可生成S
溶液中,可生成S
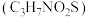 是人体细胞正常活动的必需氨基酸之一。
是人体细胞正常活动的必需氨基酸之一。(1)组成半胱氨酸的元素中,位于元素周期表第三周期的是
(2)非金属性N强于C。
①事实依据:
 的酸性比
的酸性比
②从原子结构角度解释:N和C位于同一周期,原子核外电子层数相同,
(3)半胱氨酸分子中的硫原子被硒(Se)原子取代后称为硒代半胱氨酸,硒代半胱氨酸分子是潜在的抗癌分子药物。Se与O、S在元素周期表中位于同一主族。下列推测正确的是
a.Se的最低化合价为
 价
价b.原子半径:

c.将
 通入
通入 溶液中,可生成S
溶液中,可生成S
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩十种元素,填写下列空白:
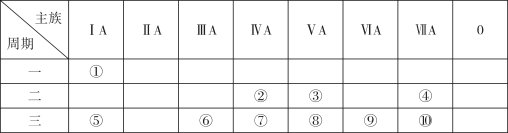
(1)形成化合物种类最多的元素的原子结构示意图为_____________ ,该元素有多种核素,其中一种考古时用于测定文物年代,请写出其原子符号____________ 。
(2)③⑤⑦三种元素的单质中,熔点最高的是____________ (写化学式),元素⑨的气态氢化物的电子式为____________ ,将⑩的单质通入该氢化物的水溶液中,发生反应的离子方程式为____________ 。
(3)这十种元素中,非金属性最强的元素为____________ (写元素符号);⑧⑨⑩三种元素的最高价氧化物对应的水化物中,酸性最弱的是____________ (写化学式)。
(4)⑤⑨⑩三种元素的简单离子半径,由大到小依次为____________ (写离子符号)。
(5)1889年,门捷列夫获得用元素⑥的单质制成的奖杯,以表彰其编制化学元素周期表的贡献。这种单质当时无比珍贵,如今已广泛使用。现在工业上冶炼该单质的化学方程式____________ 。

(1)形成化合物种类最多的元素的原子结构示意图为
(2)③⑤⑦三种元素的单质中,熔点最高的是
(3)这十种元素中,非金属性最强的元素为
(4)⑤⑨⑩三种元素的简单离子半径,由大到小依次为
(5)1889年,门捷列夫获得用元素⑥的单质制成的奖杯,以表彰其编制化学元素周期表的贡献。这种单质当时无比珍贵,如今已广泛使用。现在工业上冶炼该单质的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表的用途广泛。
(1)用“>”或“<”填空:
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液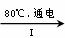 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
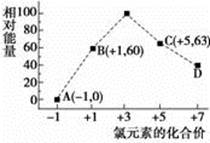
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
(1)用“>”或“<”填空:
| 离子半径 | 非金属性 | 熔点 | 沸点 |
| K+_____S2- | N____O | 金刚石_____晶体硅 | HF____HCl |
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液
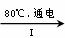 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。

①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了A~R 9种元素在周期表中的位置:(用元素符号回答)
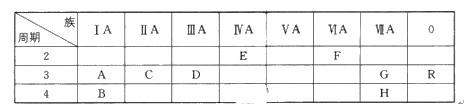
(1)这9种元素其中化学性质最不活泼的是________ ;
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_______________ ;
(3)A、B、C三种元素按原子半径由大到小的顺序排列为________ ;
(4)F元素氢化物的化学式是________ ,

(1)这9种元素其中化学性质最不活泼的是
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
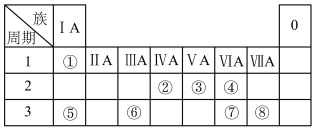
(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素⑦的原子结构示意图为_______ ,元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素④⑤组成原子个数比为1:1的化合物中含_______ (填“离子键”、“共价键”或“离子键和共价键”),将78g该化合物投入98g水中,所得溶液的质量分数为_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式),该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含 和
和 的分子的电子式分别是
的分子的电子式分别是_______ 、_______ 。

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素⑦的原子结构示意图为
(3)由元素④⑤组成原子个数比为1:1的化合物中含
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含
 和
和 的分子的电子式分别是
的分子的电子式分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某同学探究元素性质递变规律,设计了一套方案,进行实验并记录现象。
(1)实验内容:填写与实验步骤标号对应的实验现象的序号并填写相关内容
(2)实验结论:___________ 。
(3)请用原子结构的知识解释上述结论___________ 。
| 实验步骤 | 实验现象(未对应) |
| ①将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加少量酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随后消失,溶液变成红色 B.有气体产生,溶液变成浅红色 C.剧烈反应,迅速产生大量无色气体 D.反应较快,产生无色气体 E.生成白色胶状沉淀,继而沉淀消失 F.生成淡黄色沉淀 |
| ②向新制的Na2S溶液中滴加新制氯水 | |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | |
| ④将镁条放入稀盐酸中 | |
| ⑤将铝条放入稀盐酸中 | |
⑥向 溶液中滴加NaOH溶液至过量 溶液中滴加NaOH溶液至过量 |
| 实验步骤 | 实验现象的字母序号 | 相关内容 |
| ① | 化学方程式 | |
| ② | 离子半径:  (填“>”、“<”或“=”) (填“>”、“<”或“=”) | |
| ③ | 反应产物的电子式: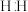 、 、 | |
| ④ | 略 | |
| ⑤ | 略 | |
| ⑥ | 离子方程式 |
(3)请用原子结构的知识解释上述结论
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】H2O2、KCl、Na2SO4、Na2O2、HCl、O2中只含离子键的是___ ,只含极性键的是___ ,只含非极性键的是___ ,既含离子键又含极性键的是___ ,既含离子键又含非极性键的是___ ,既极性键含又含非极性键的是________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4溶于水;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解。用序号填空:
(1)未破坏化学键的是_____________ 。
(2)仅离子键被破坏的是_____________ 。
(3)仅共价键被破坏的是_____________ 。
(4)离子键和共价键均被破坏的是_____________ 。
(5)写出过程③的电离方程式_____________ 。
(1)未破坏化学键的是
(2)仅离子键被破坏的是
(3)仅共价键被破坏的是
(4)离子键和共价键均被破坏的是
(5)写出过程③的电离方程式
您最近一年使用:0次



