按要求完成下列填空:
(1)①写出乙烯的电子式_______ ;
②黄铁矿主要成分的化学式_______ 。
(2)写出Si元素在元素周期表中的位置_______ 。
(3)在加热条件下木炭与浓硫酸反应的化学方程式为_______ 。
(1)①写出乙烯的电子式
②黄铁矿主要成分的化学式
(2)写出Si元素在元素周期表中的位置
(3)在加热条件下木炭与浓硫酸反应的化学方程式为
22-23高一下·浙江·期中 查看更多[1]
(已下线)【2023】【高一下】【期中考】【杭师大附中】【高中化学】【张明涛收集】
更新时间:2023/05/14 21:21:10
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】写出下列反应的离子方程式(不能写离子方程式的写化学方程式):
(1)除去铁粉中少量的二氧化硅杂质:____________________________________________
(2)向H2S溶液中通入SO2气体:____________________________________
(3)KMnO4和浓盐酸制氯气:__________________________________________
(4)除去亚硫酸氢钠溶液中少量的亚硫酸钠杂质:________________________________
(5)用热的氢氧化钠溶液洗涤沾有硫黄的试管:__________________________________________
(1)除去铁粉中少量的二氧化硅杂质:
(2)向H2S溶液中通入SO2气体:
(3)KMnO4和浓盐酸制氯气:
(4)除去亚硫酸氢钠溶液中少量的亚硫酸钠杂质:
(5)用热的氢氧化钠溶液洗涤沾有硫黄的试管:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】雾霾
(1)定义:大量极细微的颗粒物均匀地悬浮在空中,这些颗粒物容易吸附空气中的水蒸气形成____ ,使空气水平能见度小于____ ,我们把这种空气混浊现象叫作雾霾。
(2)粒物分类依据是____ 。
(3)颗粒物分类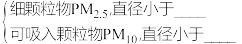
____ ,____ 。
(4)SO2的排放与雾霾形成的关系
空气中的SO2在一定条件下形成____ ,____ 在PM2.5中所占比例较大。
(1)定义:大量极细微的颗粒物均匀地悬浮在空中,这些颗粒物容易吸附空气中的水蒸气形成
(2)粒物分类依据是
(3)颗粒物分类
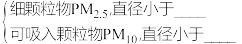
(4)SO2的排放与雾霾形成的关系
空气中的SO2在一定条件下形成
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】“价-类”二维图是学习化学的一种重要工具。如图为硫元素的“价-类”二维图,回答下列问题:

(1)A的化学式为________ 。
(2)SO2与A溶液反应有淡黄色固体生成,该反应的化学方程式为________ ,体现了A的________ (填“氧化性”或“还原性”)。
(3)①将SO2通入品红溶液,观察到的现象为________ ,体现了SO2的_______ 性。
②将SO2通入新制氯水中主要反应的离子方程式为_______ 。
(4)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要作用。现欲在实验室制备大苏打,从氧化还原角度分析,下列合理的是________ (填标号)。

(1)A的化学式为
(2)SO2与A溶液反应有淡黄色固体生成,该反应的化学方程式为
(3)①将SO2通入品红溶液,观察到的现象为
②将SO2通入新制氯水中主要反应的离子方程式为
(4)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要作用。现欲在实验室制备大苏打,从氧化还原角度分析,下列合理的是
| A.Na2S+S | B.Na2SO3+S | C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】实验室利用无水乙醇和浓硫酸制取乙烯,图1为乙烯的制取及乙烯还原性的验证装置图。
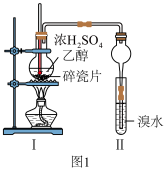
请回答下列问题:
(1)写出该实验中生成乙烯的化学方程式_______ ,反应类型为_______ 反应。该反应加热到140℃时发生的副反应的化学方程式_______ ,反应类型为_______ 反应。
(2)将量好的浓硫酸和乙醇在烧杯中混合时,需要用到的玻璃仪器是_______ 。
(3)碎瓷片的作用是_______ ,若实验中加热一段时间后发现忘记加碎瓷片,则应该采取的措施是_______ 。
A、拔出温度计,从橡胶塞的小孔中加入碎瓷片
B、停止加热,冷却后再加入碎瓷片
C、防止温度下降,迅速打开橡胶塞,加入碎瓷片
(4)甲同学认为:考虑到该混合液体反应的复杂性,酸性高锰酸钾溶液褪色的现象不能证明反应中有乙烯生成,原因是因为实验中,浓硫酸具有_______ 性和_______ 性,故烧瓶内瓶中浓硫酸与乙醇的混合液体变为棕黑色,同时产生的气体中还可能含①_______ 、②_______ (填分子式)。
(5)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加一个洗气瓶,则洗气瓶中的试剂应为_______ 溶液。
(6)为检验可能产生的气体设计如图2所示装置进行检验,将洗气瓶中的溶液转移到图2的锥形瓶中,打开分液漏斗活塞,进行实验。D中的品红溶液不褪色,E中澄清石灰水变浑浊,说明有气体_______ 产生,B中的品红溶液褪色,说明有气体_______ 产生(填分子式)。
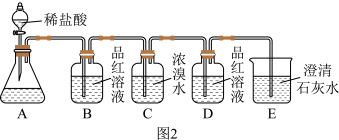

请回答下列问题:
(1)写出该实验中生成乙烯的化学方程式
(2)将量好的浓硫酸和乙醇在烧杯中混合时,需要用到的玻璃仪器是
(3)碎瓷片的作用是
A、拔出温度计,从橡胶塞的小孔中加入碎瓷片
B、停止加热,冷却后再加入碎瓷片
C、防止温度下降,迅速打开橡胶塞,加入碎瓷片
(4)甲同学认为:考虑到该混合液体反应的复杂性,酸性高锰酸钾溶液褪色的现象不能证明反应中有乙烯生成,原因是因为实验中,浓硫酸具有
(5)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加一个洗气瓶,则洗气瓶中的试剂应为
(6)为检验可能产生的气体设计如图2所示装置进行检验,将洗气瓶中的溶液转移到图2的锥形瓶中,打开分液漏斗活塞,进行实验。D中的品红溶液不褪色,E中澄清石灰水变浑浊,说明有气体

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】浓硫酸具有的重要性质有酸性、吸水性,脱水性、强氧化性。请把下列现象中浓硫酸表现出来的性质填写在对应的空白处:
(1)把浓硫酸滴在白纸上,白纸变黑,则浓硫酸表现________ ;
(2)盛有浓硫酸的烧杯敞口放置一段时间,质最增加,则浓硫酸表现出________ ;
(3)浓硫酸与碳共热时,发生反应2H2SO4(浓)+C CO2↑+ 2SO2↑+2H2O,在该反应中,浓硫酸表现出
CO2↑+ 2SO2↑+2H2O,在该反应中,浓硫酸表现出________ 。
(1)把浓硫酸滴在白纸上,白纸变黑,则浓硫酸表现
(2)盛有浓硫酸的烧杯敞口放置一段时间,质最增加,则浓硫酸表现出
(3)浓硫酸与碳共热时,发生反应2H2SO4(浓)+C
 CO2↑+ 2SO2↑+2H2O,在该反应中,浓硫酸表现出
CO2↑+ 2SO2↑+2H2O,在该反应中,浓硫酸表现出
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现据“三大酸”与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,该反应的离子方程式为_ 。
(2)在一定体积的18mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol,则浓硫酸的实际体积__ (填“大于”“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可向其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__ 。
(3)根据如图操作及现象推断酸X为__ (填序号)。
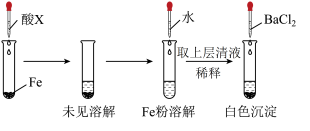
A.浓盐酸 B.浓硫酸 C.浓硝酸
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,该反应的离子方程式为
(2)在一定体积的18mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol,则浓硫酸的实际体积
(3)根据如图操作及现象推断酸X为

A.浓盐酸 B.浓硫酸 C.浓硝酸
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用乙醇制取乙二醇(HOCH2—CH2OH),需要经过3个阶段,依次写出反应的化学方程式,并注明反应类型:
(1)反应方程式________________________________ ,反应类型____________ 。
(2)反应方程式________________________________ ,反应类型_____________ 。
(3)反应方程式________________________________ ,反应类型_____________ 。
(1)反应方程式
(2)反应方程式
(3)反应方程式
您最近一年使用:0次
【推荐3】阅读短文,回答问题。
(1)聚乙烯分子中只含碳碳单键。_______ 。
(2)从元素组成角度分析,聚乙烯和汽油主要成分均属于烃类。_______ 。
(3)我国科学家的研究成果有望降低聚乙烯回收的成本。_______ 。
(4)辛烷值是衡量汽油抗爆性的一项重要指标。_______ 。
聚乙烯塑料制品为我们的生活带来了极大的便利,同时也产生了大量很难自然降解的塑料垃圾,对生态环境与人类健康造成了不利影响。聚乙烯分子中的碳碳单键是非极性键,难以活化或断裂,因此降解和回收利用的难度很大。目前已有的聚乙烯回收方法是热解回收法,通过高温加热(400℃以上)将聚乙烯转化为汽油,该法需要使用贵金属催化剂和额外补充氢气,因此成本较高。
我国科学家利用层状自支撑分子筛作为催化剂,成功实现了在低温(240℃)、无贵金属、无氢气、无溶剂条件下,将聚乙烯塑料转化为高品质汽油,其辛烷值显著高于商用汽油的辛烷值(汽油的辛烷值越高,抗爆性越好),且收率达到80%,该研究成果为废弃聚乙烯催化转化制备高品质汽油提供了新的路线,具有良好的应用前景。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。(1)聚乙烯分子中只含碳碳单键。
(2)从元素组成角度分析,聚乙烯和汽油主要成分均属于烃类。
(3)我国科学家的研究成果有望降低聚乙烯回收的成本。
(4)辛烷值是衡量汽油抗爆性的一项重要指标。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)地壳中含量最多的元素是____ 。
(2)氯元素位于元素周期表第____ 周期VIIA族。
(3)单质的化学性质最不活泼的是____ 。
(4)HF和HCl中,热稳定性较强的是____ 。
(5)元素最高价氧化物对应的水化物中,碱性最强的是____ (填化学式)。
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=____ 。
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)氯元素位于元素周期表第
(3)单质的化学性质最不活泼的是
(4)HF和HCl中,热稳定性较强的是
(5)元素最高价氧化物对应的水化物中,碱性最强的是
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表为元素周期表的短周期部分,请参照元素①~⑧在表中的位置,用化学用语回答下列题:
(1)半径最小的元素是______________ ,金属性最强的元素是____________ ;(填元素符号)
(2)⑤和⑧两元素可形成化合物,灼烧该化合物时火焰颜色为___________ 色;
(3)元素⑧在周期表中的位置是__________________________ ;
(4)①和③两元素形成的化合物的电子式为__________________ ;
(5)①分别与②、③、④形成的化合物中,最稳定是(填写化学式)______________________ ;
(6)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是(填离子符号)__________________ ;
(7)②、③的最高价含氧酸的酸性强弱比较(用化学式表示)_____________________________ 。
① | |||||||
② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)半径最小的元素是
(2)⑤和⑧两元素可形成化合物,灼烧该化合物时火焰颜色为
(3)元素⑧在周期表中的位置是
(4)①和③两元素形成的化合物的电子式为
(5)①分别与②、③、④形成的化合物中,最稳定是(填写化学式)
(6)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是(填离子符号)
(7)②、③的最高价含氧酸的酸性强弱比较(用化学式表示)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】化学元素周期表(Periodictableofelements)是根据元素原子核电荷数从小至大排序的化学元素列表。如表是元素周期表的一部分,根据表中给出的10种元素(其中X、Y、Z分别表示某种化学元素),按要求作答。
(1)Z元素符号是___________ 。
(2)表中元素化学性质最稳定的是___________ (填元素符号)。
(3)地壳中含量最多的元素在元素周期表中的位置是___________ 。
(4)写出Na的原子结构示意图___________ 。
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是___________ 。
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是___________ 。
(7)O2与S单质相比,更难与H2化合的是___________ 。
(8)写出N元素的气态氢化物的化学式___________ ,该物质与水反应的化学方程式:___________ 。
(9)Cl2与水反应的生成物中具有漂白作用的是___________ (填化学式),写出Cl2与NaOH溶液反应的离子方程式:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | X | N | O | F | Y | |||
| 3 | Na | Z | Al | Si | S | Cl |
(2)表中元素化学性质最稳定的是
(3)地壳中含量最多的元素在元素周期表中的位置是
(4)写出Na的原子结构示意图
(5)主要用来制作高纯半导体、耐高温材料、光导纤维通信材料的元素名称是
(6)卤族元素之一,属周期系VIIA族,在元素周期表中位于第二周期的元素是
(7)O2与S单质相比,更难与H2化合的是
(8)写出N元素的气态氢化物的化学式
(9)Cl2与水反应的生成物中具有漂白作用的是
您最近一年使用:0次



