某白色粉末中可能含 、
、 、
、 、
、 和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:
和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:
步骤一:取少量白色粉末溶于水,没有气体逸出,得到无色透明溶液①;
步骤二:向溶液①中滴加稀硫酸,产生浅黄色固体和气体X;
步骤三:将气体X通入 溶液、产生黑色沉淀。
溶液、产生黑色沉淀。
根据上述现象,下列关于该白色粉末的说法中正确的是
 、
、 、
、 、
、 和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:
和NaCl。某化学兴趣小组现取该白色粉末进行如下实验:步骤一:取少量白色粉末溶于水,没有气体逸出,得到无色透明溶液①;
步骤二:向溶液①中滴加稀硫酸,产生浅黄色固体和气体X;
步骤三:将气体X通入
 溶液、产生黑色沉淀。
溶液、产生黑色沉淀。根据上述现象,下列关于该白色粉末的说法中正确的是
A.白色粉末一定不含有 和NaCl 和NaCl |
B.白色粉末中 和 和 的物质的量之比大于2 的物质的量之比大于2 |
| C.黑色沉淀不溶于硝酸 |
| D.向溶液①中加入硝酸银可以检验氯离子是否存在 |
2023·辽宁沈阳·三模 查看更多[2]
更新时间:2023-05-18 20:36:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一种新型短路膜电化学电池消除 装置如图所示。下列说法错误的是
装置如图所示。下列说法错误的是
 装置如图所示。下列说法错误的是
装置如图所示。下列说法错误的是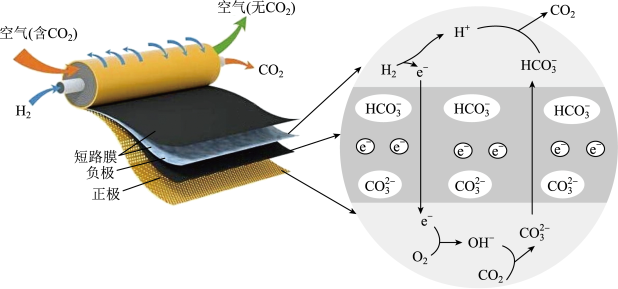
| A.短路膜和常见的离子交换膜不同,它既能传递离子,还可以传递电子 |
B.正极反应消耗标准状况下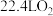 ,理论上需要转移 ,理论上需要转移 电子 电子 |
C.负极反应为: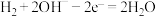 |
D.该装置可用于空气中 的捕获,缓解温室效应 的捕获,缓解温室效应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)可氧化硫酸锰(MnSO4),反应的离子方程式为5NaBiO3+2Mn2++14H+=2MnO- 4+5Bi3++Na++7H2O,下列说法错误的是
| A.若有0.1mol氧化产物生成,则转移0.5mol电子 |
| B.铋酸钠难溶于水 |
| C.该反应可以用于鉴定Mn2+离子 |
| D.该反应可以用浓盐酸酸化 |
您最近一年使用:0次
【推荐1】通过实验得出的结论正确的是
| A.将某固体试样完全溶于盐酸,再滴加BaCl2溶液,出现白色沉淀,则该固体试样中存在SO42- |
| B.将某固体试样完全溶于盐酸,再滴加KSCN溶液,没有出现血红色,则该固体试样中不存在Fe3+ |
| C.在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试样中仍可能存在NH4+ |
| D.在某固体试样加水后的上层清液中,滴加盐酸出现白色沉淀,再加NaOH溶液沉淀溶解,则该固体试样中存在SiO32- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向浓度均为0.1mol•L-1的Na2CO3和Na2S混合溶液中滴入少量AgNO3溶液 | 产生黑色沉淀(Ag2S) | Ksp(Ag2S)>Ksp(Ag2CO3) |
| B | 将少量硼酸溶液滴入碳酸钠溶液中 | 无气泡 | 酸性:H2CO3>H3BO3 |
| C | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2样品中一定含有Fe3+ |
| D | 向某溶液中加入足量氯化钙溶液后,再加入稀盐酸 | 先生成白色沉淀,后沉淀溶解并放出无色无味的气体 | 原溶液中一定含CO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某白色固体混合物由KCl、MgSO4、CaCO3、NaHCO3、NH4Cl中的三种组成,进行如下实验:
①混合物溶于水,得到澄清透明溶液;
②做焰色反应,通过钴玻璃可观察到紫色;
③向溶液中加过量碱,产生白色沉淀并产生气体。根据实验现象可判断其组成为( )
①混合物溶于水,得到澄清透明溶液;
②做焰色反应,通过钴玻璃可观察到紫色;
③向溶液中加过量碱,产生白色沉淀并产生气体。根据实验现象可判断其组成为( )
| A.KCl、CaCO3 、NH4Cl | B.KCl、MgSO4、NH4Cl |
| C.KCl、CaCO3 、NaHCO3 | D.MgSO4、KCl、NaHCO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作和现象,所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用铂丝蘸取无色溶液进行焰色反应 | 火焰呈黄色 | 该溶液定是钠盐溶液 |
| B | 向2mL浓度均为0.lmo/L的NaCl和NaI混合溶液中滴加2 滴0.1mol/L的AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向氯化钡溶液中通入少量SO2,再加入稀硝酸 | 先出现白色沉淀,后白色沉淀不溶解 | 亚硫酸钡和硫酸钡都难溶于水 |
| D | 向20mL0.1mol/L的醋酸溶液中加入10mL0.1mo/L的氢氧化钠溶液,加入再滴加2滴石蕊试液 | 溶液变红 | c(CH3COOH)>c(CH3COO-) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐3】下列关于常见离子的检验方法和结论,其中错误的是
A.先加入稀盐酸酸化,无明显现象,再加入BaCl2溶液有白色沉淀生成,证明原溶液中一定有SO |
| B.向某溶液中先加稀硝酸酸化,然后滴入AgNO3溶液,若有白色沉淀生成,说明溶液中含有Cl− |
C.加入盐酸,产生无色无味的气体,将该气体通入足量澄清石灰水中,溶液变浑浊,原溶液中可能有CO ,也可能有HCO ,也可能有HCO |
| D.对某未知溶液进行焰色试验时,有黄色火焰,透过蓝色钴玻璃显紫色,说明原溶液中一定含有钠盐和钾盐 |
您最近一年使用:0次

 酸性较强,
酸性较强, 常用作食盐中的补碘剂。
常用作食盐中的补碘剂。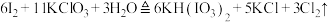 。下列说法错误的是
。下列说法错误的是 时,反应中转移电子数为20a个
时,反应中转移电子数为20a个