铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)可氧化硫酸锰(MnSO4),反应的离子方程式为5NaBiO3+2Mn2++14H+=2MnO- 4+5Bi3++Na++7H2O,下列说法错误的是
| A.若有0.1mol氧化产物生成,则转移0.5mol电子 |
| B.铋酸钠难溶于水 |
| C.该反应可以用于鉴定Mn2+离子 |
| D.该反应可以用浓盐酸酸化 |
更新时间:2016-12-09 04:46:24
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】高铁酸钠(Na2FeO4)是一种绿色净水剂。
①实验室制备原理是 ;
;
②在酸性介质中高铁酸钠不稳定,发生反应: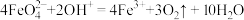 ,在碱性介质中能稳定存在;
,在碱性介质中能稳定存在;
③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性条件下,电势:FeO >Cl2。
>Cl2。
下列叙述错误的是
①实验室制备原理是
 ;
;②在酸性介质中高铁酸钠不稳定,发生反应:
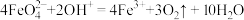 ,在碱性介质中能稳定存在;
,在碱性介质中能稳定存在;③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性条件下,电势:FeO
 >Cl2。
>Cl2。下列叙述错误的是
| A.配制Na2FeO4溶液时添加少量NaOH溶液 |
| B.由反应①知,氧化性:NaClO>Na2FeO4 |
| C.由反应②知,产生11.2LO2时转移2mol电子 |
| D.向Na2FeO4溶液中滴加浓盐酸产生的气体不只一种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验设计能获得成功的是
A.试样 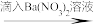 白色沉淀 白色沉淀 沉淀不溶解 沉淀不溶解结论:Na2SO3试样已变质 |
B.粗盐 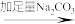 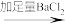    精盐 精盐结论:除去粗盐中含有CaSO4杂质得到精盐 |
C.试样 溶液颜色无变化 溶液颜色无变化 溶液变红色 溶液变红色结论:原溶液中含有Fe2+ |
D.NaI溶液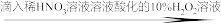  溶液变蓝色 溶液变蓝色结论:酸性条件下,H2O2氧化性强于I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】能正确表示下列变化的离子方程式是
A.NH4Al(SO4)2溶液与过量Ba(OH)2溶液反应: |
B.SO2通入酸性KMnO4溶液中: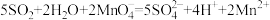 |
C.0.1 mol·L-1 AgNO3溶液中加入过量浓氨水: |
D.酸化NaIO3和NaI的混合溶液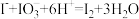 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用某分子筛作催化剂, 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
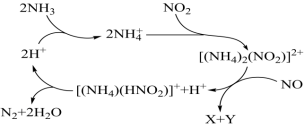
 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
A.X和Y分别为 和 和 中的一种 中的一种 |
B.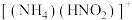 是反应过程中的催化剂 是反应过程中的催化剂 |
C.反应过程中 与 与 之间的反应是氧化还原反应 之间的反应是氧化还原反应 |
D.上述历程的总反应可表示为2NH3+NO+NO2 2N2+3H2O 2N2+3H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下化学反应:①SO2+2Fe3++2H2O=SO +2Fe2++4H+;②Cr2O
+2Fe2++4H+;②Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。则下列有关说法
+6Fe2++14H+=2Cr3++6Fe3++7H2O。则下列有关说法不正确 的是
 +2Fe2++4H+;②Cr2O
+2Fe2++4H+;②Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。则下列有关说法
+6Fe2++14H+=2Cr3++6Fe3++7H2O。则下列有关说法A.氧化性:Cr2O >Fe3+>SO2 >Fe3+>SO2 |
| B.标准状况下,若有6.72 L SO2参加反应,则最终消耗0.2mol K2Cr2O7 |
| C.反应②中,每有1mol K2Cr2O7参加反应,转移电子的数目为6NA |
| D.由上述反应原理推断:K2Cr2O7能将Na2SO3氧化成Na2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法不正确的是
| A.2.24L(标准状况)O2与钠反应时,转移电子数目可能为0.35NA |
| B.常温常压下,17g羟基(-OH)所含的电子数9NA |
| C.6.4gSO2中空气中充分氧化,转移的电子数为0.2NA |
| D.14gC2H4和C3H6的混合物中,所含原子的总数为3NA |
您最近一年使用:0次
【推荐1】下列说法不正确 的是
| A.某溶液中加入AgNO3溶液有白色沉淀生成,不能确定是否有Cl-存在 |
B.向某溶液中加入盐酸,生成能使澄清石灰水变浑浊的无色无味气体,则该溶液可能不含 |
C.向某溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,则该溶液中可能含有 |
| D.用铂丝蘸取某未知溶液于酒精灯火焰上灼烧,显黄色,证明该溶液中不含K+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有一钾盐的溶液中可能含有K2CO3、K2SO4和KCl,只取一次试液,按下列顺序加入试剂溶液能依次检验出这三种盐的是
| A.HCl、AgNO3、BaCl2 | B.AgNO3、HCl、Ba(NO3)2 |
| C.HNO3、BaCl2、AgNO3 | D.HNO3、Ba(NO3)2、AgNO3 |
您最近一年使用:0次

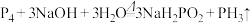 。已知:
。已知: 是一种强还原性的无色剧毒气体,结构与
是一种强还原性的无色剧毒气体,结构与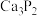 )与水反应制备
)与水反应制备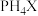 极易水解
极易水解 的水溶液呈碱性,是因为其酸根离子的水解程度大于其电离程度
的水溶液呈碱性,是因为其酸根离子的水解程度大于其电离程度

