对剧毒的氰化物可在碱性条件下用如下方法进行处理:2CN—+8OH—+5Cl2 = 2CO2+N2+10Cl—+4H2O 。下列判断正确的是 ( )
A.当有0.2mol CO2 生成时,溶液中阴离子的物质的量增加 |
B.该反应中,每有2mol CN— 反应,转移电子为  |
C.上述反应中的还原剂是 |
| D.还原性:Cl—> CN— |
14-15高三上·山东泰安·期末 查看更多[2]
更新时间:2016-12-09 05:12:50
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列反应的离子方程式书写正确的是
| A.向AlCl3中滴加氨水直至不再产生白色沉淀:Al3++3OH-=Al(OH)3↓ |
| B.Na2O2溶于水:2Na2O2+2H2O=4Na++4OH-+O2↑ |
C.少量的NaOH与NH4HCO3溶液反应:NH +OH-=NH3↑+H2O +OH-=NH3↑+H2O |
D.少量的SO2通入NaCIO溶液中:SO2+2ClO-+H2O=2HClO+SO |
您最近一年使用:0次
单选题
|
适中
(0.64)
【推荐2】Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32->Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】工业上,从有机催化剂(主要含钴和锌)回收金属的简易流程如下:

下列有关说法错误的是

下列有关说法错误的是
| A.“灼烧”的目的是除去催化剂中的有机物 |
B.“净化”中加入KMnO4,生成Fe(OH)3和MnO2发生的离子方程式为: +3Fe2++7H2O= MnO2+ 3Fe(OH)3+5H+ +3Fe2++7H2O= MnO2+ 3Fe(OH)3+5H+ |
C.“沉钴”中加入(NH4)2S2O8,还原产物为 ,Co2+转化为1molCo(OH)3需消耗1mol(NH4)2S2O8 ,Co2+转化为1molCo(OH)3需消耗1mol(NH4)2S2O8 |
| D.“沉钴”时的pH不能太高的原因是防止生成Zn(OH)2沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】关于化合物HOO-SO3H的性质,下列推测不合理 的是
| A.具有强氧化性 | B.水解可生成H2O2和H2SO4 |
| C.具有强酸性 | D.与足量NaOH溶液反应最终产物为Na2SO4和H2O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】世界卫生组织(WHO)和中国卫健委公认二氧化氯(ClO2)为新时代绿色消毒剂。常温下,ClO2气体与Cl2具有相似的颜色与气味,易溶于水,在水中的溶解度是Cl2的5~8倍。ClO2对热、震动、撞击和摩擦相当敏感,极易分解发生爆炸。ClO2几乎不与冷水反应,遇热水则会分解。经研究表明,ClO2反应释放出的原子氧可以氧化色素,所以ClO2也是优良的漂白剂。工业上可采用SO2与氯酸钠在酸性条件下反应制取ClO2,并生成NaHSO4,相信在不久的将来,ClO2将广泛应用到杀菌消毒领域。实验室可通过下列反应制取ClO2:2KClO3+H2C2O4+H2SO4═2ClO2↑+2CO2↑+K2SO4+2H2O。下列说法不正确的是
| A.ClO2是优良的漂白剂是因为具有强氧化性 |
| B.生成1molClO2有2mol电子发生转移 |
| C.一般可用冰水吸收ClO2气体,形成ClO2溶液 |
| D.工业上制取ClO2过程中,参加反应的氧化剂和还原剂物质的量之比为2:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】实践是检验真理的唯一标准。下列实践项目与所述的化学知识没有关联的是
| 选项 | 实践项目 | 化学知识 |
| A | 利用维生素C和淀粉检验加碘盐中的 | 维生素C将 还原为 还原为 , , 遇淀粉变蓝 遇淀粉变蓝 |
| B | 利用氨气和水做喷泉实验 | 氨气溶于水显碱性 |
| C | 利用 洗涤附着在试管壁上的硫黄 洗涤附着在试管壁上的硫黄 | 硫黄易溶于 |
| D | 给农作物施铵态氮肥时,需将其埋在土中 | 铵盐受热易分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略。下列有关说法不正确的是( )


| A.途径①的反应中体现了浓HNO3的强氧化性 |
| B.途径②、③的第二步反应在实际生产中可以通过增大O2的浓度来低成本 |
| C.由途径①、②、③分别制取1molH2SO4,理论上各消耗1molS,各转移6mole- |
| D.途径②、③比途径①污染相对小且原子利用率高,更能体现“绿色化学”的理论 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】溶液中有如下反应(未配平):FeSO4+NaClO3+H2SO4→Fe2(SO4)3+NaCl+H2O,有关叙述正确的是:
| A.当有1mol电子转移时,消耗硫酸1mol |
| B.消耗3molFe2+,有0.5molClO3—被氧化 |
| C.反应中氧化剂和还原剂物质的量之比为6:1 |
| D.若用浓HNO3代替NaClO3,当生成等量的Fe3+时,n(HNO3)>n(NaClO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】食盐中的碘元素以碘酸钾 形式存在,可根据反应:
形式存在,可根据反应: 验证食盐中存在
验证食盐中存在 ,根据上述反应,下列说法错误的是
,根据上述反应,下列说法错误的是
 形式存在,可根据反应:
形式存在,可根据反应: 验证食盐中存在
验证食盐中存在 ,根据上述反应,下列说法错误的是
,根据上述反应,下列说法错误的是A. 作氧化剂,发生还原反应 作氧化剂,发生还原反应 |
B. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
C.该条件下氧化性: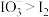 |
D.每生成 转移电子的物质的量为 转移电子的物质的量为 |
您最近一年使用:0次

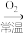 Na2O
Na2O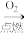 SO3
SO3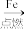 FeCl3
FeCl3
 6FeO+O2↑
6FeO+O2↑


