短周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y核外有13种运动状态不同的电子,基态时Z原子 原子轨道上成对电子与不成对电子数目相等。下列说法正确的是
原子轨道上成对电子与不成对电子数目相等。下列说法正确的是
 原子轨道上成对电子与不成对电子数目相等。下列说法正确的是
原子轨道上成对电子与不成对电子数目相等。下列说法正确的是A.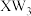 的VSEPR模型为平面三角形 的VSEPR模型为平面三角形 |
B.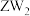 是含有极性键的非极性分子 是含有极性键的非极性分子 |
| C.Z的简单气态氢化物的稳定性比W的弱 |
| D.元素Y、W形成的化合物属于离子晶体 |
更新时间:2023-05-03 17:21:25
|
相似题推荐
单选题
|
适中
(0.65)
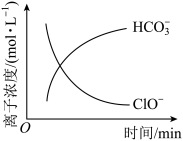
【推荐1】工业废水进行无害化处理过程中主要存在ClO﹣、N2、 、CNO﹣ 、Cl﹣等微粒,对溶液中部分离子浓度进行了跟踪监测,监测结果如图。下列说法正确的是
、CNO﹣ 、Cl﹣等微粒,对溶液中部分离子浓度进行了跟踪监测,监测结果如图。下列说法正确的是
 、CNO﹣ 、Cl﹣等微粒,对溶液中部分离子浓度进行了跟踪监测,监测结果如图。下列说法正确的是
、CNO﹣ 、Cl﹣等微粒,对溶液中部分离子浓度进行了跟踪监测,监测结果如图。下列说法正确的是
A. 中碳原子的杂化方式为sp3 中碳原子的杂化方式为sp3 |
B.处理过程中发生反应:2CNO﹣+3ClO﹣+H2O=2 +N2+3Cl﹣ +N2+3Cl﹣ |
| C.处理过程中每产生22.4L N2转移6 mol e﹣ |
| D.处理过程中加入硫酸使溶液呈强酸性,可达到更好的处理效果 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】三种前四周期主族元素X、Y、Z形成的一种化合物具有高效的储氢性能,其氢含量高达7.84%,释氢时的原理为Z(YX4)2=ZX2+2Y+3X2。下列说法错误的是
| A.化合物Z(YX4)2中的Y不满足8电子稳定结构 |
| B.化合物Z(YX4)2中含有离子键、共价键、配位键 |
| C.同周期中第一电离能小于Y的元素只有1种 |
D.YX 阴离子为正四面体结构 阴离子为正四面体结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】有机化学中的氧化还原反应是一门艺术,如何选择温和的氧化剂,在提高反应效率的同时,不破坏底物分子的结构,是科学家们不断追求的目标。DMP(Dess-Martin periodinane)是现代有机合成中应用最为广泛的、温和型和高选择性氧化剂之一,它的分子结构和氧化机理如图所示,下列有关说法正确的是
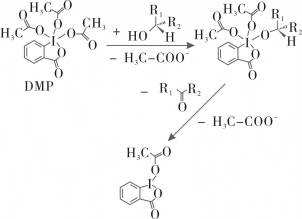

| A.DMP中,I不满足八隅律 |
| B.DMP中,I有一个孤电子对 |
| C.若把该氧化还原反应做成原电池,则活性物质DMP在负极一侧 |
| D.氧化过程中,I的化合价降低1价 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据科学人员探测,在海洋深处的沉积物中含有可燃冰,主要成分是甲烷水合物。有关其组成的两种分子的下列说法正确的是
| A.它们之间以氢键结合在一起 | B.它们的中心原子杂化轨道类型相同 |
| C.它们都是极性键构成的极性分子 | D.它们的空间结构相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化合物M(结构如图所示)可用于制备各种高性能防腐蚀涂料。W、X、Y、Z是原子序数依次增大的短周期主族元素,且占据三个不同周期,W与Z的质子数之和是X的2倍。下列说法不正确的是


| A.X、Y、Z三种元素均在元素周期表的p区 |
| B.W与X形成的分子属于极性分子 |
| C.简单离子半径 Y>X |
| D.基态原子的未成对电子数Z是Y的3倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,其中心原子Cl为sp2杂化已被联合国卫生组织(WTO)列为Al级高效安全消毒剂,其中心原子Cl为sp2杂化。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯酸钠反应,其反应的化学方程式:CH3OH+6NaClO3+3H2SO4=CO2↑+6ClO2↑+3Na2SO4+5H2O,则下列说法错误的是
| A.CO2是非极性分子 | B.键角: < < |
| C.CH3OH在反应中发生氧化反应 | D.ClO2分子空间构型为V形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关物质熔点的比较中,不正确的是
A. | B.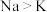 | C. | D.金刚石>晶体硅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在解释下列物质的变化规律与物质结构间的因果关系时,与化学键的强弱无关的是
| A.钠、镁、铝的熔点和沸点逐渐升高,硬度逐渐增大 |
| B.金刚石的硬度大于晶体硅的硬度,其熔点也高于晶体硅的熔点 |
| C.KF、KCl、KBr、KI的熔点依次降低 |
| D.F2、Cl2、Br2、I2的熔点和沸点逐渐升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知非金属元素A、B、C、D是原子序数依次增大的4种短周期元素,其中A是元素周期表中原子半径最小的元素,D是地壳中含量最多的元素,B原子核外电子数是未成对电子数的3倍,E原子核外电子层数为4,其基态原子的内层轨道全部排满电子,且最外层电子数与A相同。下列有关说法正确的是


| A.元素B、C、D的第一电离能由大到小的顺序为:D>C>B |
| B.由A与C以个数比1∶1组成的化合物中不可能含有离子键 |
| C.A与B、A与C、A与D均能形成18电子的分子 |
| D.如图为D和E两种元素组成的化合物的晶胞,则E离子的配位数为4 |
您最近一年使用:0次



