配平下列方程式为___________
Cl2 + KOH — KCl + KClO + H2O
Cl2 + KOH — KCl + KClO + H2O
23-24高一·全国·假期作业 查看更多[1]
(已下线)第04讲 氧化剂和还原剂 氧化还原反应的配平及规律-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
更新时间:2023-06-08 10:21:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】I.氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2.某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
(1)将20mLNO2和NO的混合气体通入倒立于水槽且盛满水的试管中,充分反应后试管中剩余10mL气体,则原混合气体中NO2与NO的体积比为___________。
II.氨气与二氧化氮的反应:将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图所示装置进行实验(加热装置和夹持装置省略)。___________ ,Y管中反应的化学方程式为___________ 。
(3)Z的作用为___________ 。
III.硝酸和硝酸盐是化工中的重要原料
(4)Cu(NO3)2受热易分解,分解反应为2Cu(NO3)2 CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。
CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。
(5)1.52g铜镁合金完全溶解于足量浓硝酸中,得到标况下NO2和N2O4的混合气体1120mL,向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀;则该合金中n(Cu):n(Mg)=______ ;NO2和N2O4的混合气体中,NO2的体积分数为___________ 。
(1)将20mLNO2和NO的混合气体通入倒立于水槽且盛满水的试管中,充分反应后试管中剩余10mL气体,则原混合气体中NO2与NO的体积比为___________。
| A.1∶1 | B.1∶3 | C.3∶1 | D.2∶1 |
II.氨气与二氧化氮的反应:将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图所示装置进行实验(加热装置和夹持装置省略)。

(3)Z的作用为
III.硝酸和硝酸盐是化工中的重要原料
(4)Cu(NO3)2受热易分解,分解反应为2Cu(NO3)2
 CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。
CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。| A.产物中有氧气,所以木条复燃 | B.不能确定NO2是否助燃 |
| C.NO2肯定也能助燃 | D.NO2肯定不能助燃 |
(5)1.52g铜镁合金完全溶解于足量浓硝酸中,得到标况下NO2和N2O4的混合气体1120mL,向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀;则该合金中n(Cu):n(Mg)=
您最近一年使用:0次
【推荐2】中国传统文化是人类文明的瑰宝,古代文献中记载了大量古代化学的研究成果。回答下面问题:
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭土,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为______________ 。
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是_________ ,反应转移4mol电子时,被S氧化的C有____________ mol。
(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式_____________________________________________________ 。
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭土,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C
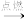 K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上接触法制硫酸过程中,在沸腾炉中煅烧硫铁矿(主要成分为FeS2)的化学方程式为:4 FeS2 + 11O2  2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
请回答下列问题:
(1)已知S为 -1价,则被氧化的元素是 。
(2)若煅烧1.0 t的硫铁矿(杂质含量为30%,杂质中不含硫元素),且FeS2的转化率为90%,则标准状况下,生成的SO2体积为 m3。
(3)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象 。
供选择的试剂:CuSO4溶液、稀硫酸、KMnO4溶液、品红溶液、NaOH 溶液等
(4)炉渣经提纯可制得FeCl3,电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路版。请写出FeCl3溶液与铜反应的化学方程式 。检验反应后的溶液中存在Fe3+的试剂可用 。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,下列试剂中,需要用到的一组是(填字母) 。
①蒸馏水 ②铁粉 ③浓硝酸 ④稀盐酸 ⑤浓氨水 ⑥氯水
 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2请回答下列问题:
(1)已知S为 -1价,则被氧化的元素是 。
(2)若煅烧1.0 t的硫铁矿(杂质含量为30%,杂质中不含硫元素),且FeS2的转化率为90%,则标准状况下,生成的SO2体积为 m3。
(3)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象 。
供选择的试剂:CuSO4溶液、稀硫酸、KMnO4溶液、品红溶液、NaOH 溶液等
(4)炉渣经提纯可制得FeCl3,电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路版。请写出FeCl3溶液与铜反应的化学方程式 。检验反应后的溶液中存在Fe3+的试剂可用 。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,下列试剂中,需要用到的一组是(填字母) 。
①蒸馏水 ②铁粉 ③浓硝酸 ④稀盐酸 ⑤浓氨水 ⑥氯水
| A.①②④⑥ | B.①③④⑥ | C.②④⑤ | D.①④⑥ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式_______ 。开始时_______ 极(阴、阳)碱性增强。
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式_______ 。
(3)氯气压缩成为液氯属于_______ 变化(选填“物理”“化学”)。常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),其中一步反应是:2NH3+3Cl2→N2+6HCl,该反应也表明氯和氮的非金属性_______ > _______ 。写出产生白烟的化学方程式:_______ 。该白烟的成分溶于水,溶液呈_______ 性。(酸、碱或中性),用离子方程式解释原因_______ 。
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
(5)取25 mLpH=2的醋酸溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)_______ c(CH3COO-)。
(1)写出电解饱和食盐水的化学方程式
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式
(3)氯气压缩成为液氯属于
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
| A.都被促进 | B.都被抑制 |
| C.甲中被促进,乙中被抑制 | D.甲中被抑制,乙中被促进 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是___________ (填化学式);用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是___________ (用化学方程式表示)。
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是___________ ;漂白粉也能用于消毒,其有效成分生效的化学方程是___________ 。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
(1)写出生成黄绿色气体的化学方程式:__________________________________________ 。
(2)家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)__________ (填“能”或“不能”)同时使用,其原因是_________________________________ 。
(3)现设计实验由大理石、水、氯气来制取漂白粉:大理石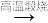


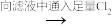 漂白粉溶液
漂白粉溶液  漂白粉
漂白粉
①请写出在制取漂白粉的实验过程中发生的氧化还原反应的化学方程式:___________________________ 。
②当通入氯气较快时,反应产物为 、
、 和
和 ,已知每消耗1
,已知每消耗1
 的同时消耗1
的同时消耗1
 ,请写出此反应的化学方程式:
,请写出此反应的化学方程式:_______________________________________ 。
(1)写出生成黄绿色气体的化学方程式:
(2)家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
(3)现设计实验由大理石、水、氯气来制取漂白粉:大理石


 漂白粉溶液
漂白粉溶液  漂白粉
漂白粉①请写出在制取漂白粉的实验过程中发生的氧化还原反应的化学方程式:
②当通入氯气较快时,反应产物为
 、
、 和
和 ,已知每消耗1
,已知每消耗1
 的同时消耗1
的同时消耗1
 ,请写出此反应的化学方程式:
,请写出此反应的化学方程式:
您最近一年使用:0次



