铁及其化合物在生产、生活中有极其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_______ ,分散剂是_______ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_______ 。
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的化学方程式是_______ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是_______ (填化学专用名词)。
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的化学方程式是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
更新时间:2023-05-12 15:49:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:① ②Cu ③NaCl ④
②Cu ③NaCl ④ 胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸
胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是_______ (填序号,下同),属于电解质的是_______ 。
(2)向④中逐滴滴加⑦,可观察到的现象是_______ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母)。

(4)有同学认为所有酸碱中和反应均可表示为 。请举个例子反驳上述观点(用化学方程式表示)
。请举个例子反驳上述观点(用化学方程式表示)_______ 。
Ⅰ.现有以下物质:①
 ②Cu ③NaCl ④
②Cu ③NaCl ④ 胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸
胶体 ⑤乙醇 ⑥CO2 ⑦稀硫酸(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为
 。请举个例子反驳上述观点(用化学方程式表示)
。请举个例子反驳上述观点(用化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾( 极易溶于水)是优良的多功能水处理剂,其原理如图所示。
极易溶于水)是优良的多功能水处理剂,其原理如图所示。
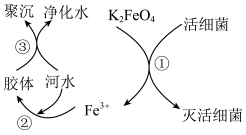
(1) 按物质类别属于
按物质类别属于___________ 。
A.酸 B.盐 C.复盐 D.氧化物
请举例一种和 同一类别的物质
同一类别的物质___________ 。
(2)①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(4)净水利用了 胶体的性质,请写出
胶体的性质,请写出 胶体制备的化学方程式
胶体制备的化学方程式___________ ,提纯所制 胶体常用的方法是
胶体常用的方法是___________ (填实验名称)。
(5)某同学往 胶体中逐滴滴入稀硫酸溶液,出现的现象是
胶体中逐滴滴入稀硫酸溶液,出现的现象是____________ 分析出现该现象的原因是___________ 。
(6) 溶液可以将池塘淤泥里的
溶液可以将池塘淤泥里的 氧化得到无色无味的气体从而起到除臭的作用,0.1mol
氧化得到无色无味的气体从而起到除臭的作用,0.1mol 可以反应标况下的氨气
可以反应标况下的氨气___________ L,为研究这个反应,某同学配制一定物质的量浓度的氨水,将标况下400体积的氨气通入1体积水中,理论上可以得到___________ mol/L密度为0.95g/mL的氨水。
 极易溶于水)是优良的多功能水处理剂,其原理如图所示。
极易溶于水)是优良的多功能水处理剂,其原理如图所示。
(1)
 按物质类别属于
按物质类别属于A.酸 B.盐 C.复盐 D.氧化物
请举例一种和
 同一类别的物质
同一类别的物质(2)①中活细菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)净水利用了
 胶体的性质,请写出
胶体的性质,请写出 胶体制备的化学方程式
胶体制备的化学方程式 胶体常用的方法是
胶体常用的方法是(5)某同学往
 胶体中逐滴滴入稀硫酸溶液,出现的现象是
胶体中逐滴滴入稀硫酸溶液,出现的现象是(6)
 溶液可以将池塘淤泥里的
溶液可以将池塘淤泥里的 氧化得到无色无味的气体从而起到除臭的作用,0.1mol
氧化得到无色无味的气体从而起到除臭的作用,0.1mol 可以反应标况下的氨气
可以反应标况下的氨气
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有如下物质:①铁丝 ②NaOH溶液 ③NaHSO4 固体 ④CO2 ⑤酒精 ⑥蒸馏水 ⑦CCl4 ⑧熔融的KNO3 ⑨红褐色的氢氧化铁胶体
(1)以上物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是_______ 。
(3)分离⑤与⑥的混合液所用的方法是_______ ;分离⑥与⑦的混合液所用的方法是_______ 。
(4)物质③溶于水的电离方程式为_______
(5)向⑨的溶液中逐渐滴加③的溶液,看到的现象是_______
(6)常选择有机溶剂CCl4萃取水溶液中的I2,选择CCl4做萃取剂的原因有:CCl4与水不反应也_______ ;I2在CCl4中溶解_______ (填“大于”或“小于”)I2在水中溶解。
(1)以上物质中,属于电解质的是
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是
(3)分离⑤与⑥的混合液所用的方法是
(4)物质③溶于水的电离方程式为
(5)向⑨的溶液中逐渐滴加③的溶液,看到的现象是
(6)常选择有机溶剂CCl4萃取水溶液中的I2,选择CCl4做萃取剂的原因有:CCl4与水不反应也
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.已知:Fe3+溶液颜色为黄色,Fe2+溶液颜色为浅绿色,Fe(OH)3为红褐色。
(1)现将少量Fe2O3粉末加入适量稀盐酸,发生反应的离子方程式_______ ,用所得溶液进行以下实验:
(2)取少量溶液于试管中,滴入NaOH溶液,观察到有红褐色沉淀生成,反应的离子方程式为_________ 。
(3)取少量溶液于试管中,加入少量还原铁粉,振荡,铁粉逐渐溶解,溶液由黄色变为浅绿色,反应的离子方程式为____________ 。
Ⅱ.现有以下物质:①NaHSO4晶体,②液态O2,③冰醋酸(固态醋酸),④汞,⑤BaSO4固体,⑥Fe(OH)3胶体,⑦酒精(C2H5OH),⑧熔化KNO3,⑨盐酸,⑩金属钠,请回答下列问题(用序号):
(1)以上物质属于电解质的是___________ 。
(2)请写出下列序号物质的电离方程式:
①________________ ;⑧_______________ 。
(3)a.写出制备⑥的实验操作为_________ 。
b.制备⑥的离子方程式为________ 。
(1)现将少量Fe2O3粉末加入适量稀盐酸,发生反应的离子方程式
(2)取少量溶液于试管中,滴入NaOH溶液,观察到有红褐色沉淀生成,反应的离子方程式为
(3)取少量溶液于试管中,加入少量还原铁粉,振荡,铁粉逐渐溶解,溶液由黄色变为浅绿色,反应的离子方程式为
Ⅱ.现有以下物质:①NaHSO4晶体,②液态O2,③冰醋酸(固态醋酸),④汞,⑤BaSO4固体,⑥Fe(OH)3胶体,⑦酒精(C2H5OH),⑧熔化KNO3,⑨盐酸,⑩金属钠,请回答下列问题(用序号):
(1)以上物质属于电解质的是
(2)请写出下列序号物质的电离方程式:
①
(3)a.写出制备⑥的实验操作为
b.制备⑥的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Fe2O3又称铁红,常用作涂料。请按照要求完成下列问题:
(1)向Fe2O3固体中加入适量盐酸制备一种饱和溶液,发生反应的化学方程式为:______ 。
(2)用上述饱和溶液进行下列实验:
①向盛有氢氧化钠溶液的烧杯中滴入过量上述饱和溶液,可观察到的现象______ ,得到的分散系属于______ (“溶液”“浊液”或“胶体”),这个变化可以用化学方程式表示为______ 。
②向小烧杯中加入20毫升蒸馏水,加热至沸腾后,向沸水中滴入几滴上述所得饱和溶液,继续煮沸至溶液呈______ ,停止加热,即可制得______ ,写出其化学方程式:______ 。
③证明有胶体生成的实验原理是_______ ,其现象:______ 。
④向该胶体中逐滴加入稀盐酸,会发生一系列变化:
a.先产生红褐色沉淀,原因是______ 。(文字规范叙述)
b.随后红褐色沉淀溶解,此时发生反应的离子方程式是______ 。
⑤向丙中加入电极通电后,Fe(OH)3胶体粒子移向_______ 极。(填“阴极”或“阳极”)
⑥可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若______ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。这种提纯胶体的方法是:_____ 。

(1)向Fe2O3固体中加入适量盐酸制备一种饱和溶液,发生反应的化学方程式为:
(2)用上述饱和溶液进行下列实验:
①向盛有氢氧化钠溶液的烧杯中滴入过量上述饱和溶液,可观察到的现象
②向小烧杯中加入20毫升蒸馏水,加热至沸腾后,向沸水中滴入几滴上述所得饱和溶液,继续煮沸至溶液呈
③证明有胶体生成的实验原理是
④向该胶体中逐滴加入稀盐酸,会发生一系列变化:
a.先产生红褐色沉淀,原因是
b.随后红褐色沉淀溶解,此时发生反应的离子方程式是
⑤向丙中加入电极通电后,Fe(OH)3胶体粒子移向
⑥可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作或实验所得出的结论一定正确的是______________ (填序号)
A.配制100 mL1.00 mol·L-1的NaCl溶液,可用托盘天平准确称取5.85克NaCl固体
B.某无色溶液中加入盐酸产生无色无味且能使澄清石灰水变浑浊的气体,则该溶液中一定含有大量CO32-
C.制备Fe(OH)3胶体时,应往沸水中加饱和FeCl3溶液,并继续加热到溶液呈红褐色为止
D.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
E.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
F. 容量瓶水洗后未干燥就配制溶液
G. 用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐
H. 量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶中
A.配制100 mL1.00 mol·L-1的NaCl溶液,可用托盘天平准确称取5.85克NaCl固体
B.某无色溶液中加入盐酸产生无色无味且能使澄清石灰水变浑浊的气体,则该溶液中一定含有大量CO32-
C.制备Fe(OH)3胶体时,应往沸水中加饱和FeCl3溶液,并继续加热到溶液呈红褐色为止
D.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
E.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
F. 容量瓶水洗后未干燥就配制溶液
G. 用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐
H. 量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】培养水培植物需要配制营养液。某品牌营养液由NH4Cl、NH4NO3、KNO3、Na3PO4四种固体配制而成。经测定该营养液中部分离子的浓度如图所示。
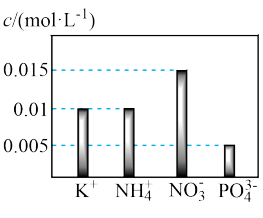
回答下列问题:
(1)固体Na3PO4溶于水的电离方程式为______ ,该营养液中 =
=______  。
。
(2)500mL该营养液中Na3PO4的物质的量为______ mol。
(3)从该营养液中取出500mL,加水稀释为2L。稀释后的溶液中NH4Cl的物质的量浓度为______  。
。
(4)用化学方法检验该营养液中含有 :
:______ (写出简要的操作步骤、试剂、现象和结论)。
(5)现实验室中仅有KCl、NH4NO3、KNO3、Na3PO4四种物质,要配制符合图示所给浓度的营养液,n(KCl)∶n(NH4NO3)∶n(KNO3)∶n(Na3PO4)=______ 。
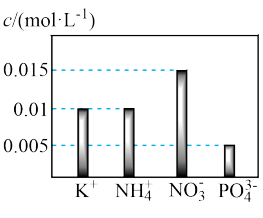
回答下列问题:
(1)固体Na3PO4溶于水的电离方程式为
 =
= 。
。(2)500mL该营养液中Na3PO4的物质的量为
(3)从该营养液中取出500mL,加水稀释为2L。稀释后的溶液中NH4Cl的物质的量浓度为
 。
。(4)用化学方法检验该营养液中含有
 :
:(5)现实验室中仅有KCl、NH4NO3、KNO3、Na3PO4四种物质,要配制符合图示所给浓度的营养液,n(KCl)∶n(NH4NO3)∶n(KNO3)∶n(Na3PO4)=
您最近一年使用:0次
【推荐2】在三支试管中分别加入 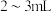
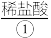 ,
, 溶液、
溶液、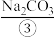 溶液,然后各滴入几滴
溶液,然后各滴入几滴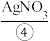 溶液,观察现象;再分别滴入少量
溶液,观察现象;再分别滴入少量 ,观察现象。回答下列问题:
,观察现象。回答下列问题:
(1)AgNO3 在水中电离的电离方程式为_______ 。
(2)①中分散质粒子直径为_______ (填“<1 nm”或“>100 nm”)。
(3)常温下,饱和②溶液_______ (填“能”或“不能”)发生丁达尔效应。
(4)从物质的组成来看,④属于_______ (填“酸”、“碱”、“盐”或“氧化物”),将其加入稀盐酸中,发生反应的化学方程式为_______ 。
(5)查阅资料可知,硝酸具有强氧化性,其浓度越小,氧化能力越弱。对于反应
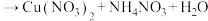 (未配平),该反应的化学方程式为
(未配平),该反应的化学方程式为_______ ,该反应中,每生成0.8gNH4NO3,转移的电子数为_______ NA。
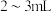
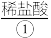 ,
, 溶液、
溶液、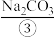 溶液,然后各滴入几滴
溶液,然后各滴入几滴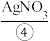 溶液,观察现象;再分别滴入少量
溶液,观察现象;再分别滴入少量 ,观察现象。回答下列问题:
,观察现象。回答下列问题:(1)AgNO3 在水中电离的电离方程式为
(2)①中分散质粒子直径为
(3)常温下,饱和②溶液
(4)从物质的组成来看,④属于
(5)查阅资料可知,硝酸具有强氧化性,其浓度越小,氧化能力越弱。对于反应

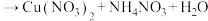 (未配平),该反应的化学方程式为
(未配平),该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是初中化学实验的几种常用仪器,请按要求填空。
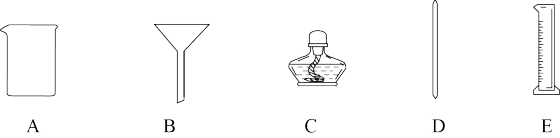
(1)①仪器C的名称叫_______ 。
②在读取E中液体体积时,视线应与凹液面的最低处_______ 。
(2)①进行过滤操作,除铁架台、A和D外,还需要用到上述仪器中的_______ (填字母)。
②配制一定质量分数的NaCl溶液,还必须补充的一种仪器是_______ 。

(1)①仪器C的名称叫
②在读取E中液体体积时,视线应与凹液面的最低处
(2)①进行过滤操作,除铁架台、A和D外,还需要用到上述仪器中的
②配制一定质量分数的NaCl溶液,还必须补充的一种仪器是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】选择合适的实验方法,将序号填在横线上。
A 加热蒸发 B 升华 C 重结晶 D 分液 E 蒸馏 F 过滤
(1)____ 分离饱和食盐水与沙子混合物。
(2)____ 从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
(3)____ 分离水和汽油混合物。
(4)____ 分离CCl4(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
A 加热蒸发 B 升华 C 重结晶 D 分液 E 蒸馏 F 过滤
(1)
(2)
(3)
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】单质碘有非常重要的用途,从海带燃烧后所得的海带灰中提取碘是单质碘的制备方法之一:海带燃烧后所得的海带灰中含有 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:

请回答下列问题:
(1)步骤③的实验操作名称是______ (填“过滤”或“蒸发”);
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是______ (填“氯水”或“稀盐酸”);
(3)I-被氧化为I2的离子方程式为____________ ;
(4)工业上合成氨的反应为: ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为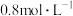
①用N2表示该反应的速率为______ ;
②其他条件不变时,升高温度,该反应的反应速率将______ (填“增大”或“减小”)。
 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
请回答下列问题:
(1)步骤③的实验操作名称是
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是
(3)I-被氧化为I2的离子方程式为
(4)工业上合成氨的反应为:
 ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为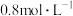
①用N2表示该反应的速率为
②其他条件不变时,升高温度,该反应的反应速率将
您最近一年使用:0次




