高铁酸钾( 极易溶于水)是优良的多功能水处理剂,其原理如图所示。
极易溶于水)是优良的多功能水处理剂,其原理如图所示。
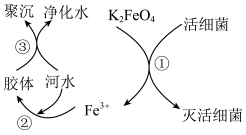
(1) 按物质类别属于
按物质类别属于___________ 。
A.酸 B.盐 C.复盐 D.氧化物
请举例一种和 同一类别的物质
同一类别的物质___________ 。
(2)①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(4)净水利用了 胶体的性质,请写出
胶体的性质,请写出 胶体制备的化学方程式
胶体制备的化学方程式___________ ,提纯所制 胶体常用的方法是
胶体常用的方法是___________ (填实验名称)。
(5)某同学往 胶体中逐滴滴入稀硫酸溶液,出现的现象是
胶体中逐滴滴入稀硫酸溶液,出现的现象是____________ 分析出现该现象的原因是___________ 。
(6) 溶液可以将池塘淤泥里的
溶液可以将池塘淤泥里的 氧化得到无色无味的气体从而起到除臭的作用,0.1mol
氧化得到无色无味的气体从而起到除臭的作用,0.1mol 可以反应标况下的氨气
可以反应标况下的氨气___________ L,为研究这个反应,某同学配制一定物质的量浓度的氨水,将标况下400体积的氨气通入1体积水中,理论上可以得到___________ mol/L密度为0.95g/mL的氨水。
 极易溶于水)是优良的多功能水处理剂,其原理如图所示。
极易溶于水)是优良的多功能水处理剂,其原理如图所示。
(1)
 按物质类别属于
按物质类别属于A.酸 B.盐 C.复盐 D.氧化物
请举例一种和
 同一类别的物质
同一类别的物质(2)①中活细菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)净水利用了
 胶体的性质,请写出
胶体的性质,请写出 胶体制备的化学方程式
胶体制备的化学方程式 胶体常用的方法是
胶体常用的方法是(5)某同学往
 胶体中逐滴滴入稀硫酸溶液,出现的现象是
胶体中逐滴滴入稀硫酸溶液,出现的现象是(6)
 溶液可以将池塘淤泥里的
溶液可以将池塘淤泥里的 氧化得到无色无味的气体从而起到除臭的作用,0.1mol
氧化得到无色无味的气体从而起到除臭的作用,0.1mol 可以反应标况下的氨气
可以反应标况下的氨气
更新时间:2024-02-17 16:27:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有Na、O、S、H四种元素,请选用其中一种或几种元素组成符合下列要求的物质,完成下列转化:(用化学方程式表达)
(1)单质 → 化合物:_______ ;
(2)酸 → 盐:_______ ;
(3)酸性氧化物 → 盐:_______ ;
(4)碱性氧化物 → 碱:_______ 。
(5)碱+酸式盐→ :_______ 。
(1)单质 → 化合物:
(2)酸 → 盐:
(3)酸性氧化物 → 盐:
(4)碱性氧化物 → 碱:
(5)碱+酸式盐→ :
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图是依据一定的分类标准,对某些物质与水反应情况进行分类:
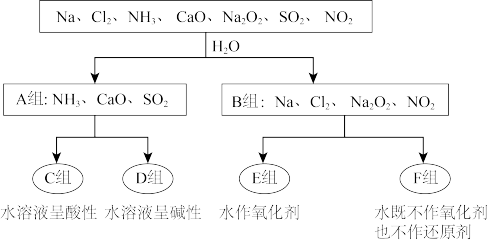
(1)根据物质与水反应的情况,这种分类方法叫_______ ,分成A、B组的分类依据是_______ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为_______ (填序号)。
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是_______ (填化学式),写出B组中红棕色气体与水反应的化学方程式_______ 。
(4)工业上常用D组中的_______ (填化学式)消除C组中物质对大气的污染。
(5)实验室用Al3+制备 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为_______
(6)C组中某一物质可使酸性 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因_______ 。
(7)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是_______ (填字母)。
a.碳氧化物 b.硫氧化物 c.氮氧化物

(1)根据物质与水反应的情况,这种分类方法叫
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是
(4)工业上常用D组中的
(5)实验室用Al3+制备
 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为(6)C组中某一物质可使酸性
 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因(7)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是
a.碳氧化物 b.硫氧化物 c.氮氧化物
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】中国青铜器制作精美,在世界青铜器中享有极高的声誉和艺术价值,代表着中国5000多年青铜发展的高超技术与文化,青铜器在出土的时候,由于时间久远,其表面有一层“绿锈”。“绿锈”俗称“铜绿”,是铜和空气中的水蒸气,CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
铜 铜绿
铜绿 A
A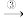 Cu(OH)2
Cu(OH)2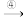 B
B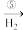 Cu
Cu
(1)从物质分类标准看,“铜绿”属于___ (填字母),生成铜绿的化学方程式是___ 。
A.酸 B.碱 C.盐 D.氧化物
(2)B的名称是___ 。
(3)请写出铜绿与盐酸反应的化学方程式___ 。
(4)上述转化过程中属于氧化还原反应的是___ (填序号)。
铜
 铜绿
铜绿 A
A Cu(OH)2
Cu(OH)2 B
B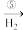 Cu
Cu(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)B的名称是
(3)请写出铜绿与盐酸反应的化学方程式
(4)上述转化过程中属于氧化还原反应的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为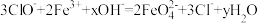
(1)上述反应中的x=_______ ,y=_______ 。
(2)上述反应中氧化剂为_______ ;还原产物为_______ 。
(3)由上述反应可知,氧化性强弱:
_______ (填“>”或“<”,下同) ;还原性强弱:
;还原性强弱:
_______  。
。
(4)请用单线桥法表示该反应中电子的转移情况:_______ 。
(5)已知: 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体具有吸附性。
胶体具有吸附性。
① 在处理饮用水的过程中
在处理饮用水的过程中_______ (填“发生了”或“未发生”)氧化还原反应。
② 胶体为
胶体为_______ 色,写出区分胶体与溶液的操作及现象:_______ 。
 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为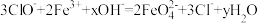
(1)上述反应中的x=
(2)上述反应中氧化剂为
(3)由上述反应可知,氧化性强弱:

 ;还原性强弱:
;还原性强弱:
 。
。(4)请用单线桥法表示该反应中电子的转移情况:
(5)已知:
 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体具有吸附性。
胶体具有吸附性。①
 在处理饮用水的过程中
在处理饮用水的过程中②
 胶体为
胶体为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是_______ ,只有还原性的是_______ ,既有氧化性又有还原性的是_______ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②N2O4+H2O→HNO3+HNO2 ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是_______ (填序号)。
Ⅱ.根据胶体制备和性质完成以下问题
(3)某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加几滴饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl。
(a)判断胶体制备是否成功,可利用胶体的_______ 。
(b)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到_______ ,其原因是_______ 。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会_______ ,原因是_______ 。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会_______ ,原因是_______ 。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②N2O4+H2O→HNO3+HNO2 ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是
Ⅱ.根据胶体制备和性质完成以下问题
(3)某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加几滴饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl。
(a)判断胶体制备是否成功,可利用胶体的
(b)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.根据下表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填入对应“答案”的空格中。
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是_____________ 。
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有_______________ 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是:Na2CO3_______ NaHCO3(填“>”或“<”)。
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为__________ L(标准状况)。
| 实验操作 | 答案 | 实验现象 |
| (1)让一束光线通过Fe(OH)3胶体 | A.呈蓝色 B.生成白色胶状沉淀 C.呈现光亮“通路” D.产生红褐色沉淀 | |
| (2)向盛有FeCl3溶液的试管中加入NaOH溶液 | ||
| (3)向Al2(SO4)3溶液中滴加氨水 | ||
| (4)向土豆片上滴加碘水 |
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
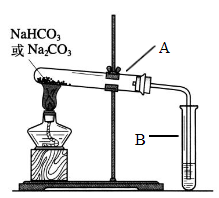
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列十种物质:①H2 ②铝 ③CH3COOH ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3 ⑩NaHSO4。
⑩NaHSO4。
(1)按物质的分类方法回答下列问题 填序号
填序号 :属于非电解质的是
:属于非电解质的是_______ ;属于电解质的是_______ ;能导电的是_______ 。
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为_______ 。
(3)写出③和⑦反应的离子方程式为_______ ,34.2g ⑨溶于水配成250mL溶液,SO 的物质的量浓度为
的物质的量浓度为_______ mol·L-1。
(4)过量的④通入⑥的溶液中反应的离子方程式为_______ 。
(5)将⑩的溶液加入⑥的溶液中至溶液呈中性时反应的离子方程式为_______ 。
 ⑩NaHSO4。
⑩NaHSO4。(1)按物质的分类方法回答下列问题
 填序号
填序号 :属于非电解质的是
:属于非电解质的是(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
(3)写出③和⑦反应的离子方程式为
 的物质的量浓度为
的物质的量浓度为(4)过量的④通入⑥的溶液中反应的离子方程式为
(5)将⑩的溶液加入⑥的溶液中至溶液呈中性时反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为测定某抗胃酸药片中碳酸钙的质量分数(设该药片中的其他成分不与盐酸或氢氧化钠反应):
I.向0.1000 g药片粉末中依次加入20.00 mL蒸馏水、25.00 mL 0.1000 mol/L稀盐酸,使之充分反应。
II.中和过量的盐酸,消耗0.1000 mol/L NaOH溶液13.00 mL。
请计算:
(1)II中消耗NaOH的物质的量为_______ mol。
(2)0.1000 g药片消耗HCl的物质的量为_______ mol。
(3)药片中碳酸钙的质量分数为_______ 。
I.向0.1000 g药片粉末中依次加入20.00 mL蒸馏水、25.00 mL 0.1000 mol/L稀盐酸,使之充分反应。
II.中和过量的盐酸,消耗0.1000 mol/L NaOH溶液13.00 mL。
请计算:
(1)II中消耗NaOH的物质的量为
(2)0.1000 g药片消耗HCl的物质的量为
(3)药片中碳酸钙的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)含有3.01×1023个H的H2O,其H2O物质的量是________ ;其H2O中含有电子的个数为______________ 。
(2)______ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________ 。
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,(注:体积分数即为物质的量分数)
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为________
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比___________ ,原子数目之比为___________ ,密度比为___________ ,氧元素的质量比为__________ 。
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为____________ ;R的相对原子质量为_____________ 。
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为___________ ;从中取出10mL,将这10mL溶液用水稀释到50mL,所得溶液中溶质的物质的量浓度为______________ 。
(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为
您最近一年使用:0次
【推荐1】(1)已知:氢化钠(NaH)为白色晶体,其中H-有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价,写出其化学反应方程式,并用双线桥标出电子转移的方向与数目______________________
(2)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用A粉还原NO3-,发生的反应可表示如下,请配平下列反应方程式:
____ 、____ 、____ 、____ 、____ 、___ 、
(3)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:
①该反应的氧化剂是____________ 氧化产物与还原产物的物质的量比是__________
②如果反应生成0.3mol的单质碘,则转移的电子数目是_____________
③先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,静置后观察到的现象是_________________________
(2)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用A粉还原NO3-,发生的反应可表示如下,请配平下列反应方程式:

(3)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:

①该反应的氧化剂是
②如果反应生成0.3mol的单质碘,则转移的电子数目是
③先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,静置后观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】目前新能源技术被不断利用,高铁电池技术就是科研机构着力研究的一个方向。
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是___________ 。
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:
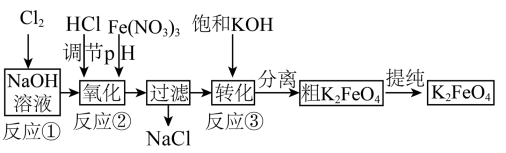
①写出反应①的离子方程式___________ 。
②请写出生产流程中“转化”(反应③)的化学方程式___________ 。
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)___________ Ksp(Na2FeO4)(填“>”“<”或“=”)。
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___________ 溶液。
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是___________ 。
(4) 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
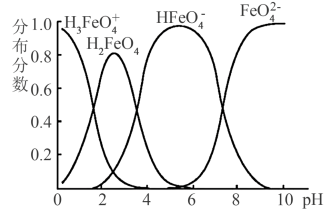
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO 的分布分数的变化情况是
的分布分数的变化情况是___________ 。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,___________ 转化为___________ 。(填化学式)
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:

①写出反应①的离子方程式
②请写出生产流程中“转化”(反应③)的化学方程式
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4
 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是(4)
 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO
 的分布分数的变化情况是
的分布分数的变化情况是②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,
您最近一年使用:0次
【推荐3】(1)用双线桥法标明该反应中电子转移的方向和数目:
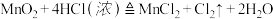
______________
(2)配平下列化学反应方程式_____________

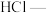



(3)写出过氧化钠与二氧化碳反应的化学方程式____________________________________
(4)写出氯气与冷的氢氧化钠反应的化学方程式______________________________________
(5)交警检测司机是否酒后驾车,是让司机向酒精检测仪吹气,其工作原理是在硫酸的环境中,重铬酸钾( )与乙醇(
)与乙醇( ,其中C为
,其中C为 价)发生氧化还原反应,重铬酸钾被还原成硫酸铬(
价)发生氧化还原反应,重铬酸钾被还原成硫酸铬( ),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式
),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式___________________________
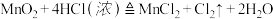
(2)配平下列化学反应方程式

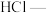



(3)写出过氧化钠与二氧化碳反应的化学方程式
(4)写出氯气与冷的氢氧化钠反应的化学方程式
(5)交警检测司机是否酒后驾车,是让司机向酒精检测仪吹气,其工作原理是在硫酸的环境中,重铬酸钾(
 )与乙醇(
)与乙醇( ,其中C为
,其中C为 价)发生氧化还原反应,重铬酸钾被还原成硫酸铬(
价)发生氧化还原反应,重铬酸钾被还原成硫酸铬( ),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式
),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式
您最近一年使用:0次



