(1)用双线桥法标明该反应中电子转移的方向和数目:
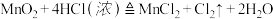
______________
(2)配平下列化学反应方程式_____________

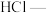



(3)写出过氧化钠与二氧化碳反应的化学方程式____________________________________
(4)写出氯气与冷的氢氧化钠反应的化学方程式______________________________________
(5)交警检测司机是否酒后驾车,是让司机向酒精检测仪吹气,其工作原理是在硫酸的环境中,重铬酸钾( )与乙醇(
)与乙醇( ,其中C为
,其中C为 价)发生氧化还原反应,重铬酸钾被还原成硫酸铬(
价)发生氧化还原反应,重铬酸钾被还原成硫酸铬( ),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式
),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式___________________________
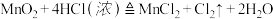
(2)配平下列化学反应方程式

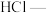



(3)写出过氧化钠与二氧化碳反应的化学方程式
(4)写出氯气与冷的氢氧化钠反应的化学方程式
(5)交警检测司机是否酒后驾车,是让司机向酒精检测仪吹气,其工作原理是在硫酸的环境中,重铬酸钾(
 )与乙醇(
)与乙醇( ,其中C为
,其中C为 价)发生氧化还原反应,重铬酸钾被还原成硫酸铬(
价)发生氧化还原反应,重铬酸钾被还原成硫酸铬( ),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式
),乙醇被氧化成二氧化碳,请书写出它们反应的化学方程式
19-20高二·浙江·期末 查看更多[1]
(已下线)【新东方】2020-59
更新时间:2020-02-27 17:19:35
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】金属钛(Ti)被广泛应用于飞机、火箭和人造卫星等领域,可通过下面的转化制取:

(1)“反应1”生成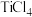 。若有14.2g
。若有14.2g 参与反应,则
参与反应,则 在标准状况下的体积约
在标准状况下的体积约___________ L;反应生成的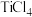 物质的量是
物质的量是___________ mol。
(2) 可以用高锰酸钾与浓盐酸反应得到:
可以用高锰酸钾与浓盐酸反应得到: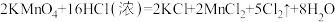 ,用
,用双线桥法 表示该反应电子转移的方向和数目:___________ 。
(3)“反应2”须在无氧和非水性 溶剂中进行,原因是___________ 。
(4)“反应2”需在700℃—800℃条件下进行,该反应的化学方程式是___________ 。

(1)“反应1”生成
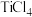 。若有14.2g
。若有14.2g 参与反应,则
参与反应,则 在标准状况下的体积约
在标准状况下的体积约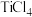 物质的量是
物质的量是(2)
 可以用高锰酸钾与浓盐酸反应得到:
可以用高锰酸钾与浓盐酸反应得到: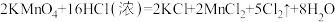 ,用
,用(3)“反应2”须在
(4)“反应2”需在700℃—800℃条件下进行,该反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钒具有众多优良的性能,用途十分广泛,有金属“维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分 V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,溶液中含 VO2+、K+、SO42-等离子。写出该反应的化学方程式:____________ 。
(2)向上述所得溶液中加入 KClO3 溶液,充分反应后,溶液中新增加了 VO2+、Cl-。写出并配平该反应的离子方程式,并标出电子转移的数目和方向_____ 。
(3)已知V2O5 能和盐酸反应生成氯气和VO2+,请再写一个离子方程式:________ ,说明还原性:SO32->Cl->VO2+。
(1)将废钒催化剂(主要成分 V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,溶液中含 VO2+、K+、SO42-等离子。写出该反应的化学方程式:
(2)向上述所得溶液中加入 KClO3 溶液,充分反应后,溶液中新增加了 VO2+、Cl-。写出并配平该反应的离子方程式,并标出电子转移的数目和方向
(3)已知V2O5 能和盐酸反应生成氯气和VO2+,请再写一个离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示为一定条件下含碘物质在水溶液中的转化关系图:
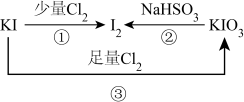
(1)转化①中的氧化剂是_____ (填化学式)
(2)转化①②③中,碘元素发生氧化反应的是_____ (填序号)
(3)转化③中,Cl2发生反应后可能生成以下物质中的_____ (填字母)。
A HCl B HClO C.HClO4
(4)转化②的化学方程式为KIO3+KOH+SO2→I2+K2SO4+H2O(未配平)
①配平反应②并用双线桥法表示电子转移的情况_______________
②每生成1.27gI2,反应中转移电子的物质的量为_____

(1)转化①中的氧化剂是
(2)转化①②③中,碘元素发生氧化反应的是
(3)转化③中,Cl2发生反应后可能生成以下物质中的
A HCl B HClO C.HClO4
(4)转化②的化学方程式为KIO3+KOH+SO2→I2+K2SO4+H2O(未配平)
①配平反应②并用双线桥法表示电子转移的情况
②每生成1.27gI2,反应中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的离子方程式。
(1)FeBr2溶液与Cl2反应
①Cl2少量:___________ ;
②n(FeBr2)∶n(Cl2)=1∶1:___________ ;
③Cl2过量:___________ 。
类似该反应的还有FeI2溶液与Cl2的反应。
(2)NH4HCO3溶液与NaOH溶液反应
①NaOH少量:___________ ;
②NaOH足量:___________ 。
类似该反应的还有NH4HSO4溶液或NH4Al(SO4)2溶液与NaOH溶液的反应。
(1)FeBr2溶液与Cl2反应
①Cl2少量:
②n(FeBr2)∶n(Cl2)=1∶1:
③Cl2过量:
类似该反应的还有FeI2溶液与Cl2的反应。
(2)NH4HCO3溶液与NaOH溶液反应
①NaOH少量:
②NaOH足量:
类似该反应的还有NH4HSO4溶液或NH4Al(SO4)2溶液与NaOH溶液的反应。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业上用粗铜电解精炼所产生的阳极泥[主要含硒化亚铜(Cu2Se)和碲化亚铜(Cu2Te)]为原料,进行综合回收利用的某种工艺流程如下:
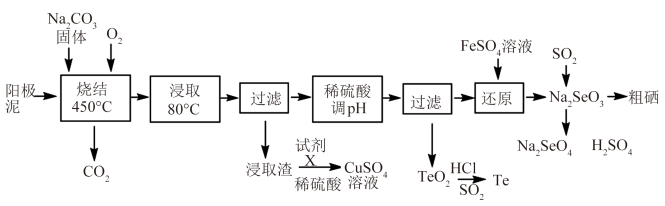
已知:①TeO2是两性氧化物,微溶于水。
②25℃时,亚碲酸(H2TeO3)的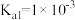 ,
,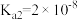 。
。
(1)“烧结”时的固体产物主要为Na2SeO3、Na2TeO4和Cu2O,该过程中Cu2Se反应的化学方程式为_______ 。
(2)还原过程的主要目的是将“烧结”时生成的少部分Na2TeO4进行转化,写出“还原”时反应的离子方程式_______ 。

已知:①TeO2是两性氧化物,微溶于水。
②25℃时,亚碲酸(H2TeO3)的
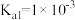 ,
,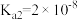 。
。(1)“烧结”时的固体产物主要为Na2SeO3、Na2TeO4和Cu2O,该过程中Cu2Se反应的化学方程式为
(2)还原过程的主要目的是将“烧结”时生成的少部分Na2TeO4进行转化,写出“还原”时反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】“铜都”安徽铜陵有许多黄铜矿(主要成分为CuFeS2,含少量Al2O3、SiO2),黄铜矿是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2 Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是_______ (填元素符号),若反应中转移0.3mol电子时,则标准状况下产生SO2的体积为_______ L。
(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式_________________ ,该反应中稀硝酸体现____________ (填“氧化性”、“还原性”或“酸性”)。
(3)焙烧黄铜矿还可得到Cu2O。将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0mol∙L-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为__________ 。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2
 Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式
(3)焙烧黄铜矿还可得到Cu2O。将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0mol∙L-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列各题。
(1)制备陶瓷是以黏土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为__________________ 。
(2)如果胃酸过多,可服用______________ (填写化学式)缓解症状,但如果患有胃溃疡,则不能服用,以防止胃穿孔。
(3)雕花玻璃是用氢氟酸对玻璃进行刻蚀而制成的,这一过程中发生反应的化学方程式为______________ 。
(4)二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂,工业上是用氯酸钠(NaClO3)与盐酸反应生产ClO2的,反应过程中同时会生成氯气。写出该反应的化学方程式____________ 。
(1)制备陶瓷是以黏土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为
(2)如果胃酸过多,可服用
(3)雕花玻璃是用氢氟酸对玻璃进行刻蚀而制成的,这一过程中发生反应的化学方程式为
(4)二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂,工业上是用氯酸钠(NaClO3)与盐酸反应生产ClO2的,反应过程中同时会生成氯气。写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有中学化学中常见的几种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生:H2O2→O2
(1)该反应中的还原剂的是________________ 。
(2)该反应中,发生还原反应的过程是__________________________ 。
(3)写出该反应的化学方程式(配平)__________________________________ 。
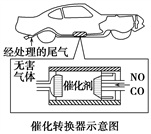
(4)随着人们环保意识的增强,许多汽车都已经装上了如图所示的尾气处理装置。在催化剂的作用下,尾气中两种主要的有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,写出该反应的化学方程式:___________________________ 。
(1)该反应中的还原剂的是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式(配平)
(4)随着人们环保意识的增强,许多汽车都已经装上了如图所示的尾气处理装置。在催化剂的作用下,尾气中两种主要的有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,写出该反应的化学方程式:

您最近一年使用:0次

 2Fe+3CO2的反应中,请回答下列问题:
2Fe+3CO2的反应中,请回答下列问题:

