乙酸乙酯是一种非常重要的有机化工原料,用途十分广泛.根据所学内容填空。
I.由乙烯合成乙酸乙酯的流程如下;
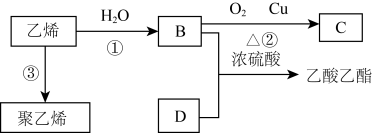
(1)写出B与D反应的化学方程式______ ;反应类型:______ ;
(2)写出反应③的化学方程式:______ 。
II.实验室用如图所示装置制备乙酸乙酯。
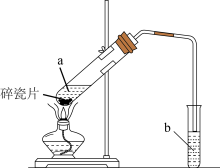
(3)实验前,向试管a中加入3 mL______ ,然后边振荡试管边慢慢加入2 mL______ 和2 mL乙酸。
(4)试管b中盛放的试剂是饱和______ 溶液。
(5)反应结束后,从试管b中分离出乙酸乙酯的方法是______ 。
(6)下列描述不能说明乙醇与乙酸的反应已达到化学平衡状态的有______ (填序号)。
a.单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
b.单位时间区,生成1 mol乙酸乙酯,同时生成1 mol乙酸
c.单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
d.正反应的速率与逆反应的速率相等
e.混合物中各物质的浓度不再变化
I.由乙烯合成乙酸乙酯的流程如下;

(1)写出B与D反应的化学方程式
(2)写出反应③的化学方程式:
II.实验室用如图所示装置制备乙酸乙酯。

(3)实验前,向试管a中加入3 mL
(4)试管b中盛放的试剂是饱和
(5)反应结束后,从试管b中分离出乙酸乙酯的方法是
(6)下列描述不能说明乙醇与乙酸的反应已达到化学平衡状态的有
a.单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
b.单位时间区,生成1 mol乙酸乙酯,同时生成1 mol乙酸
c.单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
d.正反应的速率与逆反应的速率相等
e.混合物中各物质的浓度不再变化
更新时间:2023-06-16 11:15:10
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】我国的二氧化碳排放力争在2030年前实现“碳达峰”,2060年前实现“碳中和”。为达成这一目标,一方面要减少碳排放,另一方面要尽量吸收不可避免的碳排放。
(1)以 为催化剂的光、热化学循环分解
为催化剂的光、热化学循环分解 反应,为吸收“碳排放”提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
反应,为吸收“碳排放”提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
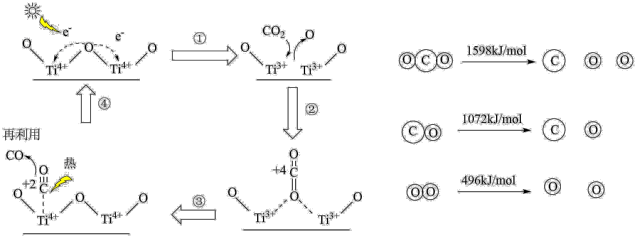
①上述过程中,能量的变化形式是由_______ 。
②写出 分解生成
分解生成 和
和 的热化学方程式
的热化学方程式_______ 。
(2) 催化重整为吸收“碳排放”的另一个新途径,回答下列问题:
催化重整为吸收“碳排放”的另一个新途径,回答下列问题:
①已知: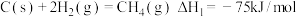
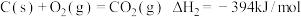
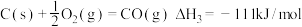
则催化重整反应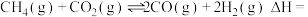
_______  。
。
②若在恒温、恒容的密闭容器中,充入 和
和 ,在一定条件下发生催化重整反应,下列描述不能说明该反应已经达到平衡状态的是
,在一定条件下发生催化重整反应,下列描述不能说明该反应已经达到平衡状态的是_______ (填标号)。
A. 和
和 的物质的量不变 B.混合气体的密度保持不变
的物质的量不变 B.混合气体的密度保持不变
C.容器中气体的压强保持不变 D.
③下列条件能够加快催化重组反应速率的是_______ 。
A.升高温度 B.充入一定量的二氧化碳
C.保持体积不变,充入 使压强增大 D.保持压强不变,充入
使压强增大 D.保持压强不变,充入 使容积增大
使容积增大
(1)以
 为催化剂的光、热化学循环分解
为催化剂的光、热化学循环分解 反应,为吸收“碳排放”提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
反应,为吸收“碳排放”提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
①上述过程中,能量的变化形式是由
②写出
 分解生成
分解生成 和
和 的热化学方程式
的热化学方程式(2)
 催化重整为吸收“碳排放”的另一个新途径,回答下列问题:
催化重整为吸收“碳排放”的另一个新途径,回答下列问题:①已知:
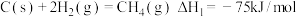
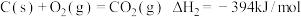
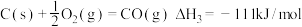
则催化重整反应
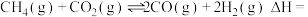
 。
。②若在恒温、恒容的密闭容器中,充入
 和
和 ,在一定条件下发生催化重整反应,下列描述不能说明该反应已经达到平衡状态的是
,在一定条件下发生催化重整反应,下列描述不能说明该反应已经达到平衡状态的是A.
 和
和 的物质的量不变 B.混合气体的密度保持不变
的物质的量不变 B.混合气体的密度保持不变C.容器中气体的压强保持不变 D.

③下列条件能够加快催化重组反应速率的是
A.升高温度 B.充入一定量的二氧化碳
C.保持体积不变,充入
 使压强增大 D.保持压强不变,充入
使压强增大 D.保持压强不变,充入 使容积增大
使容积增大
您最近一年使用:0次
【推荐2】利用化学反应原理的知识可以有效的服务于生产和生活当中。
I.工业生产中经常用活性炭还原处理氮氧化物,起到了很好的效果。有关反应为:
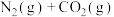 。
。
(1)写出上述反应的平衡常数表达式______ 。
(2)在2 L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
①结合表中数据,判断该反应的
______ 0(填“>”或“<”)。
②判断该反应达到平衡状态的依据是______ (填字母)。
A. B.容器内各气体浓度恒定
B.容器内各气体浓度恒定
C.容器内压强恒定 D.容器内气体平均相对分子质量恒定
II.某同学设计利用一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电、环保三位一体的结合。
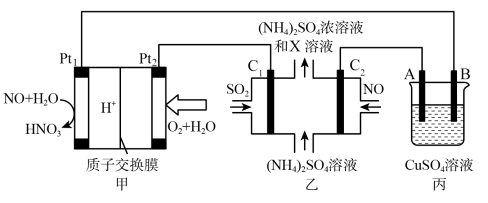
(3)甲装置中 上的电极反应式为
上的电极反应式为______ ;每转移1 mol电子,通过质子交换膜的 的物质的量为
的物质的量为______ 。
(4)乙装置中 上的电极反应式为
上的电极反应式为______ ,乙装置中物质X是______ (填化学式)。
(5)装置丙用于含锌粗铜的精炼。装置中电极A是______ (填“粗铜”或“纯铜”),工作一段时间后, 溶液的浓度将
溶液的浓度将______ (填“增大”“减小”或“不变”)。
I.工业生产中经常用活性炭还原处理氮氧化物,起到了很好的效果。有关反应为:

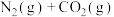 。
。(1)写出上述反应的平衡常数表达式
(2)在2 L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
| 实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时 的物质的量/mol 的物质的量/mol |
| 1 | 700 | 0.40 | 0.09 |
| 2 | 800 | 0.24 | 0.08 |

②判断该反应达到平衡状态的依据是
A.
 B.容器内各气体浓度恒定
B.容器内各气体浓度恒定C.容器内压强恒定 D.容器内气体平均相对分子质量恒定
II.某同学设计利用一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电、环保三位一体的结合。

(3)甲装置中
 上的电极反应式为
上的电极反应式为 的物质的量为
的物质的量为(4)乙装置中
 上的电极反应式为
上的电极反应式为(5)装置丙用于含锌粗铜的精炼。装置中电极A是
 溶液的浓度将
溶液的浓度将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】化学反应的速率和限度对人类生产生活有重要的意义。
I.已知 甲同学通过测定溶液变浑浊的时间,研究温度、浓度对化学反应速率的影响,设计实验如下:
甲同学通过测定溶液变浑浊的时间,研究温度、浓度对化学反应速率的影响,设计实验如下:
(1)由实验可知,
___________ ,
___________ 。
(2)为探究浓度对化学反应速率的影响,应选择实验________ 和_________ (填实验序号)。
(3)把 、
、 、
、 从小到大排序
从小到大排序___________ 。
II.在一定温度下,体积为5L的恒容密闭容器中发生反应: ,各物质的物质的量随时间变化的关系如图所示。请回答下列问题
,各物质的物质的量随时间变化的关系如图所示。请回答下列问题

(4)该反应达最大限度时Y的转化率为;2min内用X表示的反应速率为___________ ,若初始压强为 ,则平衡时
,则平衡时
___________ (用含 的表达式表示)。
的表达式表示)。
(5)下列描述能表示该反应达平衡状态的是___________ (填标号)。
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的密度不再发生变化
E.容器内气体的平均相对分子质量不再改变
I.已知
 甲同学通过测定溶液变浑浊的时间,研究温度、浓度对化学反应速率的影响,设计实验如下:
甲同学通过测定溶液变浑浊的时间,研究温度、浓度对化学反应速率的影响,设计实验如下:| 实验序号 | 实验温度/K | 有关物质 | 出现浑浊所需时间/s | ||||
| Na2S2O3溶液 | H2SO4溶液 | H2O | |||||
| V/mL | c/ | V/mL | c/ | V/mL | |||
| A | 298 | 4 | 0.1 | 4 | 0.1 | 2 |  |
| B |  | 4 | 0.1 | 5 | 0.1 |  |  |
| C | 323 | 4 | 0.1 |  | 0.1 | 1 |  |
(1)由实验可知,


(2)为探究浓度对化学反应速率的影响,应选择实验
(3)把
 、
、 、
、 从小到大排序
从小到大排序II.在一定温度下,体积为5L的恒容密闭容器中发生反应:
 ,各物质的物质的量随时间变化的关系如图所示。请回答下列问题
,各物质的物质的量随时间变化的关系如图所示。请回答下列问题
(4)该反应达最大限度时Y的转化率为;2min内用X表示的反应速率为
 ,则平衡时
,则平衡时
 的表达式表示)。
的表达式表示)。(5)下列描述能表示该反应达平衡状态的是
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的密度不再发生变化
E.容器内气体的平均相对分子质量不再改变
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】物质H是一种重要的精细化工原料和有机合成中间体。其合成方法如图所示。

已知:
①R-CH2-COOH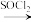 R-CH2-COCl
R-CH2-COCl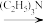

②CH3COCH2COOC2H5+R-CHO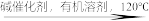

回答下列问题。
(1)物质A的名称___________ 。H的分子式是___________ 。
(2)A→B的反应类型为___________ 。
(3)B→C的反应方程式为___________ 。
(4)下表研究了E→F的反应过程中某些因素对反应的影响。
试剂用量:E:0.04 mol;乙醛:0.03 mol;碱催化剂:0.02 mol;有机溶剂:30 mL
从表格中的数据可知,在E→F的反应中,应选择___________ 作为催化剂,___________ 作为溶剂。
(5)H的一种同系物X比H多一个C原子,则X可能的结构有___________ 种。其中核磁共振氢谱中吸收峰面积之比为6:2:2:1:1的结构简式为___________ 。
(6)根据题中所给信息,设计一个由物质E和正丁醛合成3-甲基-5-正丙基苯酚 的路线
的路线_______ 。

已知:
①R-CH2-COOH
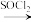 R-CH2-COCl
R-CH2-COCl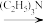

②CH3COCH2COOC2H5+R-CHO
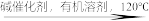

回答下列问题。
(1)物质A的名称
(2)A→B的反应类型为
(3)B→C的反应方程式为
(4)下表研究了E→F的反应过程中某些因素对反应的影响。
试剂用量:E:0.04 mol;乙醛:0.03 mol;碱催化剂:0.02 mol;有机溶剂:30 mL
| 反应温度/℃ | 碱催化剂 | 有机溶剂 | 产率/% |
| 80 | 哌啶 | 乙醇 | 47 |
| 80 | 甲醇钠 | 乙醇 | 40 |
| 100 | 叔丁醇钾 | 叔丁醇 | 41 |
| 80 | 碳酸钠 | 乙腈 | 89 |
| 80 | 碳酸钾 | 乙腈 | 78 |
| 80 | 碳酸钠 | 乙醇 | 95 |
(5)H的一种同系物X比H多一个C原子,则X可能的结构有
(6)根据题中所给信息,设计一个由物质E和正丁醛合成3-甲基-5-正丙基苯酚
 的路线
的路线
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】环己烯常用于有机合成。现通过下列流程,以环己烯为原料合成环醚、聚酯、橡胶,其中F可以作内燃机的抗冻剂,J分子中无饱和碳原子。
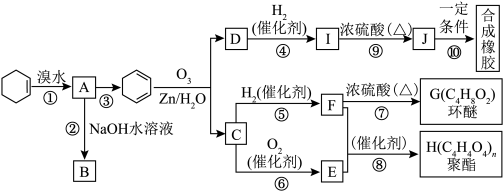
已知:R1—CH===CH—R2 R1—CHO+R2—CHO
R1—CHO+R2—CHO
(1)③的反应条件是_________________________________________________ 。
(2)A的名称是_______________________________________________ 。
(3)有机物B和I的关系为________ (填字母)。
A.同系物 B.同分异构体
C.都属于醇类 D.都属于烃
(4)①~⑩中属于取代反应的________________________________________ 。
(5)写出反应⑩的化学方程式____________________________________ 。
(6)写出两种D的属于酯类的链状同分异构体的结构简式:_____________ 。

已知:R1—CH===CH—R2
 R1—CHO+R2—CHO
R1—CHO+R2—CHO(1)③的反应条件是
(2)A的名称是
(3)有机物B和I的关系为
A.同系物 B.同分异构体
C.都属于醇类 D.都属于烃
(4)①~⑩中属于取代反应的
(5)写出反应⑩的化学方程式
(6)写出两种D的属于酯类的链状同分异构体的结构简式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】烃A的分子量为92且所有碳原子都在同一平面上。一种由烃A制备水杨酸的过程如下∶
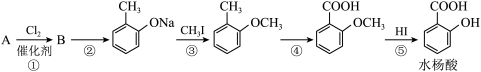
(1)请写出由B生成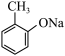 的反应方程式∶
的反应方程式∶_________________________________ ;
(2)在合成线路中,设计第③和第⑤这两步反应的目的是∶_____________________ 。
(3)若与水杨酸相关的转化关系如下∶
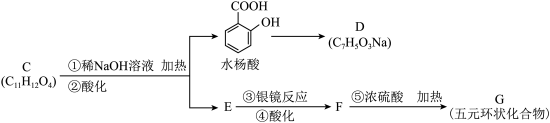
请用一个化学反应证明水杨酸中两官能团酸性差异∶____________________ 。
(4)①反应类型为∶_________ 、___________ ;
(5) G的结构简式为∶___________ ; 官能团名称∶_____________ ;
(6)请写出同时符合下列要求的水杨酸的所有同分异构体的结构简式______________ 。
①滴入FeCl3溶液,发生显色反应;
②能发生银镜反应∶
③苯环上一氯代物有两种。

(1)请写出由B生成
 的反应方程式∶
的反应方程式∶(2)在合成线路中,设计第③和第⑤这两步反应的目的是∶
(3)若与水杨酸相关的转化关系如下∶

请用一个化学反应证明水杨酸中两官能团酸性差异∶
(4)①反应类型为∶
(5) G的结构简式为∶
(6)请写出同时符合下列要求的水杨酸的所有同分异构体的结构简式
①滴入FeCl3溶液,发生显色反应;
②能发生银镜反应∶
③苯环上一氯代物有两种。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】碳酸二乙酯( )常温下为无色清澈液体。主要用作硝酸纤维素、树脂和一些药物的溶剂,或有机合成的中间体。现用下列装置制备碳酸二乙酯。
)常温下为无色清澈液体。主要用作硝酸纤维素、树脂和一些药物的溶剂,或有机合成的中间体。现用下列装置制备碳酸二乙酯。

回答下列问题:
(1)甲装置主要用于制备光气(COCl2),先将仪器B中的四氯化碳加热至55~60℃,再缓缓滴加发烟硫酸。
①仪器B的名称是____________ 。②仪器A的侧导管a的作用是______________________ 。
(2)试剂X是____________ ,其作用是_____________________________________________ 。
(3)丁装置除了吸收COCl2外,还能吸收的气体是____________ (填化学式)。仪器B中四氯化碳与发烟硫酸(用SO3表示)反应只生成两种物质的量为1:1的产物,且均易与水反应,写出该反应化学方程式:________________________________________________ 。
(4)无水乙醇与光气反应生成氯甲酸乙酯,再继续与乙醇反应生成碳酸二乙酯。
①写出无水乙醇与光气反应生成氯甲酸乙酯的化学方程式:__________________________ 。
②若起始投入92.0g无水乙醇,最终得到碳酸二乙酯94.4g,则碳酸二乙酯的产率是______ (三位有效数字)
 )常温下为无色清澈液体。主要用作硝酸纤维素、树脂和一些药物的溶剂,或有机合成的中间体。现用下列装置制备碳酸二乙酯。
)常温下为无色清澈液体。主要用作硝酸纤维素、树脂和一些药物的溶剂,或有机合成的中间体。现用下列装置制备碳酸二乙酯。
化学式 | 熔点/℃ | 沸点℃ | 物理性质 |
COCl2 | -118 | 8.2 | 微溶于水,溶于芳烃、苯、四氯化碳、氯仿、乙酸等多数有机溶剂,遇水迅速水解,生成氯化氢 |
SO3 | 16.8 | 44.8 | 溶于水,并与水反应生成硫酸和放出大量的热 |
SO2Cl2 | -54.1 | 69.1 | 溶于乙酸、苯,与水反应生成H2SO4和HC1 |
CCl4 | -22.9 | 76.8 | 微溶于水,易溶于多数有机溶剂 |
(1)甲装置主要用于制备光气(COCl2),先将仪器B中的四氯化碳加热至55~60℃,再缓缓滴加发烟硫酸。
①仪器B的名称是
(2)试剂X是
(3)丁装置除了吸收COCl2外,还能吸收的气体是
(4)无水乙醇与光气反应生成氯甲酸乙酯,再继续与乙醇反应生成碳酸二乙酯。
①写出无水乙醇与光气反应生成氯甲酸乙酯的化学方程式:
②若起始投入92.0g无水乙醇,最终得到碳酸二乙酯94.4g,则碳酸二乙酯的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室制乙酸乙酯的主要装置如图所示,主要实验步骤如下:

①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按图示连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2mL产物时停止加热。撤下b试管并用力振荡,然后静置,待其中液体分层;
⑤分离出乙酸乙酯。
请回答下列问题:
(1)写出乙醇与乙酸进行反应的化学方程式_______ ,该反应类型是_______ 。
(2)b试管所盛的饱和碳酸钠溶液的作用是_______ 。
(3)装置中使用球形干燥管除起到冷凝作用外,另一重要作用是_______ ,步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式_______ 。
(4)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管b再测有机层的厚度,实验记录如表:实验
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_______ mL和_______ mol•L-1。
②分析实验_______ (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。

①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按图示连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2mL产物时停止加热。撤下b试管并用力振荡,然后静置,待其中液体分层;
⑤分离出乙酸乙酯。
请回答下列问题:
(1)写出乙醇与乙酸进行反应的化学方程式
(2)b试管所盛的饱和碳酸钠溶液的作用是
(3)装置中使用球形干燥管除起到冷凝作用外,另一重要作用是
(4)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管b再测有机层的厚度,实验记录如表:实验
| 实验编号 | 试管a中试剂 | 试管b试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol•L-1浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
②分析实验
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热3-5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。

(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:_______ ;与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是_______ 。
(2)甲试管中,混合溶液的加入顺序:_______ ;
(3)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有_______ (填序号)。
①混合物中各物质的浓度不再变化;
②单位时间里,生成1mol乙醇,同时生成1mol乙酸;
③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸。
(4)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用图中所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如表:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_______ mL和_______ mol·L-1。
②分析实验_______ (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(5)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产品产率为。_______ (产率%=(实际产量/理论产量)×100%)
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热3-5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。

(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:
(2)甲试管中,混合溶液的加入顺序:
(3)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有
①混合物中各物质的浓度不再变化;
②单位时间里,生成1mol乙醇,同时生成1mol乙酸;
③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸。
(4)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用图中所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如表:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层的 厚度/cm |
| A | 2mL乙醇、1mL乙酸、3mL 18mol·L-1浓硫酸 | 饱和Na2CO3溶液 | 3. 0 |
| B | 2mL乙醇、1mL乙酸、3mL H2O | 0. 1 | |
| C | 2mL乙醇、1mL乙酸、3mL 2mol·L-1 H2SO4 | 0. 6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0. 6 |
②分析实验
(5)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产品产率为。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】I、实验室用下图所示装置制备乙酸乙酯。
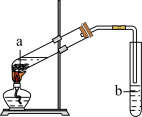
(1)试管a中生成乙酸乙酯的化学方程式是_______ 。
(2)试管a中试剂的添加顺序是先加入_______ ,再加入_______ ,最后加入乙酸。
(3)试管b中盛放的试剂是______ ,导气管不伸入液面下的理由是_______ 。
II、乳酸在生命化学中起重要作用,也是重要的化工原料。下图是获得乳酸的两种方法,其中A是一种常见的烃,它的产量可以用来衡量一个国家的石油化工发展水平。

(1)A→B的反应类型是_____ ;淀粉完全水解得到D,D的名称是________ 。
(2)B→C反应的化学方程式是________ 。
(3)乳酸在一定条件下可生成六元环酯(C6H8O4),其结构简式是________ 。

(1)试管a中生成乙酸乙酯的化学方程式是
(2)试管a中试剂的添加顺序是先加入
(3)试管b中盛放的试剂是
II、乳酸在生命化学中起重要作用,也是重要的化工原料。下图是获得乳酸的两种方法,其中A是一种常见的烃,它的产量可以用来衡量一个国家的石油化工发展水平。

(1)A→B的反应类型是
(2)B→C反应的化学方程式是
(3)乳酸在一定条件下可生成六元环酯(C6H8O4),其结构简式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】I.实验室可用如图甲所示装置探究石蜡油的分解实验。

(1)实验开始后,酸性高锰酸钾溶液中观察到的现象是_______ ;
II.实验装置也可以改为如图乙所示装置:在试管①中加入石蜡油和氧化铝,将试管②放在冷水中,在试管③中加入酸性高锰酸钾溶液。
(2)该实验中氧化铝的作用是_______ 。加入药品前,必须进行的操作是_______ 。装置中,冷水的作用是_______ 。
(3)试管②中的液体_______ (填“能”或“不能”)用于萃取溴水中的溴,说明理由:_______ 。
III.用图丙所示装置可制取乙酸乙酯。在试管a中加入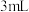 乙醇,然后边振荡试管边慢慢加入
乙醇,然后边振荡试管边慢慢加入 浓硫酸和
浓硫酸和 乙酸。
乙酸。

(4)图丙中装置A的导管应与装置_______ 的导管相连(填“B”或“C”),试管a中浓硫酸的作用是_______ 。
IV.用图丁所示的装置可比较醋酸、碳酸和硅酸的酸性强弱。
(5)图丁中E中盛装的试剂是_______ ,请写出F中发生反应的离子方程式_______ 。

(1)实验开始后,酸性高锰酸钾溶液中观察到的现象是
II.实验装置也可以改为如图乙所示装置:在试管①中加入石蜡油和氧化铝,将试管②放在冷水中,在试管③中加入酸性高锰酸钾溶液。
(2)该实验中氧化铝的作用是
(3)试管②中的液体
III.用图丙所示装置可制取乙酸乙酯。在试管a中加入
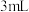 乙醇,然后边振荡试管边慢慢加入
乙醇,然后边振荡试管边慢慢加入 浓硫酸和
浓硫酸和 乙酸。
乙酸。
(4)图丙中装置A的导管应与装置
IV.用图丁所示的装置可比较醋酸、碳酸和硅酸的酸性强弱。
(5)图丁中E中盛装的试剂是
您最近一年使用:0次




