氨气在工农业生产中有重要应用。
(1)工业合成氨的化学方程式为___________ 。
(2)某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。
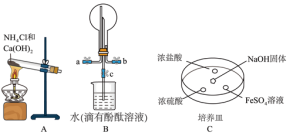
①实验室用装置A制备氨气的化学方程式为___________ 。
②用装置B收集氨时,进气口是___________ (选填“a”或“b”)。打开装置B中的活塞c,烧瓶内产生了红色喷泉,则说明氨具有的性质是___________ ,___________ 。
③向C中NaOH固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___________ ,检验白烟中阳离子的方法是:取少量白烟于试管中,___________ 。FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有Fe2++2NH3·H2O=Fe(OH)2↓+2 和
和___________ 。
(1)工业合成氨的化学方程式为
(2)某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。

①实验室用装置A制备氨气的化学方程式为
②用装置B收集氨时,进气口是
③向C中NaOH固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 和
和
更新时间:2023-05-23 10:40:50
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
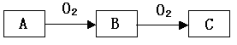
(1)若A是一种黄色单质固体,则B→C的化学方程式为_______ 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为_______ ,试用化学方程式表示该物质与二氧化碳气体的反应_______ 。将C长期露置于空气中,最后将变成物质D,D的化学式为____ 。
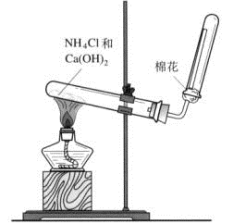
(3)若C是红棕色气体,A是一种能使湿润的红色石蕊试纸变蓝的气体。图是实验室制取A气体的装置,请结合所学知识,回答下列问题:写出实验室制取A的化学方程式_______ 。

(1)若A是一种黄色单质固体,则B→C的化学方程式为
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
(3)若C是红棕色气体,A是一种能使湿润的红色石蕊试纸变蓝的气体。图是实验室制取A气体的装置,请结合所学知识,回答下列问题:写出实验室制取A的化学方程式

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】I.某实验小组利用以下装置制取氨气并探究氨气的性质:

(1)装置A中发生反应的化学方程式为_____ 。
(2)装置B中的干燥剂是_____ (填名称)。
(3)装置C中的现象是_____ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_____ 。
(5)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是_____ (填“E”、“F”、“G”或“H”)。
Ⅱ.为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题

实验现象:
A中氧化铜全部转化成光亮的红色固体;B中U形管内物质变蓝;
(6)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是_____ 。
(7)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈_____ 色。
【实验结论】
(8)氧化铜和氨气发生反应,化学方程式是_____ 。

(1)装置A中发生反应的化学方程式为
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是
Ⅱ.为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题

实验现象:
A中氧化铜全部转化成光亮的红色固体;B中U形管内物质变蓝;
(6)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是
(7)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈
【实验结论】
(8)氧化铜和氨气发生反应,化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】同学们用下列装置制取并收集干燥的氨气。(某些夹持仪器和导管已略去)

请回答下列问题:
(1)A中发生反应的化学方程式是_____ ,检查A中装置气密性的方法是_____ 。
(2)按气流方向,各装置接口的正确连接顺序是①→_______→_______→_______。_____
(3)B的作用是______ ,C中棉花的作用是______ 。
(4)证明氨气已收集满的方法是_____ ,所利用的氨气性质是_____ (用化学方程式表示)。
(5)实验结束后,为防止剩余氨气污染空气,可将蘸有_____ 的棉花放在A的导管口。

请回答下列问题:
(1)A中发生反应的化学方程式是
(2)按气流方向,各装置接口的正确连接顺序是①→_______→_______→_______。
(3)B的作用是
(4)证明氨气已收集满的方法是
(5)实验结束后,为防止剩余氨气污染空气,可将蘸有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物X由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝的气体Y,Y为纯净物;取3.01 g X,用含HCl 0.0600 mol的盐酸完全溶解得溶液A,将溶液A分成A1和A2两等份,完成如下实验(白色沉淀C可溶于NaOH溶液):

请回答:
(1)组成X的四种元素是N、H和________ (填元素符号),X的化学式是________ 。
(2)溶液B通入过量CO2得到白色沉淀C的离子方程式是________ 。
(3)写出一个化合反应(用化学方程式或离子方程式表示)________ 。
要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“HCl+NH3=NH4Cl”相同。

请回答:
(1)组成X的四种元素是N、H和
(2)溶液B通入过量CO2得到白色沉淀C的离子方程式是
(3)写出一个化合反应(用化学方程式或离子方程式表示)
要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“HCl+NH3=NH4Cl”相同。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含NH4+废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
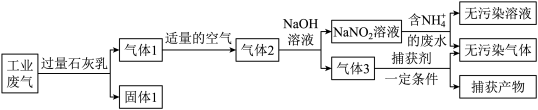
已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体1的主要成分有Ca(OH)2、__________ (填化学式)。
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为__________ g。
(3)用NaNO2溶液处理含NH4+废水反应的离子方程式为__________ 。
(4)验证废水中NH4+已基本除净的方法是___________ (写出操作、现象与结论)。
(5)气体1转化为气体2时空气不能过量的原因是__________ 。
(6)捕获剂捕获的气体主要是__________ (填化学式)。
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl。需选用的物质是__________ (填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤

已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体1的主要成分有Ca(OH)2、
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为
(3)用NaNO2溶液处理含NH4+废水反应的离子方程式为
(4)验证废水中NH4+已基本除净的方法是
(5)气体1转化为气体2时空气不能过量的原因是
(6)捕获剂捕获的气体主要是
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl。需选用的物质是
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】氮及其化合物在工农业生产、生活中被广泛使用,造福人类。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:
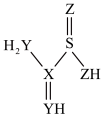
(1)硫元素在元素周期表中的位置为______ ;Y 的元素符号为______ 。
(2)下列说法错误的是______ (选填序号)。
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。
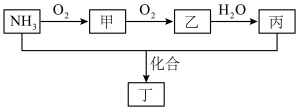
(3)NH3的电子式为______ 。
(4)图中,乙转化为丙的离子方程式为______ 。
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,______ ,将湿润的 红色石蕊试纸置于试管口,试纸变蓝。
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为______ 。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:

(1)硫元素在元素周期表中的位置为
(2)下列说法错误的是
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。

(3)NH3的电子式为
(4)图中,乙转化为丙的离子方程式为
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】三氯化铁溶液可腐蚀印刷电路板上的铜膜,腐蚀废液会污染环境。某小组为了从腐蚀废液(含有大量CuCl2、FeCl2和FeCl3)中回收铜,并将铁的化合物全部转化为腐蚀液原料循环使用,其流程如图。
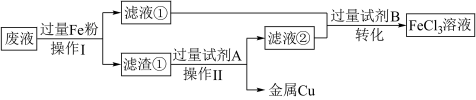
回答下列问题:
(1)操作Ⅰ的名称______ 。
(2)滤渣①中的成分_______ 。(用化学式表示)
(3)若选用Cl2作试剂B,则“转化”过程中发生反应的离子方程式为_______ ;若从“绿色化学”的角度来考虑,试剂B可以是 _______ 。
(4)取少量滤液②于试管中加入NaOH溶液,生成了白色絮状沉淀后迅速变成灰绿色,过一段时间会生成红褐色物质,请写出生成红褐色物质时发生的化学反应方程式_______ 。

回答下列问题:
(1)操作Ⅰ的名称
(2)滤渣①中的成分
(3)若选用Cl2作试剂B,则“转化”过程中发生反应的离子方程式为
(4)取少量滤液②于试管中加入NaOH溶液,生成了白色絮状沉淀后迅速变成灰绿色,过一段时间会生成红褐色物质,请写出生成红褐色物质时发生的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用如图所示方法制Fe(OH)2,但一般看不到白色的Fe(OH)2沉淀,原因是Fe(OH)2不稳定,极易被O2氧化生成Fe(OH)3.请回答:

(1)向氯化亚铁溶液中滴加氢氧化钠溶液反应的离子方程式:_______ ,现象是_______
(2)Fe(OH)2被O2 氧化的化学方程式是:_______ 。
(3)实验室保存FeCl2溶液常常加入铁粉,其作用是_______ (用离子方程式表示),检验FeCl2溶液是否变质,可向其中加入_______ (填化学式)溶液,观察现象。

(1)向氯化亚铁溶液中滴加氢氧化钠溶液反应的离子方程式:
(2)Fe(OH)2被O2 氧化的化学方程式是:
(3)实验室保存FeCl2溶液常常加入铁粉,其作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】(1)下列各图示中能较长时间看到Fe(OH)2白色沉淀的是___________ (填序号)。


(2)取20 mL未知浓度的氢氧化钠溶液,先通入一定量的CO2,然后向其中逐滴滴入0.2 mol·L-1的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图所示

通入一定量的CO2后所得溶液中溶质是___________ (填化学式),其物质的量之比为___________ 原氢氧化钠溶液的物质的量浓度为___________ 。


(2)取20 mL未知浓度的氢氧化钠溶液,先通入一定量的CO2,然后向其中逐滴滴入0.2 mol·L-1的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图所示

通入一定量的CO2后所得溶液中溶质是
您最近一年使用:0次



