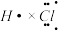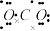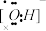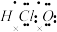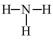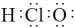立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为BCl3(g)+NH3(g)=BN(s)+3HCl(g),下列说法错误的是
| A.形成BCl3时B原子先激发后杂化,其激发态价电子排布式为:2s12p2 |
| B.元素电负性大小为N>B |
| C.反应混合物中所有化学键均为共价键 |
| D.BCl3的分子中所有原子都能达到8电子稳定结构 |
更新时间:2023-05-23 17:34:38
|
相似题推荐
单选题
|
适中
(0.65)
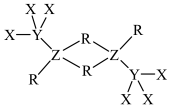
【推荐1】一种麻醉剂的分子结构如图所示。其中,X的原子核内只1个质子;元素Y、Z、W原子序数依次增大,且均位于X的下一周期:元素E的原子比W原子多8个电子。下列说法错误的是


A. 是一种强酸 是一种强酸 |
| B.元素Y和Z均可以形成多种单质 |
| C.元素W和E最高正化合价相同 |
D.非金属性: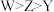 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA是阿伏加德罗常数的值。下列说法正确的是
| A.10 g H218O与D216O的混合物中所含中子数目为5NA |
| B.物质的量相同的CH4和NH3的共价键数之比为1:1 |
| C.1 mol H2和1 mol O2混合后,所含气体的体积约为44.8 L |
| D.常温下,0.5 mol Fe和足量浓硝酸混合,转移电子数为1.5NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】观察下列模型并结合有关信息进行判断,下列说法错误的是( )
| HCN | S8 | SF6 | B12结构单元 | |
| 结构模型 示意图 | 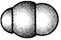 |  | 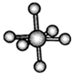 | 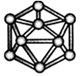 |
| 备注 | / | 易溶于CS2 | / | 熔点1873 K |
| A.HCN的结构式为H—C≡N,分子中“C≡N”键含有1个σ键和2个π键 |
| B.固态硫S8属于原子晶体,分子中S原子采用sp3杂化 |
| C.SF6是由极性键构成的非极性分子,分子构型为八面体型 |
| D.单质硼属于原子晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】CO2的应用领域广泛,是一种廉价易得的基本化工原料,我国提出力争在 2060 年前实现碳中和。碳中和:通过节能减排,植树造林,化工合成等治理 CO2的手段,使 CO2排放量减少甚至是回收利用,以此达到 CO2“零排放”的目的。在二氧化碳合成甲醇的研究中,催化剂是研究的关键。目前国内外研究主要集中于铜基催化剂,有学者提出了 CO2的转化过程如图所示。下列说法正确的是


| A.基态铜电子排布:[Ar]3d94s2 |
| B.甲酸乙酯是该过程的催化剂 |
| C.步骤④中有化学键的断裂和形成 |
| D.反应过程中,催化剂参与反应,降低了反应的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A. 是含有极性键的非极性分子 是含有极性键的非极性分子 | B.基态铬原子的价层电子排布式: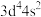 |
C. 的电子式: 的电子式: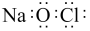 | D.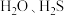 空间结构相同,键角也相等 空间结构相同,键角也相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同电子层结构,下列关系正确的是
| A.电负性:Z>Y>W>X |
| B.氢化物的稳定性:H2Y>HZ |
| C.质子数:c>d,离子的还原性:Y2->Z- |
| D.原子半径:X<W,第一电离能:X<W |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】工业上电解熔融 和冰晶石
和冰晶石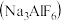 的混合物可制得铝。下列说法正确的是
的混合物可制得铝。下列说法正确的是
 和冰晶石
和冰晶石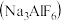 的混合物可制得铝。下列说法正确的是
的混合物可制得铝。下列说法正确的是A.半径大小: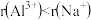 | B.电负性大小: |
C.电离能大小: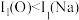 | D.碱性强弱: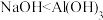 |
您最近一年使用:0次