下列几组排列顺序不正确 的项有
①沸点高低:HI>HBr>HCl>HF ②热稳定性大小:HF>H2O>NH3>PH3
③熔点高低:金刚石>食盐>金属钠>冰 ④微粒半径大小:S2->Cl->F->Na+>Al3+
⑤晶格能: NaCl<MgO ⑥溶解性:NH3<PH3
⑦热分解温度:MgCO3<BaCO3 ⑧第一电离能:Mg>Al
①沸点高低:HI>HBr>HCl>HF ②热稳定性大小:HF>H2O>NH3>PH3
③熔点高低:金刚石>食盐>金属钠>冰 ④微粒半径大小:S2->Cl->F->Na+>Al3+
⑤晶格能: NaCl<MgO ⑥溶解性:NH3<PH3
⑦热分解温度:MgCO3<BaCO3 ⑧第一电离能:Mg>Al
| A.5项 | B.2项 | C.3项 | D.4项 |
更新时间:2023-05-24 10:56:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是
| A.元素非金属性由弱到强的顺序为Z<Y<X |
| B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C.三种元素的气态氢化物中,Z的气态氢化物最稳定 |
| D.原子半径由大到小的顺序为X>Y>Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z为原子序数依次增大的短周期元素。W与Y同主族,X原子的最外层电子数为内层电子总数的3倍,Z与W的原子序数之差等于X原子序数的2倍。下列结论正确的是
| A.原子半径:W<X<Y<Z |
| B.W-比X2-还原性弱 |
| C.Z的含氧酸酸性比H2SO4强 |
| D.X、Y、Z组成的化合物中含有共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,Y是地壳中含量最多的元素,由这四种元素形成的某化合物结构如图所示。下列叙述不正确的是
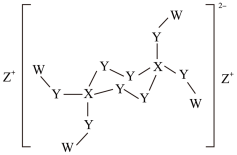

| A.简单离子半径:Y>Z |
| B.该化合物具有强氧化性,可杀菌消毒 |
C.X的最高价氧化物的水化物分子式为 |
| D.该化合物中既含有离子键,又含有极性共价键和非极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
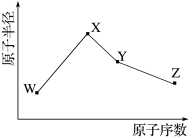
【推荐2】科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,该超分子具有高效的催化性能,其分子结构如图所示.W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大.(注:实线代表共价键,其他重复单元的W、X未标注)下列说法不正确的是


| A.Y单质的氧化性在同主族中最强 | B.离子半径: |
| C.Z与Y可组成两种离子化合物 | D.简单氢化物的热稳定性: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列各项与氢键无关的是
| A.NH3比PH3更易溶于水 |
| B.H2O的熔点比H2S高 |
| C.CaF2的熔点比CaCl2高 |
D.邻羟基苯甲醛( )沸点比对羟基苯甲醛( )沸点比对羟基苯甲醛( )低 )低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.HF、HCl、HBr、HI的稳定性逐渐减弱,而熔沸点逐渐升高 |
| B.Ba(OH)2晶体不导电,但熔化后可以导电 |
| C.干冰属于原子晶体,熔化破坏共价键和分子间作用力 |
| D.干冰升华时,分子内共价键会发生断裂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列物质性质比较,正确的是
| A.酸性:H2SO4>HClO4>H3PO4 | B.碱性:KOH>NaOH>LiOH |
| C.金属性:Al>Mg>Na | D.熔点:NaCl>NH3>H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实验的验证.以下类推的结论正确的是
| A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
| B.HCl的水溶液是强酸,推出HF的水溶液也是强酸 |
| C.CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似 |
| D.Na、K在周期表中属于同一主族,化学性质相似,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
您最近一年使用:0次

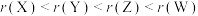

 固体的熔点为300℃;②无水
固体的熔点为300℃;②无水 晶体易升华;③熔融状态的
晶体易升华;③熔融状态的 不能导电,稀溶液具有弱的导电能力且可作为手术刀的消毒液,下列关于
不能导电,稀溶液具有弱的导电能力且可作为手术刀的消毒液,下列关于


