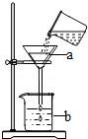
实验室中制备氯苯的装置如图所示(其中夹持仪器已略去),其原理是苯与氯气在催化剂作用下生成氯苯,同时会有少量苯发生副反应生成二氯苯。
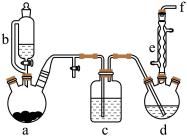
苯及其生成物沸点如表所示:
请回答下列问题:
(1)仪器a中盛有 晶体,打开仪器b中活塞,a中产生氯气。仪器b名称是
晶体,打开仪器b中活塞,a中产生氯气。仪器b名称是__________ ,仪器b中盛装的试剂是__________ 。
(2)仪器d中盛有苯、 粉末,仪器a中生成的气体经过仪器c进入仪器d中,d中主要反应的化学方程式为
粉末,仪器a中生成的气体经过仪器c进入仪器d中,d中主要反应的化学方程式为__________ ,仪器c中盛装的试剂是__________ 。
(3)仪器e的作用是__________ 。
(4)f处应接仪器名称和盛装试剂最好为下列的______ (填标号)。
A.洗气瓶,浓硫酸 B.U形管,无水 C.U形管,碱石灰
C.U形管,碱石灰
(5)实验室制得的粗氯苯,采用如下操作进行精制(部分操作可重复使用),正确的操作顺序为______ (填序号)。
①蒸馏 ②水洗、分液 ③用干燥剂干燥、过滤 ④用10% 溶液洗、分液
溶液洗、分液
(6)工业生产中使用 苯可制得
苯可制得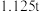 氯苯,则氯苯的产率为
氯苯,则氯苯的产率为__________ 。

苯及其生成物沸点如表所示:
有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
沸点/℃ | 80.0 | 132.2 | 180.4 | 172.0 | 173.4 |
(1)仪器a中盛有
 晶体,打开仪器b中活塞,a中产生氯气。仪器b名称是
晶体,打开仪器b中活塞,a中产生氯气。仪器b名称是(2)仪器d中盛有苯、
 粉末,仪器a中生成的气体经过仪器c进入仪器d中,d中主要反应的化学方程式为
粉末,仪器a中生成的气体经过仪器c进入仪器d中,d中主要反应的化学方程式为(3)仪器e的作用是
(4)f处应接仪器名称和盛装试剂最好为下列的
A.洗气瓶,浓硫酸 B.U形管,无水
 C.U形管,碱石灰
C.U形管,碱石灰(5)实验室制得的粗氯苯,采用如下操作进行精制(部分操作可重复使用),正确的操作顺序为
①蒸馏 ②水洗、分液 ③用干燥剂干燥、过滤 ④用10%
 溶液洗、分液
溶液洗、分液(6)工业生产中使用
 苯可制得
苯可制得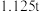 氯苯,则氯苯的产率为
氯苯,则氯苯的产率为
更新时间:2023-07-06 23:22:48
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式_______ ,B分子式______ 。
(2)与A相邻的同系物C发生加聚反应生成有机高分子材料的反应的化学反应方程式:_______ 。
(3)在碘水中加入B振荡静置后的现象_______ 。
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:_______ ,反应类型:________ 。
(5)等质量的A、B完全燃烧时消耗O2的物质的量多的是_______ (填分子名称)
(6)已知乙烯能发生以下转化:

①写出B与D反应的化学方程式_________ ;反应类型:________ 。
②写出反应②的化学方程式:________
(1)A的结构简式
(2)与A相邻的同系物C发生加聚反应生成有机高分子材料的反应的化学反应方程式:
(3)在碘水中加入B振荡静置后的现象
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:
(5)等质量的A、B完全燃烧时消耗O2的物质的量多的是
(6)已知乙烯能发生以下转化:

①写出B与D反应的化学方程式
②写出反应②的化学方程式:
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】氯苯在染料、医药工业中用于制造苯酚、硝基氯苯、苯胺硝基酚等有机中间体。实验室中制备氯苯的装置如图所示(夹持仪器已略去)。请回答下列问题:
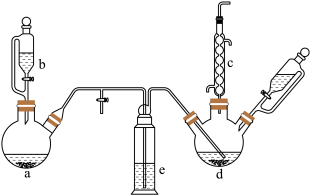
(1)仪器c的名称为:_____ 。与普通分液漏斗相比,仪器b的优点是______ 。
(2)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e是洗气瓶,瓶内盛装的试剂是______ 。
②仪器d中的反应进行过程中,保持温度在40~60℃,以减少副反应发生。仪器d的加热方式最好采用______ 加热。
(3)仪器c的作用是______ ;d中发生反应的化学方程式是______ 。
(4)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗、碱洗、再水洗,最后通过分液得到含氯苯的混合物,该混合物的成分及各成分的沸点如表所示:
①碱洗前先进行水洗的目的是______ 。
②提取该混合物中的氯苯时,采用蒸馏的方法,收集_____ ℃左右的馏分。

(1)仪器c的名称为:
(2)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e是洗气瓶,瓶内盛装的试剂是
②仪器d中的反应进行过程中,保持温度在40~60℃,以减少副反应发生。仪器d的加热方式最好采用
(3)仪器c的作用是
(4)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗、碱洗、再水洗,最后通过分液得到含氯苯的混合物,该混合物的成分及各成分的沸点如表所示:
有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
沸点/℃ | 80 | 132.2 | 180.4 | 172.0 | 173.4 |
②提取该混合物中的氯苯时,采用蒸馏的方法,收集
您最近半年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐3】已知:A的产量是衡量一个国家石油化工发展水平的重要标志。E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。G是最简单的芳香烃。
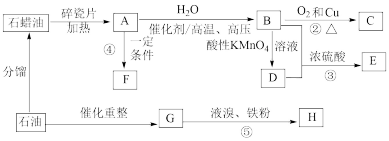
(l)C的名称为____________ 。
(2)D分子中官能团名称是_______________ 。
(3)写出一种能鉴别B和D的化学试剂____________________ 。
(4)写出下列反应的化学方程式和反应类型:
反应④___________________ ,____________________ ;
反应⑤_______________ ,________________________ 。
(5)I是E的同分异构体,能和碳酸氢钠溶液产生CO2气体。写出I所有可能的结构简式___________________________________ 。

(l)C的名称为
(2)D分子中官能团名称是
(3)写出一种能鉴别B和D的化学试剂
(4)写出下列反应的化学方程式和反应类型:
反应④
反应⑤
(5)I是E的同分异构体,能和碳酸氢钠溶液产生CO2气体。写出I所有可能的结构简式
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
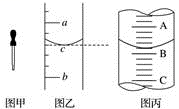
【推荐1】(1)图甲是实验室常用的一种仪器,其名称是________ ;其主要用途是________ ;
(2)小明用某规格的量筒量取一定体积的液体,液面位置如图乙,则其量得液体体积为___ 或__ (用a、b来表示)。
(3)图丙表示10 mL量筒中液面的位置,A与B、B与C刻度相差1 mL,如果刻度A为5,量筒中液体体积是________ mL。
(2)小明用某规格的量筒量取一定体积的液体,液面位置如图乙,则其量得液体体积为
(3)图丙表示10 mL量筒中液面的位置,A与B、B与C刻度相差1 mL,如果刻度A为5,量筒中液体体积是

您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】下列为实验室常用的实验装置,回答有关问题:
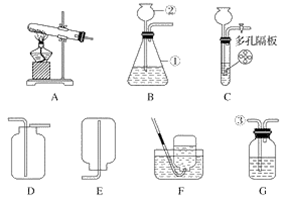
(1)写出标号仪器名称:①________ ;②__________ 。
(2)用高锰酸钾固体制氧气,应选用发生装置________ (填“A”或“B”),装入药品前应先________ ,反应的化学方程式是________________________________________ 。若用过氧化氢溶液和二氧化锰制取氧气,二氧化锰起________ 作用。
(3)用块状石灰石制取二氧化碳时,②中应加入________ ,反应的化学方程式为________________________ ,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是________________ (答出一点即可)。检验产生的气体是二氧化碳的方法是________________ 。
(4)实验室收集氢气可用________ 装置。

(1)写出标号仪器名称:①
(2)用高锰酸钾固体制氧气,应选用发生装置
(3)用块状石灰石制取二氧化碳时,②中应加入
(4)实验室收集氢气可用
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】铝土矿【主要成分为Al2O3,还含有SiO2(不溶于水和酸)、Fe2O3】是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀A、B的成分分别是__________ 、__________ ;步骤②中的试剂a是__________ ;(以上均填化学式)
(2)试写出步骤③中发生反应的离子方式__________ 、__________ ;

(1)沉淀A、B的成分分别是
(2)试写出步骤③中发生反应的离子方式
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
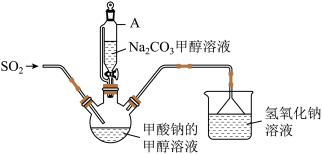
【推荐2】连二亚硫酸钠(Na2S2O4),是一种重要的化工产品,常在染料、药品的生产里作还原剂或漂白剂。已知Na2S2O4易溶于水,难溶于甲醇,易被空气氧化,遇水迅速分解,在碱性条件下较稳定,可与盐酸发生反应:2Na2S2O4+4HCl=4NaCl+S↓+3SO2↑+2H2O。实验室常用甲酸钠(HCOONa)法制备Na2S2O4,操作步骤及装置图(夹持仪器略去)如图:
I.安装好整套装置,检查装置气密性,然后再加入相应的试剂。
II.向装置中先通入一段时间N2,再向装置中通入SO2
III.控制温度60~70℃,向甲酸钠的甲醇溶液中,边搅拌边滴加Na2CO3甲醇溶液,即可生成Na2S2O4。
IV.冷却至40~50℃,过滤,洗涤干燥。回答下列问题:
(1)仪器A的名称是_____ 。
(2)步骤II中要先通入一段时间N2,目的是_____ 。
(3)上述装置中还需补充的实验仪器或装置:_____ 。
(4)制取SO2:供选择的玻璃仪器(非玻璃仪器任选)有:大试管、烧杯、圆底烧瓶、分液漏斗、导气管;化学试剂有:铜、浓硫酸、亚硫酸钠固体。请写出制取SO2的化学方程式:_____ 。
(5)步骤III中的HCOONa被氧化为CO2,生成Na2S2O4的化学方程式为:_____ 。
(6)步骤IV用甲醇对Na2S2O4进行洗涤可提高纯度,简述洗涤步骤:在无氧环境中_____ 。
(7)隔绝空气加热Na2S2O4固体,可得到产物Na2SO3和Na2S2O3。某实验小组由于没有做到完全隔绝空气,得到的产物中还含有Na2SO4。完成表中的内容,证明该分解产物中含有Na2SO4。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液、KMnO4溶液)

I.安装好整套装置,检查装置气密性,然后再加入相应的试剂。
II.向装置中先通入一段时间N2,再向装置中通入SO2
III.控制温度60~70℃,向甲酸钠的甲醇溶液中,边搅拌边滴加Na2CO3甲醇溶液,即可生成Na2S2O4。
IV.冷却至40~50℃,过滤,洗涤干燥。回答下列问题:
(1)仪器A的名称是
(2)步骤II中要先通入一段时间N2,目的是
(3)上述装置中还需补充的实验仪器或装置:
(4)制取SO2:供选择的玻璃仪器(非玻璃仪器任选)有:大试管、烧杯、圆底烧瓶、分液漏斗、导气管;化学试剂有:铜、浓硫酸、亚硫酸钠固体。请写出制取SO2的化学方程式:
(5)步骤III中的HCOONa被氧化为CO2,生成Na2S2O4的化学方程式为:
(6)步骤IV用甲醇对Na2S2O4进行洗涤可提高纯度,简述洗涤步骤:在无氧环境中
(7)隔绝空气加热Na2S2O4固体,可得到产物Na2SO3和Na2S2O3。某实验小组由于没有做到完全隔绝空气,得到的产物中还含有Na2SO4。完成表中的内容,证明该分解产物中含有Na2SO4。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液、KMnO4溶液)
| 实验步骤 | 预期的实验现象 |
| 步骤1:取少量分解产物于试管,加水溶解,加入足量稀盐酸 | 现象1:① |
| 步骤2:过滤,② | 现象2:③ |
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】现有含有少量NaCl、 Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。

(1)沉淀A的主要成分是_____________ 、______________ (填化学式)。
(2)①②③中均进行的分离操作是_______________ 。
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是__________ ,为了除去杂质,可向溶液3中加入适量的______________ 。
(4)实验探究小组在实验中需要用到456 mL1 mol•L-1的HNO3溶液,但是在实验室中只发现一瓶8 mol•L-1的HNO3溶液,该小组用8mol•L-1的HNO3溶液配制所需溶液。
①实验中所需的玻璃仪器包括________ 、_____ mL量筒、烧杯、________ 、胶头滴管等。
②该实验中需要量取8mol•L-1的HNO3溶液________ mL。
③下列实验操作中导致配制的溶液浓度偏高的是_____________ 。
A.取用8mol•L-1的HNO3溶液溶液时仰视量筒刻度线
B.量取用的量筒水洗后未进行任何操作
C.8mol•L-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
E.定容后,将容量瓶振荡摇匀后,发现液面低于刻度线,未进行任何操作

(1)沉淀A的主要成分是
(2)①②③中均进行的分离操作是
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是
(4)实验探究小组在实验中需要用到456 mL1 mol•L-1的HNO3溶液,但是在实验室中只发现一瓶8 mol•L-1的HNO3溶液,该小组用8mol•L-1的HNO3溶液配制所需溶液。
①实验中所需的玻璃仪器包括
②该实验中需要量取8mol•L-1的HNO3溶液
③下列实验操作中导致配制的溶液浓度偏高的是
A.取用8mol•L-1的HNO3溶液溶液时仰视量筒刻度线
B.量取用的量筒水洗后未进行任何操作
C.8mol•L-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
E.定容后,将容量瓶振荡摇匀后,发现液面低于刻度线,未进行任何操作
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
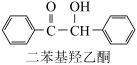
【推荐1】二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,相关物质的物理参数、化学方程式及装置图(加热和夹持装置已略去)如下:
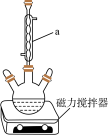
 +2FeCl3
+2FeCl3
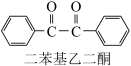 +2FeCl2+2HCl
+2FeCl2+2HCl
在反应装置中,加入10mL冰醋酸、5.50g FeCl3固体、10mL水及少量碎瓷片,加热至沸腾,停止加热,待沸腾平息后加入2.12g二苯基羟乙酮,继续加热回流至二苯基羟乙酮完全反应。反应结束后加水煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯,得到1.80g产品。
重结晶过程如下:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答以下问题:
(1)装置图中仪器a的名称是____ ,其作用是____ 。
(2)加入碎瓷片的作用是____ 。若加热后发现未加碎瓷片,应采取的正确方法是___ 。
(3)实验中可采用薄层色谱跟踪反应进程,其原理和操作与纸上层析类同,通过观察薄层色谱展开后的斑点(在实验条件下,只有二苯基羟乙酮和二苯基乙二酮能够产生斑点)判断样品中的成分。如图分别为加入二苯基羟乙酮后反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样,薄层色谱展开后的斑点:
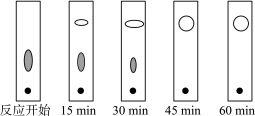
该实验条件下加热____ 后可认为反应结束。
A.15min B.30min C.45min D.60min
(4)上述重结晶过程中,____ (填步骤名称)操作除去了不溶性杂质。
(5)在重结晶过程中,不可选用明火直接加热,原因是____ 。
(6)不选择蒸馏的方法提纯二苯基乙二酮粗产品的原因是_____ 。
(7)本实验的产率是____ %。(保留3位有效数字)
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 | ||
| 二苯基羟乙酮 | 212 | 133 | 344 | 1.310 | 不溶于冷水,溶于乙醇 | |
| 二苯基乙二酮 | 210 | 97 | 348 | 1.084 | 不溶于水,能溶于乙醇 |

 +2FeCl3
+2FeCl3
 +2FeCl2+2HCl
+2FeCl2+2HCl在反应装置中,加入10mL冰醋酸、5.50g FeCl3固体、10mL水及少量碎瓷片,加热至沸腾,停止加热,待沸腾平息后加入2.12g二苯基羟乙酮,继续加热回流至二苯基羟乙酮完全反应。反应结束后加水煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯,得到1.80g产品。
重结晶过程如下:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答以下问题:
(1)装置图中仪器a的名称是
(2)加入碎瓷片的作用是
(3)实验中可采用薄层色谱跟踪反应进程,其原理和操作与纸上层析类同,通过观察薄层色谱展开后的斑点(在实验条件下,只有二苯基羟乙酮和二苯基乙二酮能够产生斑点)判断样品中的成分。如图分别为加入二苯基羟乙酮后反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样,薄层色谱展开后的斑点:

该实验条件下加热
A.15min B.30min C.45min D.60min
(4)上述重结晶过程中,
(5)在重结晶过程中,不可选用明火直接加热,原因是
(6)不选择蒸馏的方法提纯二苯基乙二酮粗产品的原因是
(7)本实验的产率是
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】溴苯是医药、染料和材料领域常用的有机合成原料。某实验小组设计如下实验来制取、提纯溴苯, 并探究该制备反应的反应类型。 (实验装置图如下)
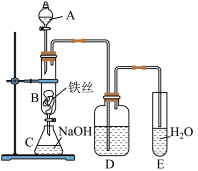
先向A中加入苯和液溴,再将混合液慢慢滴入反应器 B(B下端活塞关闭)中。实验开始后,观察到B中液体处于微沸状态。
(1)仪器A的名称是___________________ 。
(2)实验结束时,打开B下端的活塞,让反应液流入C中,充分振荡,目的是____ 。然后从C中分离出溴苯的方法是_______________________ 。
(3)D中盛装的试剂是___________________ 。
(4)向试管E中加入AgNO3溶液,产生淡黄色沉淀,则证明苯和液溴发生的反应类型是__________ ,写出B中反应的化学方程式___________________________ 。

先向A中加入苯和液溴,再将混合液慢慢滴入反应器 B(B下端活塞关闭)中。实验开始后,观察到B中液体处于微沸状态。
(1)仪器A的名称是
(2)实验结束时,打开B下端的活塞,让反应液流入C中,充分振荡,目的是
(3)D中盛装的试剂是
(4)向试管E中加入AgNO3溶液,产生淡黄色沉淀,则证明苯和液溴发生的反应类型是
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】化学是一门以实验为基础的学科,结合下列实验装置图回答相关问题。
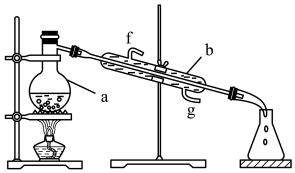
(1)写出下列仪器的名称:a.________ ;b:_________ 。
(2)实验室欲利用如图所示的装置来分离乙酸(沸点为118℃)和乙酸乙酯(沸点为77.1℃)的混合物。
①还缺少的仪器是______ ,将仪器补充完整后进行的实验操作的名称是_____ 。
②实验时,仪器b中冷却水的进口是______ .(填“f”或“g”)。
③实验时,常向仪器a中加入碎瓷片,这样做的目的是________ 。

(1)写出下列仪器的名称:a.
(2)实验室欲利用如图所示的装置来分离乙酸(沸点为118℃)和乙酸乙酯(沸点为77.1℃)的混合物。
①还缺少的仪器是
②实验时,仪器b中冷却水的进口是
③实验时,常向仪器a中加入碎瓷片,这样做的目的是
您最近半年使用:0次