已知:Al4C3与水反应生成CH4和Al(OH)3。某同学在实验室中对CH4的制备和性质进行了探究。回答下列问题:
(1)Al4C3与水反应生成CH4和Al(OH)3的化学方程式为_____________ 。
(2)甲烷的制取(如图甲所示)
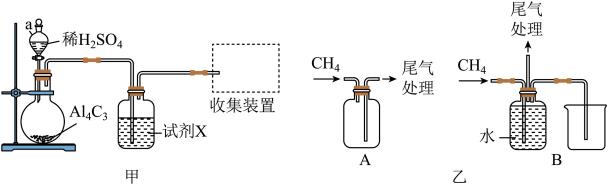
①甲中仪器a的名称为______________ ;试剂X的作用为____________ 。
②制备CH4时,用稀硫酸代替水的优点为___________ 。
③甲中收集装置适合选用乙中的_________ (填大写字母)。
(3)甲烷与氯气的反应
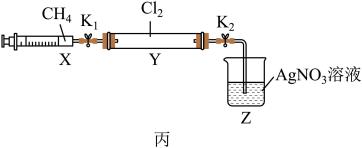
将上述收集到的CH4充入注射器X中,硬质玻璃管Y中充入Cl2(两端用止水夹K1、K2夹紧),在光照条件下按图丙装置进行实验。
(1)Al4C3与水反应生成CH4和Al(OH)3的化学方程式为
(2)甲烷的制取(如图甲所示)

①甲中仪器a的名称为
②制备CH4时,用稀硫酸代替水的优点为
③甲中收集装置适合选用乙中的
(3)甲烷与氯气的反应
将上述收集到的CH4充入注射器X中,硬质玻璃管Y中充入Cl2(两端用止水夹K1、K2夹紧),在光照条件下按图丙装置进行实验。

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,将CH注入Y中,关闭K | 无明显现象 | CH4与Cl2混合 |
| 将丙置于光亮处,使Y中气体反应 | ||
| 充分反应后,恢复至室温,打开K2 |
更新时间:2023/07/07 23:42:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下:
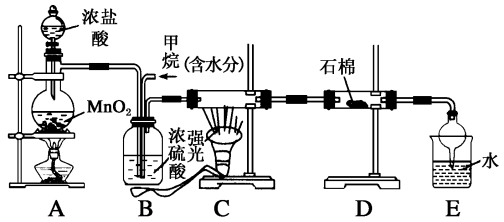
(1)B装置有三种功能:
①__________ ;②__________ ;③__________ 。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值的取值范围为__________ 。
(3)D装置的石棉中均匀混有KI粉末,其作用是_____________ 。
(4)E装置的作用是__________和________(填编号)。
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,置换出黑色小颗粒的化学方程式为__________ ,可见有机反应有很多副反应。
(6)E装置除生成盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填编号)。
(7)该装置还有缺陷,原因是没有进行尾气处理,其尾气的主要成分是__________和________(填编号)。

(1)B装置有三种功能:
①
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值的取值范围为
(3)D装置的石棉中均匀混有KI粉末,其作用是
(4)E装置的作用是__________和________(填编号)。
| A.收集气体 | B.吸收氯气 |
| C.防止倒吸 | D.吸收氯化氢 |
(6)E装置除生成盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填编号)。
| A.萃取法 | B.蒸馏法 |
| C.过滤法 | D.分液法 |
| A.CH4 | B.CH3Cl |
| C.CH2Cl2 | D.CHCl3 |
| E.CCl4 | |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:
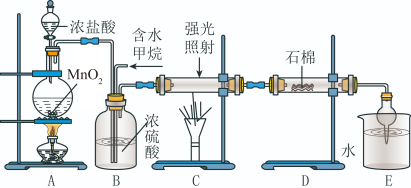
根据设计要求回答:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③___________ 。
(2)设 =x,若理论上欲获得最多的氯化氢,则x值应
=x,若理论上欲获得最多的氯化氢,则x值应___________ 。
(3)D装置的石棉中均匀混有KI粉末,其作用是___________ 。
(4)E装置的作用是___________ (填序号)。
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:___________ 。
(6)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为___________ 。该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为___________ (填序号)。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3 e.CCl4

根据设计要求回答:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③
(2)设
 =x,若理论上欲获得最多的氯化氢,则x值应
=x,若理论上欲获得最多的氯化氢,则x值应(3)D装置的石棉中均匀混有KI粉末,其作用是
(4)E装置的作用是
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:
(6)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3 e.CCl4
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.化学反应过程中伴随着能量变化。
(1)下列变化中属于吸热反应的是_______ 。
①铝片与稀盐酸的反应
②将胆矾加热变为白色粉末
③甲烷在氧气中的燃烧反应
④NH4NO3固体溶于水
⑤氯酸钾分解制氧气
⑥Ba(OH)2·8H2O与NH4Cl反应
其中⑥中发生的化学方程式为_______ 。
(2)标准状态下,下列物质气态时的相对能量如下表:
由HO(g)+HO(g)=H2O2(g)计算出H2O2中氧氧单键的键能为_______ kJ/mol,解离氧氧单键所需能量:HOO_______ H2O2(填“>”、“<”或“=”)。
Ⅱ.立方烷是一种新合成的烃,其分子结构为正方体结构,其碳架结构如图所示:

(3)立方烷的分子式为_______ ,其燃烧方程式为_______ 。
(4)光照条件下,立方烷和氯气发生_______ (填反应类型),1mol立方烷最多会生成_______ molHCl,生成的二氯代物的同分异构体有_______ 种。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应
②将胆矾加热变为白色粉末
③甲烷在氧气中的燃烧反应
④NH4NO3固体溶于水
⑤氯酸钾分解制氧气
⑥Ba(OH)2·8H2O与NH4Cl反应
其中⑥中发生的化学方程式为
(2)标准状态下,下列物质气态时的相对能量如下表:
| 物质(g) | O | H | HO | HOO | H2 | O2 | H2O2 | H2O |
| 能量/kJ/mol | 249 | 218 | 39 | 10 | 0 | 0 | -136 | -242 |
Ⅱ.立方烷是一种新合成的烃,其分子结构为正方体结构,其碳架结构如图所示:

(3)立方烷的分子式为
(4)光照条件下,立方烷和氯气发生
您最近一年使用:0次
【推荐1】某化学兴趣小组为了制取并探究氨气性质,按下列装置 部分夹持装置已略去
部分夹持装置已略去 进行实验。(制取氨气的反应原理:
进行实验。(制取氨气的反应原理: )
)
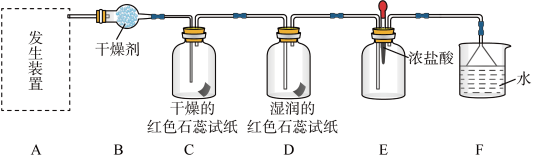
【实验探究】
(1)A装置N元素的化合价是_______ 该反应是否是氧化还原反应:_______ 。
(2)用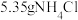 固体与足量
固体与足量 反应,最多可制得标准状况下氨气的体积为
反应,最多可制得标准状况下氨气的体积为__________ L。 的摩尔质量为
的摩尔质量为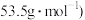
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:___________________ .
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入 滴浓盐酸,可观察到的现象是
滴浓盐酸,可观察到的现象是___________________ .
(5)如果氨气泄漏,你应采取的急救措施是:___________________ .
(6)检验氨气是否收集满的方法是__________________________________ 
【拓展应用】
(7)某同学用下图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有_______ 性质 填序号
填序号 。
。

 还原性
还原性  极易溶于水
极易溶于水  与水反应生成碱性物质
与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: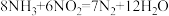 该反应中氨气体现
该反应中氨气体现_______  填“氧化性”或“还原性”
填“氧化性”或“还原性” 。
。
(9)请你列举出氨气的一种用途_________________________ 。
 部分夹持装置已略去
部分夹持装置已略去 进行实验。(制取氨气的反应原理:
进行实验。(制取氨气的反应原理: )
) 
【实验探究】
(1)A装置N元素的化合价是
(2)用
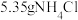 固体与足量
固体与足量 反应,最多可制得标准状况下氨气的体积为
反应,最多可制得标准状况下氨气的体积为 的摩尔质量为
的摩尔质量为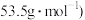
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是:
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入
 滴浓盐酸,可观察到的现象是
滴浓盐酸,可观察到的现象是(5)如果氨气泄漏,你应采取的急救措施是:
(6)检验氨气是否收集满的方法是

【拓展应用】
(7)某同学用下图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有
 填序号
填序号 。
。
 还原性
还原性  极易溶于水
极易溶于水  与水反应生成碱性物质
与水反应生成碱性物质 (8)氨气的用途很广。如可用氨气处理二氧化氮:
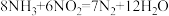 该反应中氨气体现
该反应中氨气体现 填“氧化性”或“还原性”
填“氧化性”或“还原性” 。
。(9)请你列举出氨气的一种用途
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】无水氯化锌是有机合成中重要催化剂,无水氯化锌为白色粉末,易潮解,沸点为732°C。久置市售氯化锌常含Zn(OH)Cl,影响催化效果。实验室用HCl气体“置换”除水、升华氯化锌相结合的方法提纯市售氯化锌,其装置如下图所示:

(1)装置A中盛浓硫酸的仪器名称是__________ ,装置B中试剂是__________ .
(2)实验开始时,通入HCl和N2,将管式炉I、Ⅱ升温至150°C,装置C中发生的化学反应方程式为__________ ;此时通入N2的目的是__________ 。
(3)反应一段时间后保持管式炉I、Ⅱ温度为350°℃,保证将水除尽,撤去管式炉__________ (填“I”或“II”),升温余下的管式炉至750C,该操作的目的是__________ ;最后在氮气保护下将氯化锌刮出玻璃管外,保存待用。
(4)若称取12.6g市售氯化锌样品,经提纯最终得到高纯氯化锌12.9g,则样品中氯化锌纯度为__________ 。
(5)为保证无水氯化锌的纯度,对上述装置进行改进,措施是__________ 。

(1)装置A中盛浓硫酸的仪器名称是
(2)实验开始时,通入HCl和N2,将管式炉I、Ⅱ升温至150°C,装置C中发生的化学反应方程式为
(3)反应一段时间后保持管式炉I、Ⅱ温度为350°℃,保证将水除尽,撤去管式炉
(4)若称取12.6g市售氯化锌样品,经提纯最终得到高纯氯化锌12.9g,则样品中氯化锌纯度为
(5)为保证无水氯化锌的纯度,对上述装置进行改进,措施是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】二氧化铈(CeO2) 常用于玻璃添加剂,还可用在化妆品中起到抗紫外线作用。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
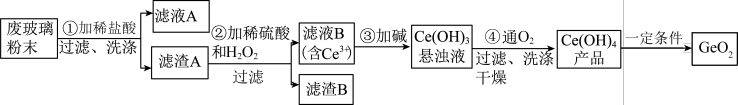
(1)步骤①过滤过程中使用的玻璃仪器主要有___________ ,滤渣A 的主要成分为___________ 。
(2)第②步反应中,氧化剂与还原剂的物质的量之比为___________ 。
(3)第④步反应的化学方程式为_________ ,该步骤中洗涤滤渣的方法是________ 。
(4)工业上以CeCl3·7H2O为原料制备无水CeCl3,流程如下:

制备过程中,如直接加热CeCl3·7H2O会发生反应生成CeOC1,该反应的化学方程式为________ ,加NH4Cl能够减少CeOCl的生成,其原因为___________ (用化学方程式表示)。

(1)步骤①过滤过程中使用的玻璃仪器主要有
(2)第②步反应中,氧化剂与还原剂的物质的量之比为
(3)第④步反应的化学方程式为
(4)工业上以CeCl3·7H2O为原料制备无水CeCl3,流程如下:

制备过程中,如直接加热CeCl3·7H2O会发生反应生成CeOC1,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】过氧化钠保存不当在空气中容易变质。
(1)某过氧化钠样品已经部分变质,只限用一种溶液,请你设计一种简便的化学方法,证明过氧化钠已经变质。____________________________________________
(2)若用最简单的实验来检验样品中还有过氧化钠,除试管、胶头滴管等外还需用的实验用品有:____________________________________________
(3)某课外活动小组为了测定样品,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。(假设C中Na2O2完全反应)。实验过程记录如下: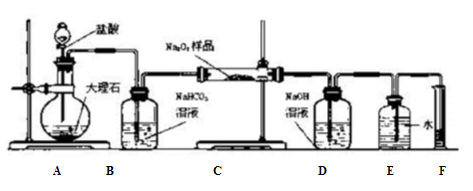
a.检查装置气密性;b.往玻璃管中放入a g样品,其它仪器中均加入足量的相应试剂,从分液漏斗往烧瓶中加入过量盐酸,立即发生剧烈反应,将广口瓶中的水排入量筒中;c实验结束后,测量量筒中收集到的水的体积,进行计算。
①写出装置A和B中发生反应的离子方程式:
装置A:__________________________________ ;
装置B:____________________________________ 。
②他们在读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为______________________ 。
(1)某过氧化钠样品已经部分变质,只限用一种溶液,请你设计一种简便的化学方法,证明过氧化钠已经变质。
(2)若用最简单的实验来检验样品中还有过氧化钠,除试管、胶头滴管等外还需用的实验用品有:
(3)某课外活动小组为了测定样品,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。(假设C中Na2O2完全反应)。实验过程记录如下:

a.检查装置气密性;b.往玻璃管中放入a g样品,其它仪器中均加入足量的相应试剂,从分液漏斗往烧瓶中加入过量盐酸,立即发生剧烈反应,将广口瓶中的水排入量筒中;c实验结束后,测量量筒中收集到的水的体积,进行计算。
①写出装置A和B中发生反应的离子方程式:
装置A:
装置B:
②他们在读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.课堂上,老师提问如何鉴别浓硫酸与稀硫酸,某学习小组设计方案如下
(1)以上方案中,可行的是______________ (填序号)
(2)其中一个稍作改进就能成为可行方案是________________ ,改进方法为____________ 。
(3)完全错误的是__________ ,因为_________________________________________ 。
Ⅱ.实验室用浓硫酸配制1.0mol/L硫酸溶液480mL,回答下列问题:
(1)如下图所示的仪器中配制溶液肯定不需要的是____________ (填字母),配制上述溶液还需要用到的玻璃仪器是_________________________ (填仪器名称)。
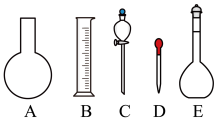
(2)容量瓶上标有以下5项中的_____________ (填序号)
①压强 ②温度 ③容量 ④浓度 ⑤刻度线
(3)在配制过程中,下列操作使所配溶液浓度偏大的是______________ (填序号)。
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
③定容时,仰视刻度线
④使用容量瓶前用蒸馏水洗涤且没干燥
(4)计算实验室配制上述溶液需用量筒取质量分数为98%、密度为1.84g/mL的浓硫酸的体积为_____________________ mL。(保留小数点后一位)
| 方案 | 结论 | |
| ① | 往酸中投入火柴梗 | 变黑者为浓硫酸 |
| ② | 加入铝片 | 产生刺激性气味者为浓硫酸 |
| ② | 加少量酸于盛水的小烧杯中 | 放热者为浓硫酸 |
| ④ | 用玻璃棒蘸浓氨水靠近酸的瓶口 | 冒白烟者为浓硫酸 |
| ⑤ | 将酸滴加到胆矾晶体上 | 变白者为浓硫酸 |
(2)其中一个稍作改进就能成为可行方案是
(3)完全错误的是
Ⅱ.实验室用浓硫酸配制1.0mol/L硫酸溶液480mL,回答下列问题:
(1)如下图所示的仪器中配制溶液肯定不需要的是

(2)容量瓶上标有以下5项中的
①压强 ②温度 ③容量 ④浓度 ⑤刻度线
(3)在配制过程中,下列操作使所配溶液浓度偏大的是
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
③定容时,仰视刻度线
④使用容量瓶前用蒸馏水洗涤且没干燥
(4)计算实验室配制上述溶液需用量筒取质量分数为98%、密度为1.84g/mL的浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学利用下图装置制备并收集干燥纯净的 ,并探究
,并探究 与碱的反应。回答下列问题:
与碱的反应。回答下列问题:
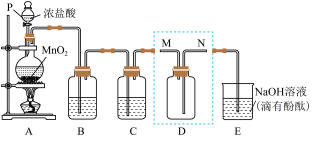
(1)装置A中发生反应的化学方程式为___________ 。
(2)实验室用下列两种方法制氯气:①用含HCl 146g的浓盐酸与足量的 反应;②用
反应;②用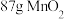 与足量浓盐酸反应。所得的氯气质量①
与足量浓盐酸反应。所得的氯气质量①___________ ②(填“>”“<”“=”)。
(3)装置B的作用是___________ 。
(4)装置D用来收集纯净且干燥的氯气,进气口为___________ (填“M”或“N”)。
(5)36.5%的浓盐酸(密度为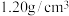 )的物质的量浓度
)的物质的量浓度___________
(6)探究 的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
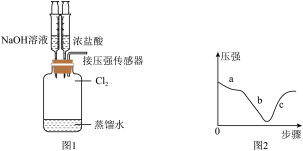
实验步骤如下:
a.向D中加入适量的蒸馏水,振荡。
b.用注射器向装置中加入NaOH溶液。
c.用注射器向装置中加入浓盐酸。
①步骤a,压强减小的原因___________ 。
②步骤b, 与NaOH溶液反应而导致压强减小
与NaOH溶液反应而导致压强减小
③步骤c,装置D中的现象___________ 。
(7)小组同学观察到E中红色褪去,并对褪色原因提出假设:
假设1:___________ ;
假设2:ClO-破坏了酚酞的结构。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许D中褪色后的溶液放入试管中,___________ (填“操作”),若___________ (填“现象”)。则假设1成立。
(8)二氧化氯( )现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。
)现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。 对酸性污水中的
对酸性污水中的 也有明显的去除效果。配平以下方程式
也有明显的去除效果。配平以下方程式________
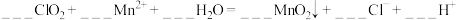
 ,并探究
,并探究 与碱的反应。回答下列问题:
与碱的反应。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)实验室用下列两种方法制氯气:①用含HCl 146g的浓盐酸与足量的
 反应;②用
反应;②用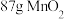 与足量浓盐酸反应。所得的氯气质量①
与足量浓盐酸反应。所得的氯气质量①(3)装置B的作用是
(4)装置D用来收集纯净且干燥的氯气,进气口为
(5)36.5%的浓盐酸(密度为
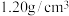 )的物质的量浓度
)的物质的量浓度(6)探究
 的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
实验步骤如下:
a.向D中加入适量的蒸馏水,振荡。
b.用注射器向装置中加入NaOH溶液。
c.用注射器向装置中加入浓盐酸。
①步骤a,压强减小的原因
②步骤b,
 与NaOH溶液反应而导致压强减小
与NaOH溶液反应而导致压强减小③步骤c,装置D中的现象
(7)小组同学观察到E中红色褪去,并对褪色原因提出假设:
假设1:
假设2:ClO-破坏了酚酞的结构。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许D中褪色后的溶液放入试管中,
(8)二氧化氯(
 )现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。
)现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。 对酸性污水中的
对酸性污水中的 也有明显的去除效果。配平以下方程式
也有明显的去除效果。配平以下方程式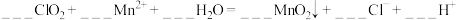
您最近一年使用:0次



