某无色透明溶液W中可能大量含表格所示中几种离子。
为了确认W的组成,进行如下实验:
①测定W溶液pH,溶液呈强酸性;
②取少量W溶液于试管,滴加 溶液,产生白色沉淀,过滤,得滤液X;
溶液,产生白色沉淀,过滤,得滤液X;
③在滤液X中滴加 溶液,又产生白色沉淀。
溶液,又产生白色沉淀。
已知:白色 微溶于水,不溶于稀硝酸。
微溶于水,不溶于稀硝酸。
请回答下列问题:
(1)不做实验可以确认W中一定不存在的离子是___________ (填离子符号,下同)。
(2)实验步骤①能确认一定不能大量存在的离子是___________ 和 ,理由是
,理由是___________ 、 )(用离子方程式表示)。
)(用离子方程式表示)。
(3)实验步骤②能确认W中一定存在的离子是___________ ,一定不存在的离子是___________ 。
(4)实验步骤③不能确认W含 ,理由是
,理由是___________ 。补充实验确认W是否含有 :
:___________ 。
(5)根据上述实验,能确认W一定含的溶质是___________ (填化学式),它属于___________ (填字母)。
A.酸 B.盐 C.碱 D.电解质
| 阳离子 |  、 、 、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 、 、 |
①测定W溶液pH,溶液呈强酸性;
②取少量W溶液于试管,滴加
 溶液,产生白色沉淀,过滤,得滤液X;
溶液,产生白色沉淀,过滤,得滤液X;③在滤液X中滴加
 溶液,又产生白色沉淀。
溶液,又产生白色沉淀。已知:白色
 微溶于水,不溶于稀硝酸。
微溶于水,不溶于稀硝酸。请回答下列问题:
(1)不做实验可以确认W中一定不存在的离子是
(2)实验步骤①能确认一定不能大量存在的离子是
 ,理由是
,理由是 )(用离子方程式表示)。
)(用离子方程式表示)。(3)实验步骤②能确认W中一定存在的离子是
(4)实验步骤③不能确认W含
 ,理由是
,理由是 :
:(5)根据上述实验,能确认W一定含的溶质是
A.酸 B.盐 C.碱 D.电解质
更新时间:2023-07-13 20:04:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】有一瓶澄清的溶液,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等离子。取该溶液进行以下实验:
等离子。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量 和数滴新制氯水,振荡,
和数滴新制氯水,振荡, 层呈紫红色;
层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;
b.溶液逐渐产生沉淀;
c.沉淀完全溶解;
④取适量③得到的碱性溶液,加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除_______ 的存在。
(2)由②可以证明_______ 的存在;同时排除_______ 的存在。
(3)由③可以证明_______ 的存在;写出c所涉及的离子反应方程式:_______ 。
(4)由④可以排除_______ 的存在,同时证明_______ 的存在。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等离子。取该溶液进行以下实验:
等离子。取该溶液进行以下实验:①用pH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量
 和数滴新制氯水,振荡,
和数滴新制氯水,振荡, 层呈紫红色;
层呈紫红色;③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性;
b.溶液逐渐产生沉淀;
c.沉淀完全溶解;
④取适量③得到的碱性溶液,加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。根据上述实验现象,回答下列问题。
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以排除
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某强酸性溶液X含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验内容如下。
中的一种或几种,取该溶液进行连续实验,实验内容如下。
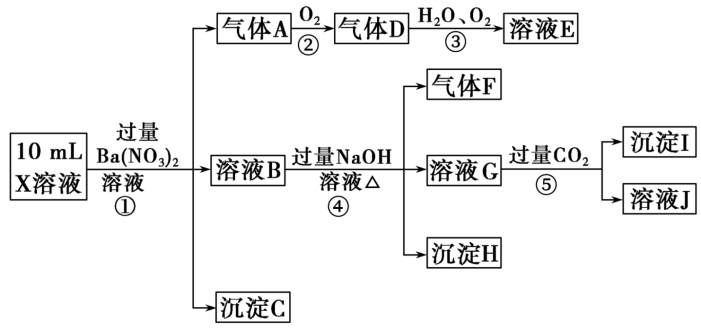
根据以上信息,回答下列问题:
(1)反应③的化学方程式为_____ 。
(2)沉淀C、H和气体F的化学式分别为______ 。
(3)写出①中生成A的离子方程式:_____ 。
(4)上述离子中,溶液X中肯定不含有的离子是_____ ,可能含有的离子是_____ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验内容如下。
中的一种或几种,取该溶液进行连续实验,实验内容如下。
根据以上信息,回答下列问题:
(1)反应③的化学方程式为
(2)沉淀C、H和气体F的化学式分别为
(3)写出①中生成A的离子方程式:
(4)上述离子中,溶液X中肯定不含有的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某无色溶液,其中可能存在如下离子:Na+.Ag+.Ba2+.Al3+.AlO2―.S2―.CO32―.SO32―.SO42―,现取该溶液进行有关实验,结果与下图所示。

试回答下列问题:
(1)生成沉淀甲的离子方程式为_____________________ 。
(2)由溶液甲生成沉淀乙的离子方程式___________________ 。
(3)沉淀丙是_____ 。如何用一化学实验来确定其成分___________________ 。
(4)气体甲的成分有哪几种可能_________________________________ 。
(5)综合上述信息,可以肯定存在的离子有_______ ,一定不存在的离子是__________ ,可能存在的离子是_________ 。

试回答下列问题:
(1)生成沉淀甲的离子方程式为
(2)由溶液甲生成沉淀乙的离子方程式
(3)沉淀丙是
(4)气体甲的成分有哪几种可能
(5)综合上述信息,可以肯定存在的离子有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z三种可溶性盐,其阳离子分别是Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl−、SO 、NO
、NO 中的某一种。现进行以下实验:
中的某一种。现进行以下实验:
①将三种盐各取少量,分别溶于盛有5 mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2 mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
回答下列问题:
(1)根据上述事实,推断这三种盐的化学式:X___________ ,Y___________ ,Z___________ 。
(2)若上述三种阳离子Ba2+、Cu2+、Ag+对应的盐都为硝酸盐,将其混合配成溶液,选择合适试剂,将这三种离子逐一沉淀分离。其流程图如下图所示:

①沉淀1的化学式为___________ 。
②若C为Na2S,且它与B的阳离子相同,则试剂B的名称是___________ 。
 、NO
、NO 中的某一种。现进行以下实验:
中的某一种。现进行以下实验:①将三种盐各取少量,分别溶于盛有5 mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2 mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
回答下列问题:
(1)根据上述事实,推断这三种盐的化学式:X
(2)若上述三种阳离子Ba2+、Cu2+、Ag+对应的盐都为硝酸盐,将其混合配成溶液,选择合适试剂,将这三种离子逐一沉淀分离。其流程图如下图所示:
| 部分物质的溶解性表 | |||
| 阴离子 | 阳离子 | ||
| Ba2+ | Cu2+ | Ag+ | |
| Cl- | 溶 | 溶 | 不 |
CO | 不 | 不 | 不 |
SO | 不 | 溶 | 微 |
| S2- | 溶 | 不 | 不 |

①沉淀1的化学式为
②若C为Na2S,且它与B的阳离子相同,则试剂B的名称是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有一包白色粉末,可能含有① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 中的一种或几种。
中的一种或几种。
实验步骤如下:
ⅰ.取少量固体投入水中,既有气体生成,又有沉淀产生。
ⅱ.过滤,取少量滤液加 溶液,无沉淀产生。
溶液,无沉淀产生。
ⅲ.另取少量滤液,加入足量 溶液,也无沉淀产生。
溶液,也无沉淀产生。
(1)推断白色粉末中一定有___________ (填序号),一定没有___________ (填序号)。
(2)请写出实验步骤ⅰ中产生气体的离子方程式:___________ 。
(3)请写出实验步骤ⅰ中产生沉淀的离子方程式:___________ 。
(4)写出③在水溶液中的电离方程式:___________ 。
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 中的一种或几种。
中的一种或几种。实验步骤如下:
ⅰ.取少量固体投入水中,既有气体生成,又有沉淀产生。
ⅱ.过滤,取少量滤液加
 溶液,无沉淀产生。
溶液,无沉淀产生。ⅲ.另取少量滤液,加入足量
 溶液,也无沉淀产生。
溶液,也无沉淀产生。(1)推断白色粉末中一定有
(2)请写出实验步骤ⅰ中产生气体的离子方程式:
(3)请写出实验步骤ⅰ中产生沉淀的离子方程式:
(4)写出③在水溶液中的电离方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水。
分别取它们的水溶液进行实验,结果如下:
① A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3沉淀部分溶解,剩余白色固体;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将76.8 g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6 mol·L-1 H2SO4,Cu片逐渐溶解,管口附近有红棕色气体出现。
(1)据此推断A、B、C的化学式:A________ ;B________ ;C________ 。
(2)E溶液显_____ 性,用离子方程式表示:_____________________________
(3)写出步骤②中发生反应的离子方程式:_______________________________________________________________ 。
(4)写出步骤⑤中发生反应的离子方程式:____________________________________________________________ 。
若要将Cu片完全溶解,至少加入稀H2SO4的体积是________ mL。
| 阳离子 | Na+ | Al3+ | Fe3+ | Cu2+ | Ba2+ |
| 阴离子 | OH- | Cl- | CO32- | NO3- | SO42- |
① A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3沉淀部分溶解,剩余白色固体;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将76.8 g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6 mol·L-1 H2SO4,Cu片逐渐溶解,管口附近有红棕色气体出现。
(1)据此推断A、B、C的化学式:A
(2)E溶液显
(3)写出步骤②中发生反应的离子方程式:
(4)写出步骤⑤中发生反应的离子方程式:
若要将Cu片完全溶解,至少加入稀H2SO4的体积是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓) CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。
①请用“双线桥”法标明该反应电子转移的方向和数目___________ 。
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为___________ L。
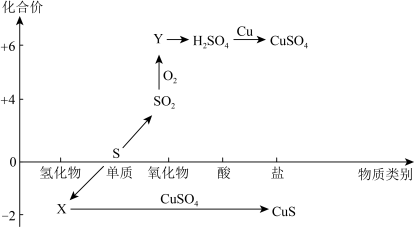
(2)检验
 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓)
 CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某工厂排放的废液中含有大量的K+,Cl-,Br-,还有少量的Ca2+,Mg2+,SO42-。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程图(提示:图中a是使Br-变为Br2的反应过程)。

已知加入试剂a后废液中发生的反应的化学方程式是Cl2 +2Br = 2KCl+Br2。试剂b须从以下试剂中选择:(1)饱和Na2CO3溶液、(2)饱和K2CO3溶液、(3)KOH溶液、(4)BaCl2溶液、(5)Ba(NO3)2溶液、(6)稀盐酸。请根据以上流程,回答下列问题:
(1)操作①、②、③、④、⑤的名称依次是________ (填字母)
A.萃取、过滤、分液、过滤、蒸发结晶
B.萃取、分液、蒸馏、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶
D.萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+,Mg2+,SO42-,选出试剂b(用序号填写,写出试剂名称不得分)所代表的试剂,按滴加顺序依次是_____
(3)调至pH=7发生反应的化学方程式为_____ 。
(4)检测SO42-已沉淀完全的实验方法为_____ 。
(5)以下关于萃取分液操作的叙述中,不正确的是_____ 。

A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,如图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体

已知加入试剂a后废液中发生的反应的化学方程式是Cl2 +2Br = 2KCl+Br2。试剂b须从以下试剂中选择:(1)饱和Na2CO3溶液、(2)饱和K2CO3溶液、(3)KOH溶液、(4)BaCl2溶液、(5)Ba(NO3)2溶液、(6)稀盐酸。请根据以上流程,回答下列问题:
(1)操作①、②、③、④、⑤的名称依次是
A.萃取、过滤、分液、过滤、蒸发结晶
B.萃取、分液、蒸馏、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶
D.萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+,Mg2+,SO42-,选出试剂b(用序号填写,写出试剂名称不得分)所代表的试剂,按滴加顺序依次是
(3)调至pH=7发生反应的化学方程式为
(4)检测SO42-已沉淀完全的实验方法为
(5)以下关于萃取分液操作的叙述中,不正确的是

A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,如图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某工厂的工业废水中含有大量的Fe2+、SO42-和较多的Cu2+及少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,在方框和 括号内填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实 验方案。

(1)操作②的名称为__________ ,所需要的玻璃仪器为__________ 、玻璃棒、烧杯。
(2)试剂⑤的化学式为__________ ,发生化学反应的离子方程式为__________ 。
(3)为验证溶液⑧中含有SO42-:取少量的溶液⑧于试管中,先加入____ 再加入__________ ,若观察到有白色沉淀,则说明溶液⑧中含有SO42-。写出上述反应的离子方程式______________________________ .

(1)操作②的名称为
(2)试剂⑤的化学式为
(3)为验证溶液⑧中含有SO42-:取少量的溶液⑧于试管中,先加入
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有四种阳离子Na+、Ba2+、Mg2+、H+和四种阴离子OH-、Cl-、 、
、 可分别组成A、B、C、D四种易溶于水易电离的物质(离子均不重复)。
可分别组成A、B、C、D四种易溶于水易电离的物质(离子均不重复)。
已知:①A溶液能使紫色石蕊试液变红,且加入盐酸无现象,继续加入氯化钡,有白色沉淀生成
②B溶液分别与A、C、D溶液混合,均有白色沉淀生成;
③C溶液能与A溶液反应产生无色无味气体。
请填空:
(1)写出下列物质的化学式:B___________ C___________ 。
(2)写出下列反应的离子方程式:
①A溶液与C溶液反应的离子方程式:___________ 。
②B溶液与D溶液反应的离子方程式:___________ 。
(3)向C的溶液中加入足量的NaOH溶液,发生反应的离子方程式为___________ 。
 、
、 可分别组成A、B、C、D四种易溶于水易电离的物质(离子均不重复)。
可分别组成A、B、C、D四种易溶于水易电离的物质(离子均不重复)。已知:①A溶液能使紫色石蕊试液变红,且加入盐酸无现象,继续加入氯化钡,有白色沉淀生成
②B溶液分别与A、C、D溶液混合,均有白色沉淀生成;
③C溶液能与A溶液反应产生无色无味气体。
请填空:
(1)写出下列物质的化学式:B
(2)写出下列反应的离子方程式:
①A溶液与C溶液反应的离子方程式:
②B溶液与D溶液反应的离子方程式:
(3)向C的溶液中加入足量的NaOH溶液,发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液中只可能大量含有 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,对其进行如下实验:
中的若干种,对其进行如下实验:
i:取少量该溶液于试管中,加入过量 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;
ii:向 中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
 :向
:向 中所得滤液中加入足量硝酸酸化后,再加入
中所得滤液中加入足量硝酸酸化后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为______ 。
(2)实验i中过滤时用到的玻璃仪器为烧杯、______ 。
(3)实验 中发生反应的离子方程式为
中发生反应的离子方程式为______ 。
(4)实验
______ (填“能”或“不能”)说明该溶液中存在 ;若能请说明理由,若不能请简单设计实验证明该溶液中是否存在
;若能请说明理由,若不能请简单设计实验证明该溶液中是否存在 :
:______ 。
(5)上述实验______ (填“能”或“不能”)说明该溶液中存在 ,若能请说明理由,若不能请简单设计实验证明该溶液中是否存在
,若能请说明理由,若不能请简单设计实验证明该溶液中是否存在 :
:______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,对其进行如下实验:
中的若干种,对其进行如下实验:i:取少量该溶液于试管中,加入过量
 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;ii:向
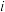 中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成; :向
:向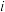 中所得滤液中加入足量硝酸酸化后,再加入
中所得滤液中加入足量硝酸酸化后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为
(2)实验i中过滤时用到的玻璃仪器为烧杯、
(3)实验
 中发生反应的离子方程式为
中发生反应的离子方程式为(4)实验

 ;若能请说明理由,若不能请简单设计实验证明该溶液中是否存在
;若能请说明理由,若不能请简单设计实验证明该溶液中是否存在 :
:(5)上述实验
 ,若能请说明理由,若不能请简单设计实验证明该溶液中是否存在
,若能请说明理由,若不能请简单设计实验证明该溶液中是否存在 :
:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】天然气中常混有 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:
①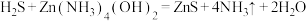
②
③
(1)反应①中, 体现
体现_______ (选填“酸性”“氧化性”或“还原性”)。
采用以下方法测定 的含量。
的含量。
步骤I:将1L天然气中的 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
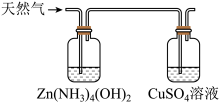
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。
(2)①滴定达到终点的现象为:溶液由_______ 色变_______ 色,且半分钟不恢复原色。
②根据条件计算天然气中H2S的含量为_______ mg·L-1。
③若在步骤I收集H2S的过程中,有少量硫化氢进入 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量_______ (选填“偏高”“偏低”或“无影响”)。
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-_______ 。
(4)利用硫碘循环处理H2S的方法如图所示:
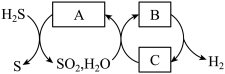
写出上述流程中A、B、C的化学式。
A:_______ ;B:_______ ;C:_______ 。
 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:①
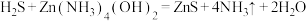
②

③

(1)反应①中,
 体现
体现采用以下方法测定
 的含量。
的含量。步骤I:将1L天然气中的
 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的
 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。(2)①滴定达到终点的现象为:溶液由
②根据条件计算天然气中H2S的含量为
③若在步骤I收集H2S的过程中,有少量硫化氢进入
 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-
(4)利用硫碘循环处理H2S的方法如图所示:

写出上述流程中A、B、C的化学式。
A:
您最近一年使用:0次



