环己酮是一种重要的化工原料,将双氧水和环己醇反应后的溶液加水蒸馏得产品与水的共沸馏出液,向其中加入食盐,搅拌分液,将有机层干燥后进行压力为20mmHg的减压蒸馏得到较纯净的环己酮。
相关数据如下:
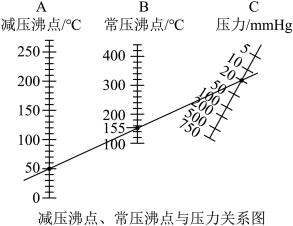
下列说法错误的是
相关数据如下:
| 物质 | 常压沸点/℃ | 密度/g/cm3 | 部分性质 |
| 环己醇 | 161.0 | 0.968 | 能溶于水,具有还原性,易被氧化 |
| 环己酮 | 155.0 | 0.947 | 微溶于水,遇氧化剂易发生开环反应 |

下列说法错误的是
| A.加入食盐的目的是降低环己酮在水中的溶解度,便于液体分离 |
| B.为提高环己酮产率,应加入过量的双氧水 |
| C.减压蒸馏时,加热方式最好选用水浴加热 |
| D.分液时先将下层液体从下口放出,再将上层液体从上口倒出 |
更新时间:2023-07-14 09:06:14
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】在恒容容器中,用 和
和 合成甲醇:
合成甲醇: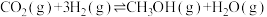 。相同时间内不同温度下,将
。相同时间内不同温度下,将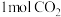 和
和 在反应器中反应,测定
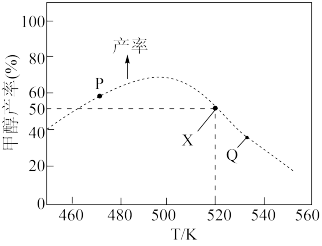
在反应器中反应,测定 的产率[产率=(实际产量/理论产量)×100%]与温度的关系如图所示。下列说法正确的是
的产率[产率=(实际产量/理论产量)×100%]与温度的关系如图所示。下列说法正确的是
 和
和 合成甲醇:
合成甲醇: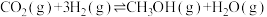 。相同时间内不同温度下,将
。相同时间内不同温度下,将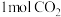 和
和 在反应器中反应,测定
在反应器中反应,测定 的产率[产率=(实际产量/理论产量)×100%]与温度的关系如图所示。下列说法正确的是
的产率[产率=(实际产量/理论产量)×100%]与温度的关系如图所示。下列说法正确的是
A.图中X点速率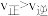 |
| B.该反应是吸热反应 |
C.图中P点所示条件下,延长反应时间能提高 的产率 的产率 |
D.X点所对应甲醇的产率50%,则可以计算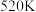 时的平衡常数 时的平衡常数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
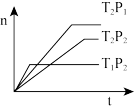
【推荐2】反应2X(g)+Y(g) 2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
 2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
| A.T1<T2,P1<P2 |
| B.T1<T2,P1>P2 |
| C.T1>T2,P1>P2 |
| D.T1>T2,P1<P2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】某工厂废液中含有少量硫酸,拟选用下列物质中和后再排放:如果要求花最少的钱来中和相同量的废硫酸,则应选择
| 物质 | CaCO3 | Ca(OH)2 | NH3 | NaOH |
| 市场参考价(元/kg) | 1.8 | 2.0 | 6.5 | 11.5 |
| A.CaCO3 | B.Ca(OH)2 | C.NH3 | D.NaOH |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】工业上常用的一种提溴技术叫做“吹出法”,过程如下,有关说法不正确 的是
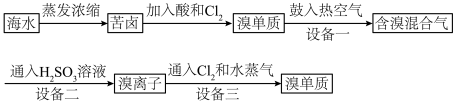
A.酸化的主要目的是防止 将 将 氧化成 氧化成 |
| B.鼓入热空气吹出溴是利用了溴的低沸点 |
| C.将含溴混合气从底部通入设备二(吸收塔)中 |
| D.设备三中的蒸汽冷凝后得到液溴和溴水的混合物,可用分液法分离 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.NaHCO3受热易分解,因此可用于胃酸中和剂 |
| B.蒸馏、分馏、萃取、过滤都属于物理变化 |
| C.纳米材料粒子直径一般在1~100nm之间,因此纳米材料属于胶体 |
| D.HClO是弱酸,所以NaClO属于弱电解质 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】除去下列物质中的杂质,所用试剂和方法正确的是
| 选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
| A | 铁粉 | 铝粉 | 盐酸、过滤 |
| B | KNO3溶液 | K2SO4溶液 | BaCl2溶液、过滤 |
| C | Cl2气体 | HCl气体 | NaOH溶液、洗气 |
| D | KBr溶液 | Br2 | 苯、萃取分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列制取物质的实验可能成功的是
| A.把苯甲酸、甲醇、稀硫酸混合置于有回流设备的装置中,加热,合成苯甲酸甲酯 |
| B.把苯和少量溴水及少量铁屑放在用带导管的瓶塞塞紧瓶口的烧瓶里,反应制取溴苯 |
| C.把醋酸钠晶体(CH3COONa•3H2O)与干燥的碱石灰按一定比例混合后,加热,制取甲烷 |
| D.把浓硝酸、浓硫酸、苯的混合液放在60℃的水浴中反应,制取硝基苯 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】中学化学实验可用如图所示的装置制取乙酸乙酯,下列说法正确的是
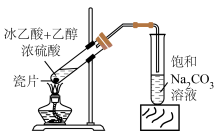

| A.反应混合液的加入顺序依次为浓硫酸、乙醇、冰乙酸 |
| B.浓硫酸不仅可以加快该反应的速率,还能提高该反应的产率 |
| C.右侧长导管起到了冷凝回流的作用,应深入液面下 |
| D.饱和碳酸钠溶液可用氢氧化钠溶液代替 |
您最近一年使用:0次

 反应变化过程中物质的浓度与反应的时间变化关系。图中t2→t3秒间的曲线变化是由于下列哪种条件的改变所引起的
反应变化过程中物质的浓度与反应的时间变化关系。图中t2→t3秒间的曲线变化是由于下列哪种条件的改变所引起的






