学习小组进行实验研究乙醇的化学性质。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(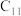 ~
~ 的烷烃)中,现象如下。
的烷烃)中,现象如下。
①对比乙、丙的现象,说明 与
与 反应时断裂
反应时断裂___________ (填序号)。
a.C-H键 b.O-H键 c.C-C键
②乙中反应的化学方程式是___________ 。
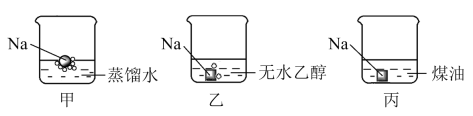
(2)实验室用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图。
①饱和 溶液的作用是
溶液的作用是___________ 。
②关于该实验的说法正确的是___________ (填序号)。
a.浓硫酸是该反应的催化剂
b.在试管中加入几片碎瓷片以防止暴沸
c.实验中加入过量乙醇,可使乙酸的转化率达到100%
(3)发生化学反应时,物质变化的同时常常伴随有能量变化。将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为___________ 能。
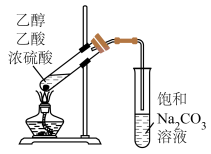
(4)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。
①证实化学能转化为电能的现象是___________ 。
②解释Cu片表面产生气泡的原因:___________ 。
(5)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
当 和
和 化合生成2
化合生成2
 时,放出
时,放出___________  的能量。
的能量。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(
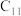 ~
~ 的烷烃)中,现象如下。
的烷烃)中,现象如下。
①对比乙、丙的现象,说明
 与
与 反应时断裂
反应时断裂a.C-H键 b.O-H键 c.C-C键
②乙中反应的化学方程式是
(2)实验室用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图。

①饱和
 溶液的作用是
溶液的作用是②关于该实验的说法正确的是
a.浓硫酸是该反应的催化剂
b.在试管中加入几片碎瓷片以防止暴沸
c.实验中加入过量乙醇,可使乙酸的转化率达到100%
(3)发生化学反应时,物质变化的同时常常伴随有能量变化。将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(4)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是
②解释Cu片表面产生气泡的原因:
(5)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
| 化学键 | H-H | O-O | H-O |
| 键能/kJ·mol | 436 | 498 | 463 |
 和
和 化合生成2
化合生成2
 时,放出
时,放出 的能量。
的能量。
更新时间:2023-07-13 22:26:39
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)异丁烷的结构简式为___________ ,甲基的电子式为___________ ,相对分子质量为86的烷烃的分子式为___________ ,C17H33COOH名称为___________ 。
(2)断开l mol H-H键、1molN-H键、1molN≡N键分别需要吸收能量为436 kJ、391 kJ、946 kJ,则H2与N2反应生成2 mol NH3放出能量___________ kJ。
(2)断开l mol H-H键、1molN-H键、1molN≡N键分别需要吸收能量为436 kJ、391 kJ、946 kJ,则H2与N2反应生成2 mol NH3放出能量
您最近一年使用:0次
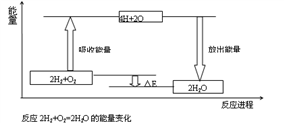
【推荐2】试从化学键的角度理解化学反应中的能量变化。(以2H2+O2===2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH—O键能够释放463KJ能量。
⑴从宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应要______ (填“吸收”或“放出”)能量,能量变化值的大小△E=_________ (用E反和E生表示)
⑵从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=______ KJ;形成生成物中的化学键放出的总能量为=______ KJ。E吸______ E放(填“>”或“<”),所以该反应要_____ (填“吸收”或“放出”)能量,能量变化值的大小△E=____ KJ(填数值)
⑶由图可知,化学反应的本质是________________________________ 化学反应中能量变化的主要原因是________________ (从总能量说明)
⑴从宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应要
⑵从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=
⑶由图可知,化学反应的本质是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】盖斯定律是人们研究热化学的重要工具和方法。
(1)已知1molSi固体中有2molSi—Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi-O键。某些化学键键能(1mol化学键断裂需要吸收的能量)数据如下:
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方式:___________ 。
(2)肼(N2H4)通常作为火箭的燃料。已知3.2g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式:______
(3)煤加工的重要手段是煤的气化,如用煤合成水煤气的原理为C(s)+H2O(g) CO(g)+H2(g) △H。
CO(g)+H2(g) △H。
已知: C(s)+O2(g)=CO2(g) △H=-393.35 kJ·mol-1

CO(g) + O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1
求:①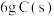 完全燃烧放出的热量为
完全燃烧放出的热量为___________ kJ。
②C(s)+ H2O(g)= CO(g) +H2(g) △H=___________ 。
(1)已知1molSi固体中有2molSi—Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi-O键。某些化学键键能(1mol化学键断裂需要吸收的能量)数据如下:
| 化学键 | Si—O | Si—Si | O=O |
| 键能(kJ·mol-1) | 460 | 176 | 498 |
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方式:
(2)肼(N2H4)通常作为火箭的燃料。已知3.2g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式:
(3)煤加工的重要手段是煤的气化,如用煤合成水煤气的原理为C(s)+H2O(g)
 CO(g)+H2(g) △H。
CO(g)+H2(g) △H。已知: C(s)+O2(g)=CO2(g) △H=-393.35 kJ·mol-1

CO(g) +
 O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1求:①
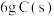 完全燃烧放出的热量为
完全燃烧放出的热量为②C(s)+ H2O(g)= CO(g) +H2(g) △H=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题。
(1)在溴苯的制备实验中,若锥形瓶中有淡黄色沉淀生成,能不能证明该反应中一定有 生成?为什么?
生成?为什么?
_______ 。
(2)在硝基苯的制备实验中,水浴加热有什么优点?_______ 。
(3)在乙醇和乙酸的酯化反应中,怎样加入试剂和碎瓷片_______ 。
(4)在乙醇和乙酸的酯化反应中,若乙酸中的氧为 ,在什么物质中含有
,在什么物质中含有
_______ 。
(1)在溴苯的制备实验中,若锥形瓶中有淡黄色沉淀生成,能不能证明该反应中一定有
 生成?为什么?
生成?为什么?(2)在硝基苯的制备实验中,水浴加热有什么优点?
(3)在乙醇和乙酸的酯化反应中,怎样加入试剂和碎瓷片
(4)在乙醇和乙酸的酯化反应中,若乙酸中的氧为
 ,在什么物质中含有
,在什么物质中含有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)下列实验操作或叙述正确的是_______ (填字母)。
A向饱和苯酚钠溶液中,不断通入足量二氧化碳气体,溶液最终呈浑浊
B.用金属钠检验无水乙醇中含有的少量水
C.除去乙烷中少量的乙烯:与适量的氢气混合加热,把乙烯转化为乙烷
D.向苯酚浓溶液中滴入少量浓溴水可观察到白色的三溴苯酚沉淀
E.用氨水洗去试管内壁的银镜
F.证明氯乙烷分子中含有氯原子,可将氯乙烷溶于 的
的 溶液中
溶液中
G.乙醇与氢溴酸反应中断裂了 键
键
H.甲醛与苯酚制取酚醛树脂的反应属于聚合反应
I.实验室制取乙烯气体时,将温度计的水银球放入液面下
(2)利用如图装置用正丁醇合成正丁醛。
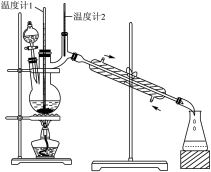
已知:①正丁醇沸点:117.2℃,正丁醛沸点:75.7℃;
②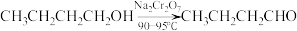
下列说法不正确的是_______。(填字母)
(3)要检验 中的含氧官能团,选用下列的一种试剂是_______(填字母)。
中的含氧官能团,选用下列的一种试剂是_______(填字母)。
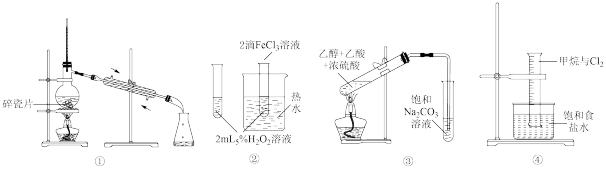
(4)下列对应实验仪器准确的是_______(填字母)。
(1)下列实验操作或叙述正确的是
A向饱和苯酚钠溶液中,不断通入足量二氧化碳气体,溶液最终呈浑浊
B.用金属钠检验无水乙醇中含有的少量水
C.除去乙烷中少量的乙烯:与适量的氢气混合加热,把乙烯转化为乙烷
D.向苯酚浓溶液中滴入少量浓溴水可观察到白色的三溴苯酚沉淀
E.用氨水洗去试管内壁的银镜
F.证明氯乙烷分子中含有氯原子,可将氯乙烷溶于
 的
的 溶液中
溶液中G.乙醇与氢溴酸反应中断裂了
 键
键H.甲醛与苯酚制取酚醛树脂的反应属于聚合反应
I.实验室制取乙烯气体时,将温度计的水银球放入液面下
(2)利用如图装置用正丁醇合成正丁醛。

已知:①正丁醇沸点:117.2℃,正丁醛沸点:75.7℃;
②
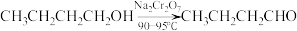
下列说法不正确的是_______。(填字母)
A.为防止产物进一步氧化,应将正丁醇逐滴加入 酸性溶液中 酸性溶液中 |
| B.将产物正丁醛蒸馏出来,有利提高产率 |
| C.向分馏出的馏出物中加入少量金属钠,可检验其中是否含有正丁醇 |
D.向分离所得的粗正丁醛中,加入 固体,过滤,蒸馏,可提纯正丁醛 固体,过滤,蒸馏,可提纯正丁醛 |
 中的含氧官能团,选用下列的一种试剂是_______(填字母)。
中的含氧官能团,选用下列的一种试剂是_______(填字母)。| A.溴水 | B.酸性高锰酸钾溶液 | C.溴的 溶液 溶液 | D.银氨溶液 |

| A.装置①可用于分离苯和溴苯 | B.装置②验证 对 对 分解反应有催化作用 分解反应有催化作用 |
| C.装置③制备并收集乙酸乙酯 | D.装置④量筒内液面上升,内壁出现油状液体 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】I.A的结构式如图,完成下列填空。
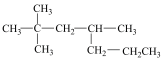
(1)A的一氯代物的同分异构体有___________ 种(不考虑立体异构,下同)。
(2)若A是烯烃B加氢而制得,则这样的烯烃B可能有___________ 种。
Ⅱ.如图,在左试管中先加入2mL95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
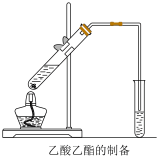
试回答:
(3)在右试管中通常加入___________ 溶液,该溶液的作用是___________ 。分离右试管中所得乙酸乙酯的操作为(只填名称)___________ 。
(4)反应中加入浓硫酸的作用是___________ 。
(5)左试管中发生反应的化学方程式为___________ 。
(6)如果用9.2g的乙醇和18.0g的乙酸反应制得乙酸乙酯10.56g,则本实验的产率是_______ ;(得数保留小数点后一位;产率指的是某种生成物的实际产量与理论产量的比值)。

(1)A的一氯代物的同分异构体有
(2)若A是烯烃B加氢而制得,则这样的烯烃B可能有
Ⅱ.如图,在左试管中先加入2mL95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。

试回答:
(3)在右试管中通常加入
(4)反应中加入浓硫酸的作用是
(5)左试管中发生反应的化学方程式为
(6)如果用9.2g的乙醇和18.0g的乙酸反应制得乙酸乙酯10.56g,则本实验的产率是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】乙烯产量是衡量一个国家石油化工水平的主要标志。下图是由乙烯合成乙酸乙酯可能的合成路线:
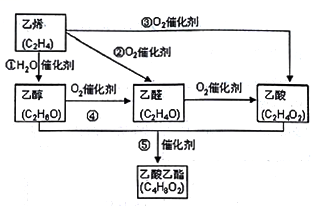
请回答下列问题:
(1)反应④的化学方程式为_______________________________________________________ 。
(2)在实验室制备乙酸乙酯时,用到饱和的碳酸钠溶液,其作用是_____________________ 。
(3)乙醇的结构式为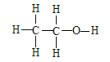 ,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为
,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为_______________________________________ 。

请回答下列问题:
(1)反应④的化学方程式为
(2)在实验室制备乙酸乙酯时,用到饱和的碳酸钠溶液,其作用是
(3)乙醇的结构式为
 ,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为
,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为
您最近一年使用:0次





