氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊溶液中,可以观察到的现象是___________________ ;
(2)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。其反应原理为(用化学方程式表示):________ 。
(3)某同学帮助水质检测站配制480mL 0.5 NaOH溶液以备使用:
NaOH溶液以备使用:
①该同学应称取NaOH固体____________ g;
②上述实验除了需要托盘天平、药匙、烧杯、玻璃棒、量筒等仪器外,还需要的仪器有____________ 。
③下列操作使配制的NaOH溶液浓度偏低的有____________ 。
A.将砝码放在左盘上,NaOH放在右盘上进行称量 B.定容时仰视刻度线
C.定容摇匀后,液面下降,又加水至刻度线 D.溶解后未冷却到室温就转移
(4)取上述配制的NaOH溶液____________ L才能与0.224L氯气(标准状况下)恰好完全反应。
(1)把氯气通入紫色石蕊溶液中,可以观察到的现象是
(2)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。其反应原理为(用化学方程式表示):
(3)某同学帮助水质检测站配制480mL 0.5
 NaOH溶液以备使用:
NaOH溶液以备使用:①该同学应称取NaOH固体
②上述实验除了需要托盘天平、药匙、烧杯、玻璃棒、量筒等仪器外,还需要的仪器有
③下列操作使配制的NaOH溶液浓度偏低的有
A.将砝码放在左盘上,NaOH放在右盘上进行称量 B.定容时仰视刻度线
C.定容摇匀后,液面下降,又加水至刻度线 D.溶解后未冷却到室温就转移
(4)取上述配制的NaOH溶液
更新时间:2023-06-08 17:27:54
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下:
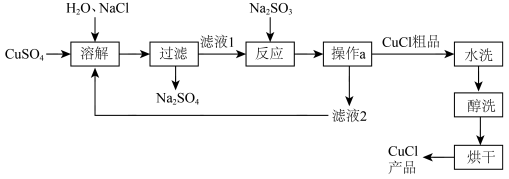
(1)“滤液1”中除了Na+、 外,还存在较多的离子是
外,还存在较多的离子是___________ (写离子符号)
(2)“反应”中发生的化学变化是2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为___________ 。
(3)“操作a”的名称是___________ 。本流程中可以循环利用的物质(水除外)是___________ 。(写化学式)
(4)“水洗”的目的是___________ 。
(5)160gCuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是___________ g。

(1)“滤液1”中除了Na+、
 外,还存在较多的离子是
外,还存在较多的离子是(2)“反应”中发生的化学变化是2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
(3)“操作a”的名称是
(4)“水洗”的目的是
(5)160gCuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】“84消毒液”是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒,在2020年抗击新型冠状病毒过程中,发挥了其重要的作用。某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
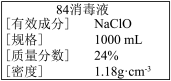
(1)此“84消毒液”的物质的量浓度约为________ 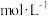 。(计算结果保留一位小数)
。(计算结果保留一位小数)
(2)某同学量取100 mL 此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中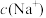 =
=____________ 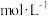 。
。
(3)某同学欲用NaClO固体配制物质的量浓度为0.1mol/L,1000mL NaClO 的消毒液。
①请计算该同学配制此溶液需称取称量NaClO固体的质量为_________ g。
②如图所示的仪器中配制溶液需要使用的是_______ (填仪器序号),还缺少的玻璃仪器是________ 。
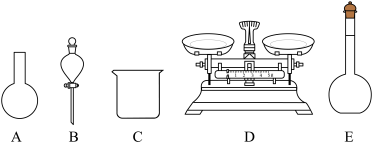
③下列操作中,容量瓶不具备的功能是________ (填序号)。
a. 配制一定体积准确浓度的标准溶液
b. 贮存溶液
c. 测量容量瓶规格以下的任意体积的溶液
d. 用来固体和液体的反应
e. 用来加热溶解固体溶质
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏低的是______ (填序号)。
A. 定容时俯视刻度线 B. 转移前,容量瓶内有蒸馏水
C. 未洗涤烧杯和玻璃棒 D. 定容时水多用胶头滴管吸出

(1)此“84消毒液”的物质的量浓度约为
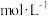 。(计算结果保留一位小数)
。(计算结果保留一位小数)(2)某同学量取100 mL 此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中
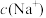 =
=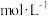 。
。(3)某同学欲用NaClO固体配制物质的量浓度为0.1mol/L,1000mL NaClO 的消毒液。
①请计算该同学配制此溶液需称取称量NaClO固体的质量为
②如图所示的仪器中配制溶液需要使用的是

③下列操作中,容量瓶不具备的功能是
a. 配制一定体积准确浓度的标准溶液
b. 贮存溶液
c. 测量容量瓶规格以下的任意体积的溶液
d. 用来固体和液体的反应
e. 用来加热溶解固体溶质
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏低的是
A. 定容时俯视刻度线 B. 转移前,容量瓶内有蒸馏水
C. 未洗涤烧杯和玻璃棒 D. 定容时水多用胶头滴管吸出
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以废旧铅酸电池中的含铅废料(Pb、PbO、 PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
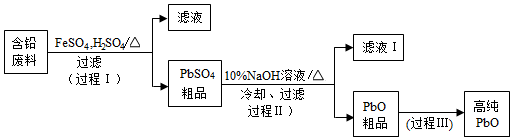
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是_________________________ 。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
ⅰ: 2Fe2++PbO2+4H++SO42-=2Fe3++PbSO4+2H2O
ⅱ:……
写出ⅱ的离子方程式:______________________ 。
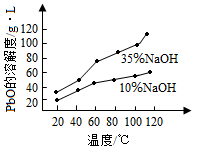
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq) NaHPbO2(aq),其溶解度曲线如图所示。过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是
NaHPbO2(aq),其溶解度曲线如图所示。过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是_________ (选填序号)。
A.减少PbO的损失,提高产品的产率
B.重复利用氢氧化钠,提高原料的利用率
C.增加Na2SO4浓度,提高脱硫效率
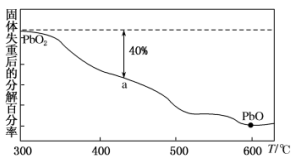
(4)PbO2在加热的过程中发生分解生成PbO和O2,其失重曲线如图所示,已知失重曲线上的a点为样品分解40%的残留固体,若a点固体组成表示为PbOx,则x=_________ 。

(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是
(2)过程Ⅰ中,Fe2+催化过程可表示为:
ⅰ: 2Fe2++PbO2+4H++SO42-=2Fe3++PbSO4+2H2O
ⅱ:……
写出ⅱ的离子方程式:
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)
 NaHPbO2(aq),其溶解度曲线如图所示。过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是
NaHPbO2(aq),其溶解度曲线如图所示。过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是
A.减少PbO的损失,提高产品的产率
B.重复利用氢氧化钠,提高原料的利用率
C.增加Na2SO4浓度,提高脱硫效率
(4)PbO2在加热的过程中发生分解生成PbO和O2,其失重曲线如图所示,已知失重曲线上的a点为样品分解40%的残留固体,若a点固体组成表示为PbOx,则x=

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用如图装置制取氯气,并用氯气进行实验。回答下列问题:
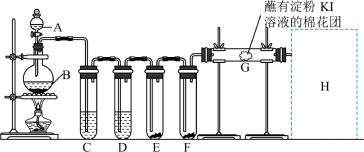
(1)A中盛有浓盐酸,B中盛有 ,该反应的化学方程式为:
,该反应的化学方程式为:___________ ,如果生成1mol的氯气,则被还原的HCl为___________ mol。
(2)D中放入浓 的目的是
的目的是___________ 。
(3)E中为干燥的有色布条,F中为湿润的有色布条,可观察到的现象是___________ ,解释E、F装置中现象不同的原因:___________ 。
(4)G处的现象是___________ 。
(5)用离子方程式写出H处尾气吸收装置中的反应原理___________ 。

(1)A中盛有浓盐酸,B中盛有
 ,该反应的化学方程式为:
,该反应的化学方程式为:(2)D中放入浓
 的目的是
的目的是(3)E中为干燥的有色布条,F中为湿润的有色布条,可观察到的现象是
(4)G处的现象是
(5)用离子方程式写出H处尾气吸收装置中的反应原理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组利用如图所示的装置制备无水氯化铁。
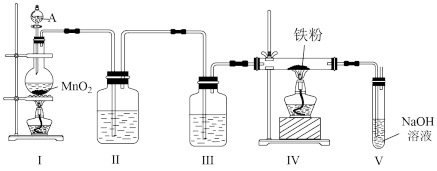
(1)装置Ⅰ中仪器A的名称是_______ ,写出装置Ⅰ中制备氯气的离子方程式_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)写出在装置V中发生的反应的化学方程式_______ 。
(4)实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到_______ ,即可证明滤液中含有 。
。
(5)另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的_______ 装置(填序号)。


(1)装置Ⅰ中仪器A的名称是
(2)装置Ⅱ的作用是
(3)写出在装置V中发生的反应的化学方程式
(4)实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到
 。
。(5)另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】用下图装置可以完成一系列实验(图中夹持装置及加热装置已略去),不考虑①②③中物质间的相互影响。请回答下列问题:
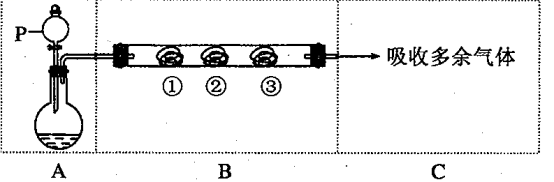
(1)若装置A选用浓盐酸和二氧化锰混合制取Cl2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
(2)若装置A选用浓硫酸和亚硫酸钠固体制取SO2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:

(1)若装置A选用浓盐酸和二氧化锰混合制取Cl2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
| B中棉花的位置 | ① | ② | ③ |
| 所蘸试剂 | 石蕊溶液 | 淀粉KI溶液 | 浓氨水 |
| 现象 | |||
| 涉及的化学方程式 | 3Cl2+8NH3=6NH4Cl+N2 |
(2)若装置A选用浓硫酸和亚硫酸钠固体制取SO2气体,装置B中的三处棉花依次做了如下处理。请填写表中空白:
| B中棉花的位置 | ① | ② | ③ |
| 所蘸试剂 | H2S溶液 | 酸性KMnO4溶液 | 品红溶液 |
| 现象 | 褪色 | ||
| 体现SO2的性质 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐1】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g。
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数______ (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积______ (填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察______ 。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由______ 色变成______ 色。
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1010mol•L-1,则该样品中氮的质量分数为______ 。
步骤I:称取样品1.500g。
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010mol•L-1,则该样品中氮的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用密度为1.84g/cm3,溶质的质量分数为98%的硫酸,配制200mL物质的量浓度为0.46mol/L的硫酸。
(1)应量取98%的硫酸的体积为______ mL,该试验中两次用到玻璃棒,其作用分别是____________ ,____________ 。
(2)使用容量瓶前必须进行的第一步操作是_____________________ 。
(3)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却其正确的操作顺序为___________________________________ 。
(1)应量取98%的硫酸的体积为
(2)使用容量瓶前必须进行的第一步操作是
(3)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却其正确的操作顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】掌握仪器的名称、组装及使用方法是化学实验的基础,下图为两套实验装置。
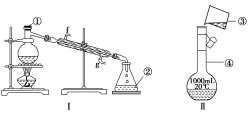
(1)写出下列仪器的名称:①________ ,②________ ,④__________ 。
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有______________ ,将仪器补充完整后进行的实验操作的名称为________ ;冷凝管的进水口是________ (填“f”或“g”);
(3)现需配制250 mL 0.2 mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中的错误是___________________________ 。

(1)写出下列仪器的名称:①
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有
(3)现需配制250 mL 0.2 mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中的错误是
您最近一年使用:0次



