下列各组物质性质的比较,结论正确的是
A.稳定性: | B.分子的极性: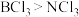 |
C.溶液酸性: | D.沸点: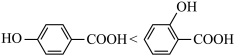 |
更新时间:2023-06-17 18:26:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误 的是
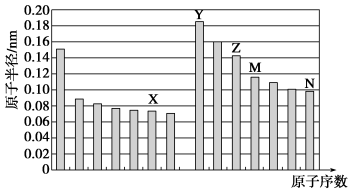
| A.非金属性:X>M |
| B.气态氢化物的稳定性:M<N |
| C.X和Y形成的化合物只可能含离子键 |
| D.M最高价氧化物对应的水化物是一种弱酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期主族元素X、Y、Z的原子序数依次增大,X原子最外层电子数是次外层电子数的3倍,Y是短周期中金属性最强的元素,Z与X位于同一主族。下列叙述正确的是
| A.X是第二周期第ⅣA族元素 | B.Y形成的最高价氧化物的水化物是弱碱 |
| C.X的简单气态氢化物的稳定性比Z的弱 | D.X、Y、Z三种元素可形成化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法错误的是
① 晶体中与每个
晶体中与每个 距离相等且最近的
距离相等且最近的 共有
共有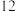 个
个
②含有共价键的晶体一定具有高的熔、沸点及硬度
③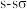 键与
键与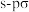 键的电子云形状相同
键的电子云形状相同
④含有 键的化合物与只含
键的化合物与只含 键的化合物的化学性质不同
键的化合物的化学性质不同
①
 晶体中与每个
晶体中与每个 距离相等且最近的
距离相等且最近的 共有
共有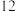 个
个②含有共价键的晶体一定具有高的熔、沸点及硬度
③
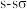 键与
键与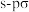 键的电子云形状相同
键的电子云形状相同④含有
 键的化合物与只含
键的化合物与只含 键的化合物的化学性质不同
键的化合物的化学性质不同| A.①② | B.①④ | C.②③ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法错误的是
| A.CO2分子中存在非极性共价键 |
| B.晶体硅的熔点、硬度比金刚石的小 |
| C.NH3的沸点比PH3的高,因为氨分子间存在氢键 |
| D.(NH4)2[PtCl6]既含有离子键又含有共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】研究表明:H2O2具有立体结构,两个氢原子像在一本半展开的书的两页纸上,两页纸面的夹角为94°,氧原子在书的夹缝上,O—H键与O—O键之间的夹角为97°。下列说法不正确的是
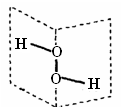

| A.H2O2分子中既含极性键,又含非极性键 |
| B.H2O2为极性分子 |
| C.H2O2分子中的两个O原子均是sp3杂化 |
| D.H2O2分子中既有σ键,又有π键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列证据和推理结论均合理的是
| 证据 | 推理结论 | |
| A | 键角: 、 、 相等 相等 | 键角: 、 、 相等 相等 |
| B | 酸性: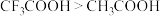 |  键极性: 键极性: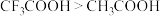 |
| C |  | 非金属性 |
| D | 含碳量:钢>纯铁 | 耐腐蚀性:钢>纯铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是


| A.相对分子质量 | B.稳定性 | C.沸点 | D.R-H键长 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于原子或分子的结构与性质的说法错误的是
①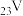 的电子排布式
的电子排布式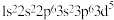 违反了洪特规则
违反了洪特规则
②基态氮原子有3种空间运动状态5种能量不同的电子
③ 、
、 、
、 、
、 熔、沸点随相对分子质量的增大而升高
熔、沸点随相对分子质量的增大而升高
④非极性分子可以含有极性键,但分子的正负电荷中心必须重合
⑤中心原子是 杂化的,其分子的空间结构一定为平面三角形
杂化的,其分子的空间结构一定为平面三角形
⑥邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
①
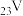 的电子排布式
的电子排布式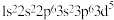 违反了洪特规则
违反了洪特规则②基态氮原子有3种空间运动状态5种能量不同的电子
③
 、
、 、
、 、
、 熔、沸点随相对分子质量的增大而升高
熔、沸点随相对分子质量的增大而升高④非极性分子可以含有极性键,但分子的正负电荷中心必须重合
⑤中心原子是
 杂化的,其分子的空间结构一定为平面三角形
杂化的,其分子的空间结构一定为平面三角形⑥邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
| A.①②⑤ | B.①④⑤ | C.②③⑥ | D.③④⑥ |
您最近一年使用:0次

 为原子序数依次增大的短周期主族元素,已知
为原子序数依次增大的短周期主族元素,已知 原子最外层电子数是其内层电子数的3倍;
原子最外层电子数是其内层电子数的3倍; 原子半径在短周期主族元素中最大;
原子半径在短周期主族元素中最大; 的单质多出现在火山口附近,且为黄色晶体。下列说法正确的是
的单质多出现在火山口附近,且为黄色晶体。下列说法正确的是
 可形成共价化合物
可形成共价化合物

 ,将
,将 转化为
转化为 ,反应过程如图所示。下列说法错误的是
,反应过程如图所示。下列说法错误的是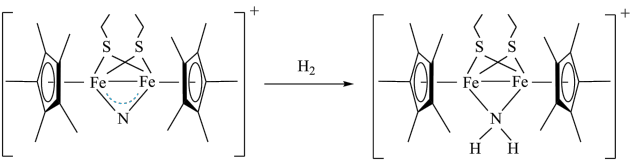

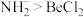
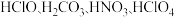 的酸性依次增强
的酸性依次增强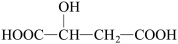 含有1个手性碳原子
含有1个手性碳原子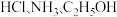 均易溶于水的原因之一是与
均易溶于水的原因之一是与 均能形成氢键
均能形成氢键


