学习化学知识可以辨别“真”“伪”,下列叙述属于“真”的是
A. 可作净水剂的原因是 可作净水剂的原因是 易溶于水 易溶于水 |
| B.电解精炼铜过程中,阳极质量的减少量与阴极质量的增加量相等 |
| C.在测定中和热实验中,使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差 |
D. 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
更新时间:2023-06-20 21:26:14
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作和现象及所得结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向Na2CO3,Na2S的混合溶液中滴入少量AgNO3溶液,有黑色沉淀生成 | Ksp(Ag2S)>Ksp(Ag2CO3) |
| B | 在一块铁片(已除铁锈)上滴2滴含有酚酞的食盐水,静置5~10min,溶液边缘出现红色 | 铁片上发生了析氢腐蚀 |
| C | 测定中和反应的反应热时,将50mL0.55mol·L-1NaOH溶液分批次倒入50mL0.5mol·L-1盐酸中,温度升高3.2℃ | 测得该反应的中和热为ΔH=-53.5kJ·mol-1 |
| D | 用0.1mol·L-1的NaOH溶液滴定20.00mL未知浓度的乙酸溶液,选用甲基橙作指示剂,达到滴定终点时,消耗了20.00mLNaOH溶液 | 乙酸溶液的物质的量浓度大于0.1mol·L-1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学以实验为基础。下列装置或操作不正确的是
 | 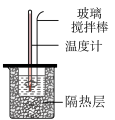 | 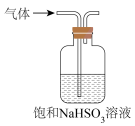 | 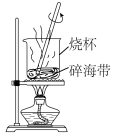 |
| A.碱式滴定管排气泡 | B.测定中和热 | C.除去SO2中少量的HCl | D.灼烧碎海带 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,该反应一定是熵增反应 |
| B.用浓硫酸代替稀硫酸与铁反应能增大生成H2的反应速率 |
| C.NaF水溶液中含有HF,因此NaF溶液不能存放于玻璃试剂瓶中 |
| D.用铜做阳极,电解硫酸铜溶液,溶液中Cu2+的物质的量浓度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】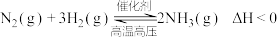 。反应达平衡时,下列措施能提高
。反应达平衡时,下列措施能提高 转化率的是
转化率的是
①降温 ②恒压通入惰性气体 ③增加 的浓度 ④加压
的浓度 ④加压
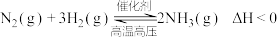 。反应达平衡时,下列措施能提高
。反应达平衡时,下列措施能提高 转化率的是
转化率的是①降温 ②恒压通入惰性气体 ③增加
 的浓度 ④加压
的浓度 ④加压| A.①④ | B.①②④ | C.②③ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某温度下,在金(Au)表面N2O发生分解反应速率方程式为v=kcn(N2O)(k为速率常数,只与温度、催化剂有关,与浓度无关;n为反应级数,可以为正数或负数,也可以为整数、分数或0),N2O的浓度与催化剂表面积及时间关系如图所示。已知反应物消耗一半所用的时间称为半衰期(T1/2)。
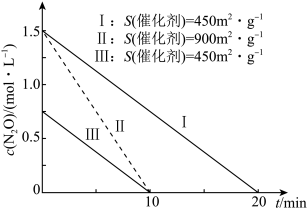
下列叙述错误的是

下列叙述错误的是
| A.该反应级数为2, I条件下k=0.075 mol· L-1 |
| B.在II条件下,O2反应速率为0.075 mol·L-1·min- 1 |
| C.其他条件相同,c(N2O)增大,反应速率不变 |
| D.在III条件下,N2O起始浓度为3.0 mol·L-1时,T1/2为20 min 。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验装置(部分夹持装置略)正确且能够达到实验目的是
| |
|
|
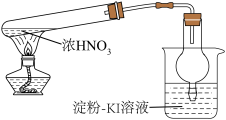
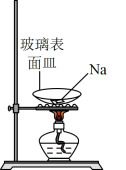
A.验证浓 分解生成 分解生成 | B.铝件镀银 | C.Na的燃烧 | D.制备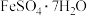 晶体 晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列原理的应用及离子方程式书写均正确的是
A.用 水解制备 水解制备 (加大量水并加热): (加大量水并加热): |
B.泡沫灭火器原理: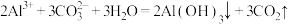 |
C.铅蓄电池放电时正极上的反应: |
D.某弱酸的酸式盐NaHB在水溶液中的水解: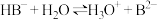 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有关下列图象说法不正确 的是
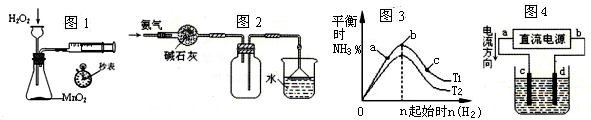
| A.用图1装置定量测定H2O2分解反应的速率 |
| B.图2装置可用于收集并吸收多余的氨气 |
| C.图3表示合成氨反应在其他条件不变的情况下,改变起始物n(H2)对此反应平衡的影响。可知反应物N2的转化率最高的是c点;T1﹤T2,K1>K2(T1和T2表示温度,K1、K2表示对应温度下平衡常数) |
| D.用图4装置完成粗铜的提纯,c为粗铜,d为纯铜,溶液为CuSO4溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各图所示装置能达到实验目的的是


| A.图甲,验证铁的析氢腐蚀 |
| B.图乙,验证外加电流的阴极保护法 |
| C.图丙,钢闸门采用牺牲阳极的阴极保护法 |
| D.图丁,在铁制品上镀铜 |
您最近一年使用:0次

 0.05
0.05
 溶液的试管中,分别滴加4滴0.015
溶液的试管中,分别滴加4滴0.015 溶液,比较两试管颜色
溶液,比较两试管颜色 溶液一次倒入盐酸中,先搅拌均匀,然后插入温度计测量溶液的温度
溶液一次倒入盐酸中,先搅拌均匀,然后插入温度计测量溶液的温度 溶液的
溶液的

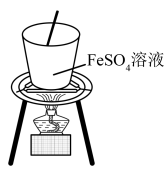
 水解生成
水解生成 胶体,起到净水作用
胶体,起到净水作用 溶液和
溶液和 溶液混合产生泡沫用于灭火
溶液混合产生泡沫用于灭火 溶液和
溶液和


