CO和N2O反应过程中的能量变化如图所示。下列说法正确的是
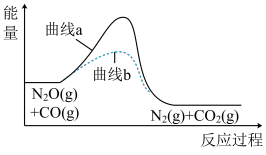

| A.曲线a表示加入催化剂,曲线b表示未加催化剂 |
| B.使用催化剂能提高反应速率,增大反应热 |
| C.NO2和CO的碰撞绝大部分是有效碰撞 |
| D.该反应中反应物总键能低于生成物总键能 |
20-21高二上·广东茂名·期末 查看更多[2]
广东省高州市2020-2021学年高二上学期期末考试化学试题(已下线)专题03 化学反应速率及影响因素、活化能【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
更新时间:2023-06-26 19:47:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知:
①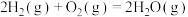
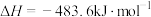
②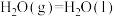
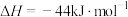
③ 、
、 、
、 键能分别为
键能分别为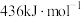 、
、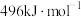 、
、 。
。
下列说法正确的是
①
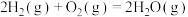
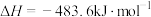
②
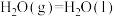
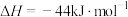
③
 、
、 、
、 键能分别为
键能分别为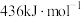 、
、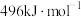 、
、 。
。下列说法正确的是
A.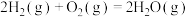 反应不能自发进行 反应不能自发进行 |
B.若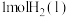 燃烧生成 燃烧生成  时,放出的热量低于 时,放出的热量低于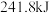 |
C.若只用以上的键能数据,可估算出 的燃烧热 的燃烧热 |
D. 和 和 的能量总和大于 的能量总和大于 的能量 的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据如图所示示意图,下列说法错误的是
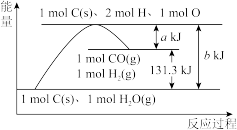
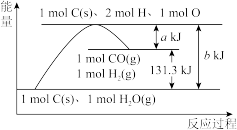
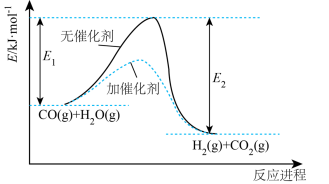
| A.反应C(s)+H2O(g)=CO(g)+H2(g)为吸热反应 |
| B.该反应过程中反应物断键吸收的总能量大于生成物成键放出的总能量 |
| C.1molC(s)、2molH、1molO转变成1molCO(g)和1molH2(g),放出的热量为akJ |
| D.1molC(s)和1molH2O(l)反应生成1molCO(g)和1molH2(g),吸收的热量为131.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知甲酸的分解反应:HCOOH⇌CO+H2O,△H。在H+催化作用下反应历程为:
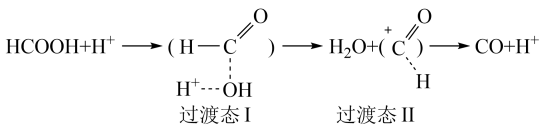
根据过渡态理论,其反应过程中的能量变化如图所示,E1、E2、E3均为大于0。
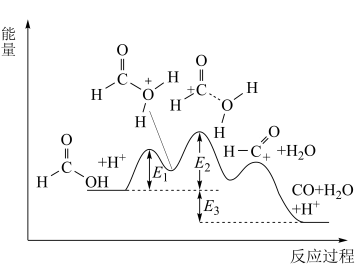
下列说法不正确 的是

根据过渡态理论,其反应过程中的能量变化如图所示,E1、E2、E3均为大于0。

下列说法
| A.E2为正反应的最高活化能 |
| B.该反应为放热反应,△H=E3 |
| C.图像中第一个峰(过渡态)对应的物质结构为过渡态I |
| D.使用催化剂后,正逆反应速率同等程度改变,平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】理论研究表明,在 和
和 下,
下,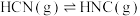 异构化反应过程的能量变化如图所示,下列说法正确的是
异构化反应过程的能量变化如图所示,下列说法正确的是
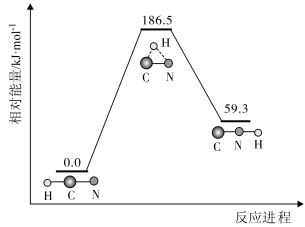
 和
和 下,
下,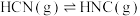 异构化反应过程的能量变化如图所示,下列说法正确的是
异构化反应过程的能量变化如图所示,下列说法正确的是
A.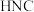 比 比 稳定 稳定 |
| B.使用催化剂,可以改变反应的反应热 |
| C.正反应的活化能小于逆反应的活化能 |
D.该异构化反应的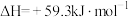 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列化学理论、化工生产或实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 化学反应的历程一般为:普通反应物分子 活化分子 活化分子 产物分子 产物分子 | 普通分子吸收能量转化为活化分子,活化分子间有适当的取向时,才能发生有效碰撞,生成产物分子 |
| B | 把Ba(OH)2•8H2O晶体与氯化铵晶体放入烧杯,用玻璃棒快速搅拌,烧杯变凉 | 反应物的总能量低于生成物的总能量 |
| C | 2NO(g)+2CO(g)=N2(g)+2CO2(g)反应△S<0,但是此反应可以自发进行 | 要判断反应自发进行的方向,必须综合考虑反应体系的焓变和熵变 |
| D | 在2L的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),把密闭容器的容积改为1L,重新发生该反应 2NH3(g),把密闭容器的容积改为1L,重新发生该反应 | 化学反应速率减慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】反应
 的能量变化如图所示。
的能量变化如图所示。
下列说法正确的是
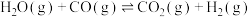
 的能量变化如图所示。
的能量变化如图所示。
下列说法正确的是
A.催化剂能使 、 、 减小值相等 减小值相等 |
| B.升高温度,该反应平衡常数增大 |
| C.平衡时反应物活化分子浓度为0 |
D.增大 的浓度, 的浓度, 的平衡转化率增大 的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用下列实验装置进行相应的实验,能达到实验目的的是
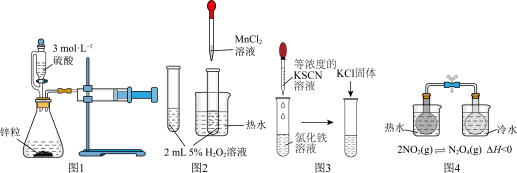

A.图1测量锌粒和稀硫酸反应中生成 的体积,计算该反应的速率 的体积,计算该反应的速率 |
B.图2验证 对过氧化氢的分解有催化作用 对过氧化氢的分解有催化作用 |
| C.图3验证勒夏特列原理中KCl的浓度对该反应平衡的影响 |
| D.图4探究温度对化学平衡的影响 |
您最近一年使用:0次

 和
和 反应生成
反应生成 和
和 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是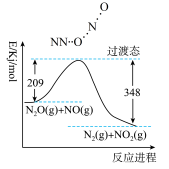
 时转移
时转移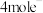
 氮氮三键形成时,该反应放出139KJ的能量
氮氮三键形成时,该反应放出139KJ的能量 和
和 溶液均显碱性,均可用作食用碱和抗酸胃药
溶液均显碱性,均可用作食用碱和抗酸胃药

