下列说法中,正确的是
| A.S区全部是金属元素 |
| B.第四周期元素中,未成对电子数最多的元素位于第VIB族 |
| C.第一电离能的大小可以作为判断元素金属性强弱的依据 |
| D.电负性大于1.8的一定是非金属,小于1.8的一定是金属 |
更新时间:2023-06-25 17:23:35
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 是一种良好的离子导体,具有反钙钛矿晶体结构,
是一种良好的离子导体,具有反钙钛矿晶体结构, 可由以下两种方法制得:
可由以下两种方法制得:
方法I:
方法II: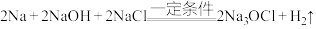
下列说法正确的是
 是一种良好的离子导体,具有反钙钛矿晶体结构,
是一种良好的离子导体,具有反钙钛矿晶体结构, 可由以下两种方法制得:
可由以下两种方法制得:方法I:

方法II:
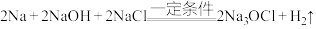
下列说法正确的是
| A.电负性:O>Cl>Na>H |
B.简单离子半径: |
| C.方法II中的反应涉及金属键、离子键、极性键的断裂 |
| D.上述方法涉及的元素中,位于周期表s区的只有一种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】今年是门捷列夫发现元素周期律151周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8.下列说法不正确的是
| W | ||||
| X | Y | Z |
| A.简单离子半径:Y>X |
| B.常温常压下,Y单质可以作光电池材料 |
| C.气态氢化物热稳定性:W<Z |
| D.Z最高价氧化物对应的水化物为中强酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列元素性质的递变规律中正确的是
| A.原子半径:Be<B<C<N |
| B.第一电离能:B<Be<Mg<Na |
| C.电负性:O>N>S>P |
| D.气态氢化物的稳定性:NH3<PH3<SiH4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】物质结构与性质是高中化学的基础,下列说法正确的是
| A.基态氢原子的第一电离能最大 | B.依据 模型预测 模型预测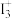 为V形离子 为V形离子 |
C. 晶体中的化学键是纯粹的离子键 晶体中的化学键是纯粹的离子键 | D.液晶不能表现出类似晶体的各向异性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z为原子序数逐渐增大的短周期主族元素。X、Y、Z能形成一种化合物,其结构如图,下列说法错误的是
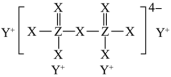
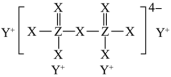
| A.X、Y、Z存在同素异形体 |
| B.简单离子半径:Z>X>Y |
| C.同周期元素组成的单质中Y还原性最强 |
| D.同周期元素中Z的第一电离能大于左右相邻的元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W四种短周期元素在周期表中的位置关系如下图所示,0.1 mol/L X最高价氧化物的水化物pH=1,下列说法正确的是
| X | ||
| Y | Z | W |
| A.离子半径:W<Z | B.第一电离能:Y<Z |
| C.氢化物的稳定性Y>Z>W | D.氢化物的沸点:Y>X |
您最近一年使用:0次
【推荐1】物质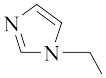 中环上所有原子共面,下列说法错误的是
中环上所有原子共面,下列说法错误的是
 中环上所有原子共面,下列说法错误的是
中环上所有原子共面,下列说法错误的是| A.电负性:N>C>H | B.分子中2个N原子均易与 形成分子间氢键 形成分子间氢键 |
C.分子中的大 键可表示为 键可表示为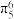 | D.分子中两个N原子的杂化方式相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z是原子序数依次增大的短周期主族元素,原子序数总和为25,由这四种元素形成的某化合物的结构如图所示。下列说法错误的是


A.电负性大小: |
| B.该化合物具有强氧化性,可用于消毒杀菌 |
| C.该化合物含离子键、共价键、配位键 |
| D.该化合物中所有原子最外层均满足8个电子稳定结构 |
您最近一年使用:0次

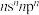 。下列说法错误的是
。下列说法错误的是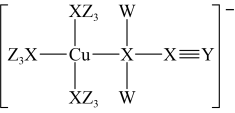
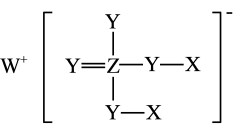
 是一种新型光催化剂.下列说法错误的是
是一种新型光催化剂.下列说法错误的是


