下表是元素周期表的短周期部分

(1)④、⑥和⑧的简单离子的半径从大到小为___________ (用离子符号表示)
(2)②、⑦和⑨的最高价氧化物对应水化物的酸性从强到弱为___________ (用化学式表示)。
(3)实验室制备③的简单氢化物化学方程式为___________ 。⑨所形成的单质与水反应的离子方程式为___________ 。
(4)主族元素砷(As)的部分信息如图所示
①砷(As)在周期表中的位置是___________ 。
②下列说法不正确的是___________ (填序号)。
A.砷元素的最高化合价为+4
B.推测砷有多种氧化物
C.③的气态氢化物的稳定性大于砷的气态氢化物的稳定性
D.As的最高价氧化物对应水化物是一种强酸
(5)设计一个简单的实验证明⑨的非金属性强于⑧___________ 。

(1)④、⑥和⑧的简单离子的半径从大到小为
(2)②、⑦和⑨的最高价氧化物对应水化物的酸性从强到弱为
(3)实验室制备③的简单氢化物化学方程式为
(4)主族元素砷(As)的部分信息如图所示

①砷(As)在周期表中的位置是
②下列说法不正确的是
A.砷元素的最高化合价为+4
B.推测砷有多种氧化物
C.③的气态氢化物的稳定性大于砷的气态氢化物的稳定性
D.As的最高价氧化物对应水化物是一种强酸
(5)设计一个简单的实验证明⑨的非金属性强于⑧
更新时间:2023-06-27 17:13:12
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
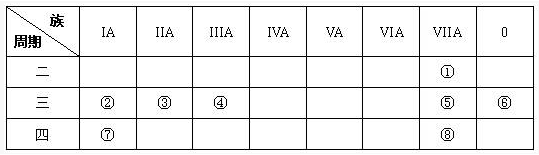
(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______ .
(2)用电子式表示①与③形成化合物的过程______ .:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______ . ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______ .
(4)①②③④四种元素的简单离子半径由大到小的顺序是______ .(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______ .(用化学式和“>”表示)。

(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为
(2)用电子式表示①与③形成化合物的过程
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)①②③④四种元素的简单离子半径由大到小的顺序是
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】短周期元素A、B、C、D在元素周期表中的位置如图所示,其中A所处的周期序数与主族序数相等。
请回答下列问题:
(1)A在周期表中的位置是_____ ;D单质的电子式为_____ 。
(2)C、D的最简单氢化物中,稳定性较强的是_____ (填化学式);C的最高价含氧酸是____ (填“离子”或“共价”)化合物。
(3)A、D的简单离子的半径大小关系为:_____ (用化学式填空);用一个反应可证明元素B、D的非金属性强弱关系,该反应的化学反应方程式为______ 。
| B | D | |
| A | C |
(1)A在周期表中的位置是
(2)C、D的最简单氢化物中,稳定性较强的是
(3)A、D的简单离子的半径大小关系为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示标出的是元素周期表的一部分,据图回答下列问题(用元素符号表示)。

(1)图中用字母标出的14种元素中,金属性最强的是_______ (填相应的化学用语,下同),非金属性最强的是_______ ,d最高价氧化物的电子式_______ 。
(2)b、g气态氢化物中热稳定性最强的是_______ ,b、i、f的离子半径由小到大排列_______ 。
(3)f的 价含氧酸的结构式为
价含氧酸的结构式为_______ ;h与j的最高价氧化物的水化物反应的离子方程式_______ 。
(4)j的一种氧化物常用作呼吸面具的供氧剂,每生成 氧气,转移电子的物质的量为
氧气,转移电子的物质的量为_______ 。

(1)图中用字母标出的14种元素中,金属性最强的是
(2)b、g气态氢化物中热稳定性最强的是
(3)f的
 价含氧酸的结构式为
价含氧酸的结构式为(4)j的一种氧化物常用作呼吸面具的供氧剂,每生成
 氧气,转移电子的物质的量为
氧气,转移电子的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】为验证卤素单质Cl2、Br2、I2氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,说明KMnO4的氧化性比Cl2___________ ,(填“强”或“弱”)对应的离子方程式是___________ 。
(2)B中溶液发生反应的离子方程式是___________ 。
(3)浸有NaOH溶液的棉花的作用是吸收没反应的气体,写出反应的离子方程式:___________ 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作是___________ ,现象是___________ 。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,___________ (填“失电子”或“得电子”)能力逐渐减弱。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,说明KMnO4的氧化性比Cl2
(2)B中溶液发生反应的离子方程式是
(3)浸有NaOH溶液的棉花的作用是吸收没反应的气体,写出反应的离子方程式:
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作是
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D为同一主族元素,C和F为同一主族元素,A元素的原子半径是所有主族元素中原子半径最小的,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中金属离子半径最小的元素,F形成的化合物是形成酸雨的主要原因。请回答下列问题:
(1)写出B元素的名称:_____ 。
(2)写出C元素在周期表中的位置_____ 。
(3)E元素的原子结构示意图为_____ 。
(4)B、D、E三种元素的原子半径由大到小的顺序为_____ (填元素符号)。
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是_____ (填对应氢化物的化学式)。
②F、G的元素最高价氧化物对应水化物酸性较强的是_____ (填对应酸的化学式)。
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为_____ 。
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_____ 。
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:
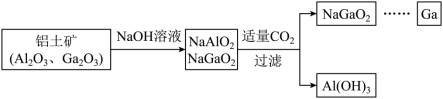
氢氧化镓与NaOH反应的化学方程式为_____ ;酸性:Al(OH)3_____ Ga(OH)3(填“>”或“<”)。
(1)写出B元素的名称:
(2)写出C元素在周期表中的位置
(3)E元素的原子结构示意图为
(4)B、D、E三种元素的原子半径由大到小的顺序为
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是
②F、G的元素最高价氧化物对应水化物酸性较强的是
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:

氢氧化镓与NaOH反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表是指导我们学习元素及其化合物知识的重要工具,除了同周期、同主族元素的变化规律外,某些主族元素与右下方的主族元素的性质相似,称为对角线规则,如钠与钙的化学性质相似。已知碱土金属元素铍(Be)、镁、钙、锶、钡是周期表中第IIA族从上到下排列的元素。
回答下列问题:
(1)锶元素的化合价为_______ ,从铍到钡的金属性逐渐_______ ;从原子结构角度分析,碱土金属元素化学性质相似的原因是_______ 。
(2)预测氢氧化锶属于_______ (填“强”或“弱”)碱,写出金属钙与水反应的化学方程式_______ 。
(3)铍元素与铝的化学性质相似,氢氧化铍具有两性,难溶于水,写出氢氧化铍与氢氧化钠溶液反应的离子方程式_______ 。
(4)过氧化钡化学式为BaO2,其电子式为_______ ,实验室常用BaO2与稀硫酸反应制备过氧化氢,写出反应的化学方程式_______ 。
回答下列问题:
(1)锶元素的化合价为
(2)预测氢氧化锶属于
(3)铍元素与铝的化学性质相似,氢氧化铍具有两性,难溶于水,写出氢氧化铍与氢氧化钠溶液反应的离子方程式
(4)过氧化钡化学式为BaO2,其电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,思考扇形元素周期表的填充规律,回答下列问题:
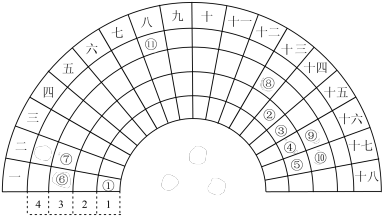
(1)写出⑪在长式周期表中的位置____ 。
(2)在①~⑪元素中,金属性最强的是____ ,在元素④⑥⑨形成的简单离子半径由小到大的顺序是____ (用离子符号表示)。
(3)①~⑪中元素最高价氧化物对应水化物中酸性最强的是____ (填化学式)。写出⑥和⑧的最高价氧化物对应水化物反应的离子方程式____ 。
(4)表中元素④和⑥可以形成一种淡黄色物质X,0.1molX与水反应转移电子数为____ 。

(1)写出⑪在长式周期表中的位置
(2)在①~⑪元素中,金属性最强的是
(3)①~⑪中元素最高价氧化物对应水化物中酸性最强的是
(4)表中元素④和⑥可以形成一种淡黄色物质X,0.1molX与水反应转移电子数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】几种主族元素在周期表中的位置如图。
根据上表回答下列问题:
(1)⑥元素的氢化物是__ (填化学式),__ (填结构式)。
(2)①③⑦三种元素原子半径由大到小的顺序是__ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为__ ,该元素在周期表中的位置是__ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的__ (填化学式)。
(5)①与水反应的离子方程式__ 。
(6)⑦的非金属性强于⑧,下列表述中能证明这一事实的是__ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)④与⑤元素形成的分子可能是__ 。
A. B.
B.  C.
C. 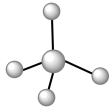
族 周期 | IA | 0 | ||||||
1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ⑤ | ⑥ | ||||||
3 | ① | ③ | ⑦ | |||||
4 | ② | ⑧ |
(1)⑥元素的氢化物是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的
(5)①与水反应的离子方程式
(6)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)④与⑤元素形成的分子可能是
A.
 B.
B.  C.
C. 
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表列出了周期表短周期中7种元素的有关数据:
根据上表信息,回答下列问题:
(1)元素①、②、⑦的最高价氧化物的水化物酸性从大到小的顺序是___________ (填化学式),元素⑤、⑥、⑦的简单离子半径从大到小的顺序是___________ (填离子符号)。
(2)元素③、⑥中氢化物稳定性更强的是___________ (填化学式),③的最高价氧化物的水化物的浓溶液与①的单质反应的化学方程式为___________ 。
(3)7种元素中金属性最强的单质在氧气中完全燃烧所得产物的电子式___________ ,该物质含有的化学键为:___________ 。
(4)下列关于元素周期表的叙述,正确的是___________(填标号)。
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(nm) | 0.077 | 0.110 | 0.102 | 0.152 | 0.186 | 0.071 | 0.099 |
| 最高价态 | +4 | +5 | +6 | +1 | +1 | 0 | +7 |
| 最低价态 | -4 | -3 | -2 | 0 | 0 | -1 | -1 |
(1)元素①、②、⑦的最高价氧化物的水化物酸性从大到小的顺序是
(2)元素③、⑥中氢化物稳定性更强的是
(3)7种元素中金属性最强的单质在氧气中完全燃烧所得产物的电子式
(4)下列关于元素周期表的叙述,正确的是___________(填标号)。
| A.元素周期表共有7个横行,称为周期;共有16个纵行,称为族 |
| B.前20号元素称为短周期元素 |
| C.副族元素中,没有非金属元素 |
| D.ⅠA族的元素都被称作碱金属元素 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W、Q均为短周期主族元素。X是原子半径最小的元素;Y是地壳中含量最高的元素;Z是非金属性最强的元素,Z和W同主族;Q是短周期金属性最强的元素。回答下列问题:
(1)X与W形成化合物的电子式为_______ ;Y在元素周期表中的位置为_______ 。
(2) 属于
属于_______ (填“共价化合物”或“离子化合物”)。
(3)Z、W简单气态氢化物稳定性较强的是_______ (填化学式)。
(4)W、Q最高价氧化物对应水化物之间W、Q最高价氧化物对应水化物为_______ 。
(1)X与W形成化合物的电子式为
(2)
 属于
属于(3)Z、W简单气态氢化物稳定性较强的是
(4)W、Q最高价氧化物对应水化物之间W、Q最高价氧化物对应水化物为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.下表为元素周期表的一部分,请回答下列问题。_______ ;画出元素⑥的原子的电子排布式_______ 。
(2)②、③、④的第一电离能由大到小的顺序为(用元素符号表示)_______ 。
(3)③、⑤的简单氢化物的沸点由高到低的顺序是(用化学式表示)_______ ,原因是_______ 。
(4)②形成的简单氢化物的空间结构是_______ ,其原子的杂化方式是_______ 。
(5)①、②、⑥形成的化合物中,化学键类型有_______ ,电子式是_______ 。
Ⅱ.在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示,试回答:_______ 。
(7)该晶体中钙、氧、钛的离子个数比是_______ 。

(2)②、③、④的第一电离能由大到小的顺序为(用元素符号表示)
(3)③、⑤的简单氢化物的沸点由高到低的顺序是(用化学式表示)
(4)②形成的简单氢化物的空间结构是
(5)①、②、⑥形成的化合物中,化学键类型有
Ⅱ.在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示,试回答:

(7)该晶体中钙、氧、钛的离子个数比是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、G五种短周期主族元素,原子序数依次增大,X元素的气态氢化物水溶液呈碱性;Y、M同主族,可形成MY2、MY3两种分;元素Z和G可形成1:1的离子化合物,请回答下列问题:
(1)Y在元素周期表中的位置为___________ .
(2)元素Y和Z按原子个数1:1形成的化合物中存在化学键的类型_____________ .
(3)能说明元素G的非金属性比元素M的非金属性强的是_________ (填序号).
①最高价氧化物对应水化物的酸性:G比M强
②气态氢化物的还原性:M比G强
③气态氢化物溶于水后的酸性:G比M强
④G的最高正价比M的最高正价高
(4)M和X可形成一种化合物,其相对分子质量在170~190之间,且M的质量分数约为70%,该化合物的化学式为___________ .
(1)Y在元素周期表中的位置为
(2)元素Y和Z按原子个数1:1形成的化合物中存在化学键的类型
(3)能说明元素G的非金属性比元素M的非金属性强的是
①最高价氧化物对应水化物的酸性:G比M强
②气态氢化物的还原性:M比G强
③气态氢化物溶于水后的酸性:G比M强
④G的最高正价比M的最高正价高
(4)M和X可形成一种化合物,其相对分子质量在170~190之间,且M的质量分数约为70%,该化合物的化学式为
您最近一年使用:0次



