已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D为同一主族元素,C和F为同一主族元素,A元素的原子半径是所有主族元素中原子半径最小的,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中金属离子半径最小的元素,F形成的化合物是形成酸雨的主要原因。请回答下列问题:
(1)写出B元素的名称:_____ 。
(2)写出C元素在周期表中的位置_____ 。
(3)E元素的原子结构示意图为_____ 。
(4)B、D、E三种元素的原子半径由大到小的顺序为_____ (填元素符号)。
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是_____ (填对应氢化物的化学式)。
②F、G的元素最高价氧化物对应水化物酸性较强的是_____ (填对应酸的化学式)。
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为_____ 。
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_____ 。
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:
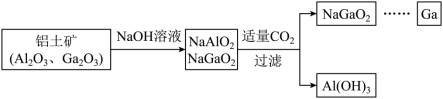
氢氧化镓与NaOH反应的化学方程式为_____ ;酸性:Al(OH)3_____ Ga(OH)3(填“>”或“<”)。
(1)写出B元素的名称:
(2)写出C元素在周期表中的位置
(3)E元素的原子结构示意图为
(4)B、D、E三种元素的原子半径由大到小的顺序为
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是
②F、G的元素最高价氧化物对应水化物酸性较强的是
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:

氢氧化镓与NaOH反应的化学方程式为
更新时间:2022-12-13 21:09:00
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答问题:
(1)镁元素在周期表中的位置是_______ 。
(2)②的最高价氧化物的结构式为_______ 。
(3)④⑤元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:_______ ;写出⑥的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式_______ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能 具有的性质是_______(填字母)。
(5)已知X为第ⅡA族元素(前四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,写出Y的原子序数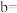
_______ (用含a的代数式表示)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的最高价氧化物的结构式为
(3)④⑤元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W
A.最高化合价为 |
B.简单气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 |
| D.单质在常温下可与氢气化合 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为九种主族元素在周期表中的位置:
请回答下列问题:
(1)I元素的位置是第________ 周期,第______ 族。
(2)C、B、D 三种元素的金属性由强到弱的顺序为_______ (填元素符号)。
(3)E、F两种元素对应的最简单氢化物的稳定性:________________ (填化学式)。
(4)C的单质与水反应的离子方程式为_______ 。
(5)用电子式表示A和G形成化合物的过程:____ 。
| A | |||||||
| E | F | ||||||
| B | D | I | G | ||||
| C | H | ||||||
请回答下列问题:
(1)I元素的位置是第
(2)C、B、D 三种元素的金属性由强到弱的顺序为
(3)E、F两种元素对应的最简单氢化物的稳定性:
(4)C的单质与水反应的离子方程式为
(5)用电子式表示A和G形成化合物的过程:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。
(1)“类铝”在门捷列夫顶言4年后,被布瓦博德朗在一种矿石中发现,命名为镓( )。
)。
①镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为_______ 。
②已知 难溶于水,为判断
难溶于水,为判断 是否为两性氢氧化物,设计实验时,需要选用的试剂有
是否为两性氢氧化物,设计实验时,需要选用的试剂有 溶液、
溶液、_______ 和_______ 。
③工业上冶炼金属镓通常采用的方法是_______ 。
④设计实验证明碱性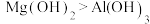 :
:_______ 。
(2)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗( )。
)。
①硅和锗单质分别与 反应时,反应较难进行的是
反应时,反应较难进行的是_______ (填“硅”或“锗”)。
②根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
(3)某同学查找 、
、 、
、 三种元素在周期表的位置如图所示:
三种元素在周期表的位置如图所示:
 、
、 、
、 的
的 价氢氧化物碱性强弱顺序为
价氢氧化物碱性强弱顺序为_______ (用化学式表示)。
(1)“类铝”在门捷列夫顶言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(
 )。
)。①镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为
②已知
 难溶于水,为判断
难溶于水,为判断 是否为两性氢氧化物,设计实验时,需要选用的试剂有
是否为两性氢氧化物,设计实验时,需要选用的试剂有 溶液、
溶液、③工业上冶炼金属镓通常采用的方法是
④设计实验证明碱性
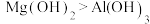 :
:(2)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(
 )。
)。①硅和锗单质分别与
 反应时,反应较难进行的是
反应时,反应较难进行的是②根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是
(3)某同学查找
 、
、 、
、 三种元素在周期表的位置如图所示:
三种元素在周期表的位置如图所示:| 周期 | ⅣA |
| 4 |  |
| 5 |  |
| 6 |  |
 、
、 、
、 的
的 价氢氧化物碱性强弱顺序为
价氢氧化物碱性强弱顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】SO2是大气污染物,SO2废气的处理可以先用H2还原成H2S后再设法回收S,主要涉及反应:3H2+SO2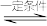 H2S+2H2O。完成下列填空:
H2S+2H2O。完成下列填空:
(1)写出硫化氢的电子式_______ ,硫原子的核外有_______ 种不同运动状态的电子。
(2)列举一个硫元素比氧元素非金属性弱的事实:_______ 。
(3)在一定温度下,向2L反应器中通入含SO2的废气与H2,经过10min,有0.4mol水生成,则这段时间内v(SO2)=_______ 。
(4)一定条件下SO2与H2的反应达到平衡时,SO2的平衡转化率随温度(t)、压强(P)的变化如下图所示:
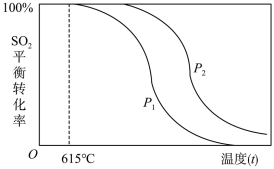
①根据上述信息可以判断:P1_______ P2(填“>”、“<”或“=”)
②随着温度的升高,该反应的化学平衡常数K将_______ (填“变大”、“变小”或“不变”)。
③SO2废气的另一种处理方法是用Na2SO3溶液吸收,得到NaHSO3溶液。
(5)写出该方法吸收SO2的化学方程式_______ 。
(6)所得的NaHSO3溶液呈酸性,运用相关化学用语进行解释_______ 。
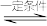 H2S+2H2O。完成下列填空:
H2S+2H2O。完成下列填空:(1)写出硫化氢的电子式
(2)列举一个硫元素比氧元素非金属性弱的事实:
(3)在一定温度下,向2L反应器中通入含SO2的废气与H2,经过10min,有0.4mol水生成,则这段时间内v(SO2)=
(4)一定条件下SO2与H2的反应达到平衡时,SO2的平衡转化率随温度(t)、压强(P)的变化如下图所示:

①根据上述信息可以判断:P1
②随着温度的升高,该反应的化学平衡常数K将
③SO2废气的另一种处理方法是用Na2SO3溶液吸收,得到NaHSO3溶液。
(5)写出该方法吸收SO2的化学方程式
(6)所得的NaHSO3溶液呈酸性,运用相关化学用语进行解释
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如图:
(1)属于第二周期且无正价的元素是_____ (填元素符号,下同),属于第ⅤA族的是_____ ,化学性质最稳定的元素是_____ 。
(2)H的最高价氧化物与L的最高价氧化物对应水化物反应的离子方程式为:_____ 。
(3)B与J形成原子个数比为1∶1的化合物,该化合物的电子式为:______ ,含有共价键的类型为:_____ ;用电子式表示N与K形成离子化合物的过程_____ 。
(4)A、G、F气态氢化物稳定性由强至弱的顺序:_____ (用对应的化学式表示);B、I、F、K、N对应的简单离子的半径由大到小的顺序:_____ (用对应的离子符号表示)。
| 周期 | ||||||||||||||||||
| 1 | ||||||||||||||||||
| 2 | D | B | A | |||||||||||||||
| 3 | J | I | H | C | G | F | E | |||||||||||
| 4 | L | K | N | |||||||||||||||
| 5 | M | |||||||||||||||||
| 6 | ||||||||||||||||||
(2)H的最高价氧化物与L的最高价氧化物对应水化物反应的离子方程式为:
(3)B与J形成原子个数比为1∶1的化合物,该化合物的电子式为:
(4)A、G、F气态氢化物稳定性由强至弱的顺序:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E、F、G七种短周期元素,其原子序数依次增大.A的质量数等于其质子数;B原子的最外层电子数是其电子层数的2倍;D的最外层电子数是其电子层数的3倍;E、F、G三种元素同周期且它们的最高价氧化物的水化物两两反应生成均盐和水,E、F、G的最外层电子数之和为10.回答下列问题。
(1)元素C、G的名称____ ,____ ;
(2)F元素在周期表中的位置____ ;
(3)以上七种元素能形成的最高价氧化物对应的水合物中酸性最强的为____ (填化学式);
(4)D、E两元素形成的1:1的化合物的电子式____ ,其中含有的化学键的类型为____ ;用电子式表示A、C两元素组成中学化学最常见化合物的形成过程____ ;
(5)写出分别由A、D、E、G四种元素组成的两种化合物反应的离子方程式____ ;
(1)元素C、G的名称
(2)F元素在周期表中的位置
(3)以上七种元素能形成的最高价氧化物对应的水合物中酸性最强的为
(4)D、E两元素形成的1:1的化合物的电子式
(5)写出分别由A、D、E、G四种元素组成的两种化合物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,相关信息如表。
(1)元素Y在元素周期表中的位置是_______ 。
(2)W的单质与氢氧化钠溶液反应的离子方程式为_______ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

已知:H2SiO3是一种难溶于水的白色物质。
①M为_______ (填化学式),其作用是_______ 。
②能说明X元素的非金属性比硅元素强的实验现象是_______ 。
(5)元素Z与W相比,金属性较强的是_______ (填元素名称),请写出能证明这一结论的实验事实_______ (列举一条)。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是内层电子数的2倍 |
| Y | 其单质与氢气在暗处能剧烈化合并发生爆炸 |
| Z | 短周期主族元素中原子半径最大 |
| W | 其氧化物是两性氧化物 |
| Q | 同周期元素中,最高价氧化物对应水化物的酸性最强 |
(1)元素Y在元素周期表中的位置是
(2)W的单质与氢氧化钠溶液反应的离子方程式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

已知:H2SiO3是一种难溶于水的白色物质。
①M为
②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:

(1)④、⑤、⑦的原子半径由大到小的顺序为____________ (用化学用语表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_______________ 。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式_________________ 。
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式:_______________________ 。
②写出检验A溶液中溶质的阴离子的方法:___________________ 。
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液中的c(OH- ) =10-2 mol/L (忽略溶液体积变化),则该电解过程中转移电子的物质的量为_________ mol。

(1)④、⑤、⑦的原子半径由大到小的顺序为
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式:
②写出检验A溶液中溶质的阴离子的方法:
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液中的c(OH- ) =10-2 mol/L (忽略溶液体积变化),则该电解过程中转移电子的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】短周期主族元素 、
、 、
、 、
、 的原子序数依次增大,其族序数之和为15,
的原子序数依次增大,其族序数之和为15, 最外层电子数是内层的3倍,
最外层电子数是内层的3倍, 、
、 相邻,
相邻, 的
的 电子层有1个电子。回答下列问题:
电子层有1个电子。回答下列问题:
(1) 在元素周期表的位置是
在元素周期表的位置是_______ , 的原子结构示意图为
的原子结构示意图为_______ 。
(2) 与
与 的简单氢化物中较稳定的是
的简单氢化物中较稳定的是_______ (填化学式,下同), 与
与 的简单离子,半径较大的是
的简单离子,半径较大的是_______ 。
(3) 与
与 两元素的单质反应,生成原子个数比为
两元素的单质反应,生成原子个数比为 的化合物,该化合物的电子式为
的化合物,该化合物的电子式为_______ ,含有的化学键类型是_______ 。
(4) 与
与 两元素的最高价氧化物的水化物相互反应的离子方程式为
两元素的最高价氧化物的水化物相互反应的离子方程式为_______ 。
 、
、 、
、 、
、 的原子序数依次增大,其族序数之和为15,
的原子序数依次增大,其族序数之和为15, 最外层电子数是内层的3倍,
最外层电子数是内层的3倍, 、
、 相邻,
相邻, 的
的 电子层有1个电子。回答下列问题:
电子层有1个电子。回答下列问题:(1)
 在元素周期表的位置是
在元素周期表的位置是 的原子结构示意图为
的原子结构示意图为(2)
 与
与 的简单氢化物中较稳定的是
的简单氢化物中较稳定的是 与
与 的简单离子,半径较大的是
的简单离子,半径较大的是(3)
 与
与 两元素的单质反应,生成原子个数比为
两元素的单质反应,生成原子个数比为 的化合物,该化合物的电子式为
的化合物,该化合物的电子式为(4)
 与
与 两元素的最高价氧化物的水化物相互反应的离子方程式为
两元素的最高价氧化物的水化物相互反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍。试回答:
(1)这四种元素分别是:A________ ,B________ ,C________ ,D________ 。
(2)这四种元素中在常温常压下的液态或气态氢化物的稳定性由大而小的顺序是________ 。
(3)A与B形成的三原子分子的电子式是________ ,B与D形成的原子个数比为1∶1的化合物的电子式是________ 。
(4)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是_______________________________ 。
(5)非金属性:A_______ C(填“>”,“=”,“<”),可以判断出这一结论的化学方程式是:________________________________________________________________ 。
(1)这四种元素分别是:A
(2)这四种元素中在常温常压下的液态或气态氢化物的稳定性由大而小的顺序是
(3)A与B形成的三原子分子的电子式是
(4)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是
(5)非金属性:A
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知1到18号元素中的X、Y、Z、W、R五种元素,元素X的一种核素不含中子,Y的最外层电子数是次外层电子数的两倍,Z的最外层电子数比Y多2,W的原子失去1个电子后与 具有相同的电子层结构,R的原子序数为17。回答下列问题:
具有相同的电子层结构,R的原子序数为17。回答下列问题:
(1)元素Y的元素符号__________ ;Z的离子结构示意图__________ 。
(2) 是一种化学用语,用来表示核素。元素X的某核素与不含中子的核素互称同位素,则这种核素可表示为
是一种化学用语,用来表示核素。元素X的某核素与不含中子的核素互称同位素,则这种核素可表示为__________ (任写一种,X用元素符号表示)。
(3)化合物 与
与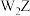 反应的化学方程式
反应的化学方程式____________________ 。
(4)图1为教材中模拟工业制备 的装置,通电后,U型管内发生的反应的化学方程式为(R用相应元素符号表示)
的装置,通电后,U型管内发生的反应的化学方程式为(R用相应元素符号表示)____________________ ,在两电极区分别滴入2滴酚酞溶液,观察到溶液变红现象的是__________ 极区(选填“a”、“b”)。
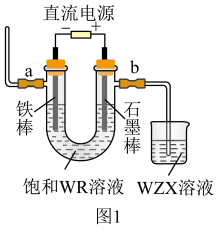
(5)多种含R元素的化合物因为具有强氧化性,常用于杀菌、消毒、漂白。
① 时,将气体
时,将气体 溶于水形成“
溶于水形成“ (气体)—
(气体)— (水溶液)”体系,体系中
(水溶液)”体系,体系中 (溶液)、
(溶液)、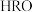 和
和 三者的物质的量分数(
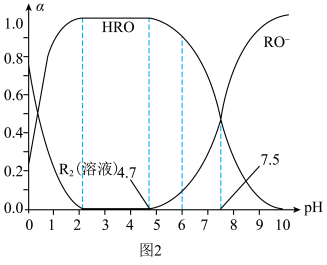
三者的物质的量分数( )随
)随 变化的关系如图2所示。已知
变化的关系如图2所示。已知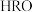 的杀菌能力比
的杀菌能力比 强,用
强,用 处理饮用水时,杀菌效果最强的
处理饮用水时,杀菌效果最强的 范围为
范围为__________ (填字母)。
A.0~2 B.2~4.7 C.4.7~7.5 D.7.5~10
② 的杀菌效果比
的杀菌效果比 好。常用的制备
好。常用的制备 的反应原理可用下面的化学方程式表示,在方程式中标出电子转移的方向和数目:
的反应原理可用下面的化学方程式表示,在方程式中标出电子转移的方向和数目: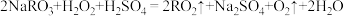
______ ;等物质的量的 杀菌效果是
杀菌效果是 的
的__________ 倍( 与
与 消毒杀菌后均被还原为
消毒杀菌后均被还原为 ,杀菌效果与单位物质的量的氧化剂得电子的物质的量有关)。
,杀菌效果与单位物质的量的氧化剂得电子的物质的量有关)。
 具有相同的电子层结构,R的原子序数为17。回答下列问题:
具有相同的电子层结构,R的原子序数为17。回答下列问题:(1)元素Y的元素符号
(2)
 是一种化学用语,用来表示核素。元素X的某核素与不含中子的核素互称同位素,则这种核素可表示为
是一种化学用语,用来表示核素。元素X的某核素与不含中子的核素互称同位素,则这种核素可表示为(3)化合物
 与
与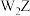 反应的化学方程式
反应的化学方程式(4)图1为教材中模拟工业制备
 的装置,通电后,U型管内发生的反应的化学方程式为(R用相应元素符号表示)
的装置,通电后,U型管内发生的反应的化学方程式为(R用相应元素符号表示)
(5)多种含R元素的化合物因为具有强氧化性,常用于杀菌、消毒、漂白。
①
 时,将气体
时,将气体 溶于水形成“
溶于水形成“ (气体)—
(气体)— (水溶液)”体系,体系中
(水溶液)”体系,体系中 (溶液)、
(溶液)、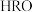 和
和 三者的物质的量分数(
三者的物质的量分数( )随
)随 变化的关系如图2所示。已知
变化的关系如图2所示。已知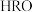 的杀菌能力比
的杀菌能力比 强,用
强,用 处理饮用水时,杀菌效果最强的
处理饮用水时,杀菌效果最强的 范围为
范围为A.0~2 B.2~4.7 C.4.7~7.5 D.7.5~10

②
 的杀菌效果比
的杀菌效果比 好。常用的制备
好。常用的制备 的反应原理可用下面的化学方程式表示,在方程式中标出电子转移的方向和数目:
的反应原理可用下面的化学方程式表示,在方程式中标出电子转移的方向和数目: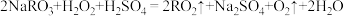
 杀菌效果是
杀菌效果是 的
的 与
与 消毒杀菌后均被还原为
消毒杀菌后均被还原为 ,杀菌效果与单位物质的量的氧化剂得电子的物质的量有关)。
,杀菌效果与单位物质的量的氧化剂得电子的物质的量有关)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知W、X、Y、Z是短周期的四种元素,其相关信息与原子半径关系如表所示:
(1)W元素位于元素周期表第____________ 周期____________ 族,W与X形成化合物的化学式为____________ 。
(2)W、X、Z的简单离子半径由大到小的顺序为__________ (用离子符号表示)。
(3)实验室制备Y的最高价氧化物对应水化物的方法是____________________ (写出操作方法),Y的最高价氧化物与X的最高价氧化物对应水化物反应的离子方程式为______________________ 。
(4)Y、Z的最高价氧化物对应水化物的酸性由强到弱的顺序为____________________ 。
| 元素 | 相关信息 | 原子半径关系 |
| W | 其中一种核素的质量数为18,中子数为10 |  |
| X | 与Ne原子的核外电子数相差1 | |
| Y | 单质是一种常见的半导体材料 | |
| Z | 非金属性在同周期主族元素中最强 |
(2)W、X、Z的简单离子半径由大到小的顺序为
(3)实验室制备Y的最高价氧化物对应水化物的方法是
(4)Y、Z的最高价氧化物对应水化物的酸性由强到弱的顺序为
您最近一年使用:0次



