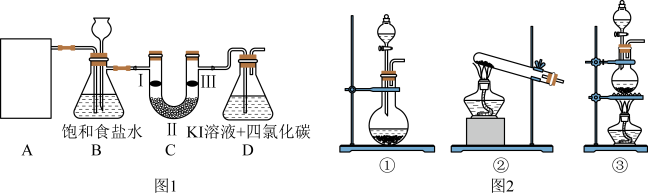
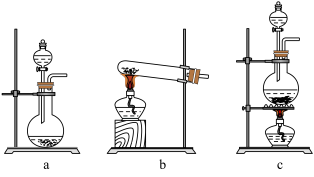
下图是实验室制备氯气并进行一系列相关实验的部分装置(夹持设备已略)。
(1)实验室可以用 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为_______ 。该实验中,A部分的发生装置可选图2中的_______ (填序号)。
(2)装置B中饱和食盐水的作用是_______ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,写出发生堵塞时B中的现象_______ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入_______ (填字母)。
(4)设计装置D的目的是比较氯、碘单质的氧化性。当向D中缓缓通入一定量氯气时,观察到D中_______ ,即可证明 氧化性大于
氧化性大于 。
。
(5)该实验装置存在明显的缺陷,应进行的改进措施是_______ (用离子方程式表示)。

(1)实验室可以用
 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入
| 选项 | a | b | c | d |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
 氧化性大于
氧化性大于 。
。(5)该实验装置存在明显的缺陷,应进行的改进措施是
20-21高一上·陕西汉中·期末 查看更多[3]
宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)陕西省汉中市2020-2021学年高一上学期期末考试化学试题
更新时间:2023-07-31 16:18:06
|
相似题推荐
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐1】氯气与水的反应
(1)新制氯水能杀菌、消毒,是因为氯气与H2O反应,反应的化学方程式是_______ :,次氯酸具有强氧化性,能杀菌、消毒。
(2)氯水的成分:
①稳定性:
次氯酸分解反应的化学方程式为_______ 。
②强氧化性:
a.能将有色物质氧化为无色物质,作漂白剂。
b.杀菌、消毒。
③弱酸性:
HClO的酸性比H2CO3弱,向NaClO溶液中通入足量CO2,离子方程式为:_______ 。
(1)新制氯水能杀菌、消毒,是因为氯气与H2O反应,反应的化学方程式是
(2)氯水的成分:

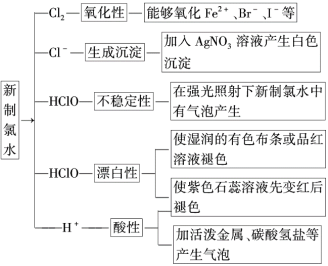
①稳定性:
次氯酸分解反应的化学方程式为
②强氧化性:
a.能将有色物质氧化为无色物质,作漂白剂。
b.杀菌、消毒。
③弱酸性:
HClO的酸性比H2CO3弱,向NaClO溶液中通入足量CO2,离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐2】已知反应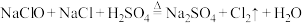 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
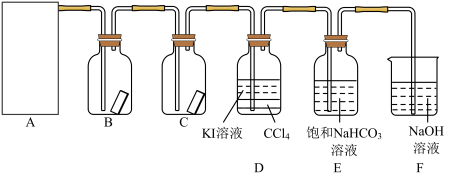
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是_______ (填字母)。
(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是_______ ,请提出合理的改进方法:_______ 。
(3)写出氯气与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ,该反应中氧化剂与还原剂的物质的量之比为_______ 。为验证尾气吸收后的溶液中存在 ,正确的操作是
,正确的操作是_______ 。
(4)氯气通入饱和 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有_______ (填化学式)。
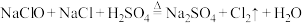 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是

(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
(3)写出氯气与
 溶液反应的离子方程式:
溶液反应的离子方程式: ,正确的操作是
,正确的操作是(4)氯气通入饱和
 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
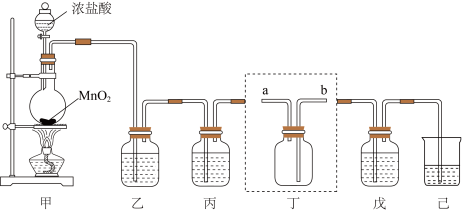
(1)盛装浓盐酸的仪器的名称为______ ,装置甲中发生反应的离子方程式为______ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为______ (填a或b);装置乙盛装的试剂是______ 。
(3)将氯气通入装置己中制备“84”漂白液,其有效成分是:______ (填化学式);有同学认为装置己还有一个作用,该作用为______ 。
(4)“84消毒液”使用时应按比例稀释,放置20~30min,在空气中放置过程中生成碳酸氢钠,该反应的离子方程式为:______ 。
(5)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为______ 。

(1)盛装浓盐酸的仪器的名称为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备“84”漂白液,其有效成分是:
(4)“84消毒液”使用时应按比例稀释,放置20~30min,在空气中放置过程中生成碳酸氢钠,该反应的离子方程式为:
(5)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐1】如下图所示的装置中,A是氯气发生装置,C、D 为气体净化装置(C中装有饱和食盐水;D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液。

试回答:
(1)实验室制氯气的化学方程式:_______ ;
(2)C装置的作用是_______ ;D 装置的作用是_______ ;E中发生化学反应的方程式为:_______ 。
(3)烧杯G 中装有氢氧化钠溶液的作用是_______ ;发生反应的化学方程式为:_______ 。

试回答:
(1)实验室制氯气的化学方程式:
(2)C装置的作用是
(3)烧杯G 中装有氢氧化钠溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】某化学兴趣小组用图甲装置制备了氯气,并进行了一系列实验。
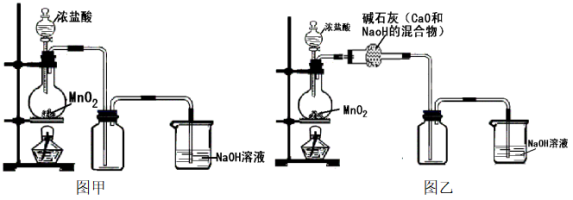
(1)实验室制备氯气的反应的化学方程式是_______ 。
(2)乙同学认为图甲装置制备的氯气不纯净,其中混有HCl气体和水蒸气,对装置进行了如图乙改进。你认为合理吗?(合理则填入“合理”二字,如不合理则填入“不合理”并用文字说明理由)_______ ;
(3)最后均将气体通入氢氧化钠溶液中,这样做的目的是_______ 。

(1)实验室制备氯气的反应的化学方程式是
(2)乙同学认为图甲装置制备的氯气不纯净,其中混有HCl气体和水蒸气,对装置进行了如图乙改进。你认为合理吗?(合理则填入“合理”二字,如不合理则填入“不合理”并用文字说明理由)
(3)最后均将气体通入氢氧化钠溶液中,这样做的目的是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】某学习小组用如图装置研究气体X的性质,气体X的主要成分是Cl2,其中含有少量水蒸气。请回答下列问题:
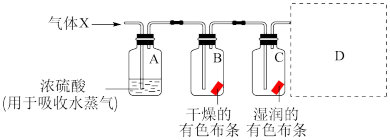
(1)分别描述B、C装置中的现象________________________________________________ ;结合化学方程式及物质性质说明B、C装置中现象不同的原因_________________________________________________ 。
(2)Cl2是有毒气体,为了防止多余Cl2污染空气,可以在D处用如图装置进行尾气处理,请画出装置示意图并标明所加试剂,用离子方程式表示该原理___________________________________________ 。

(1)分别描述B、C装置中的现象
(2)Cl2是有毒气体,为了防止多余Cl2污染空气,可以在D处用如图装置进行尾气处理,请画出装置示意图并标明所加试剂,用离子方程式表示该原理
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐1】实验室制取并收集氯气的装置如图所示,请回答下列问题
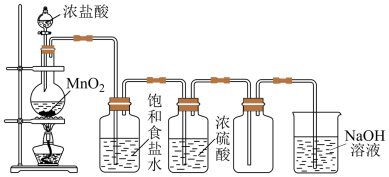
(1)气体发生装置中进行的反应化学方程式是______ 。
(2)在装置中:①饱和食盐水的作用是______ ,②浓硫酸的作用是______ 。
(3)化学实验中检验是否有 产生常用湿润的淀粉
产生常用湿润的淀粉 试纸
试纸 如果有
如果有 产生,可观察到的现象是
产生,可观察到的现象是______ 。
(4)写出尾气吸收装置中进行的反应的离子方程式______ 。

(1)气体发生装置中进行的反应化学方程式是
(2)在装置中:①饱和食盐水的作用是
(3)化学实验中检验是否有
 产生常用湿润的淀粉
产生常用湿润的淀粉 试纸
试纸 如果有
如果有 产生,可观察到的现象是
产生,可观察到的现象是(4)写出尾气吸收装置中进行的反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐2】实验室制取并收集氯气的装置如图所示,请回答下列问题
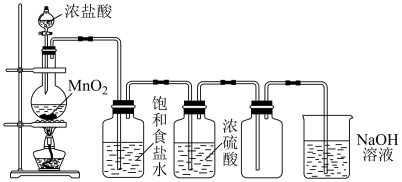
(1)气体发生装置中进行的反应化学方程式是____________ 。
(2)在装置中:①饱和食盐水的作用是____________ ,②浓硫酸的作用是____________ 。
(3)化学实验中不能用 与单质直接化合生成的是下列物质中是__________。
与单质直接化合生成的是下列物质中是__________。
(4) 溶液的作用
溶液的作用____________ ,并写出反应的离子方程式____________ 。

(1)气体发生装置中进行的反应化学方程式是
(2)在装置中:①饱和食盐水的作用是
(3)化学实验中不能用
 与单质直接化合生成的是下列物质中是__________。
与单质直接化合生成的是下列物质中是__________。A. | B. | C. | D. |
 溶液的作用
溶液的作用
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】氯气在工业生产中有重要的用途。某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
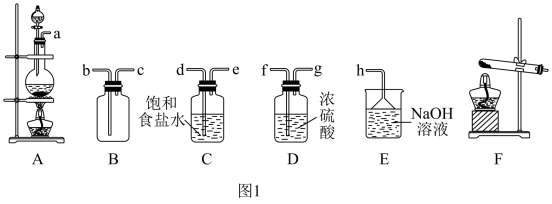
(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
①写出实验室制氯气的化学反应方程式:___________ ;浓盐酸起酸性作用和还原剂作用的质量之比为___________ 。
②选择装置,将各仪器按先后顺序连接起来,应该是a接___________,___________接___________,___________接___________,___________接h。(用导管口处的字母表示)___________
(2)E装置吸收氯气,可得漂白液的有效成分:___________ (填化学式);若将氯气通入冷的石灰乳中,可得漂白粉,写出反应方程式:___________ 。
(3)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。
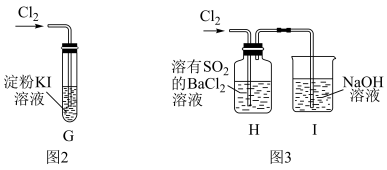
①G中的现象是___________ ,原因是___________ (用化学方程式表示)。
②H中的现象是___________ 。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
①写出实验室制氯气的化学反应方程式:
②选择装置,将各仪器按先后顺序连接起来,应该是a接___________,___________接___________,___________接___________,___________接h。(用导管口处的字母表示)
(2)E装置吸收氯气,可得漂白液的有效成分:
(3)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中的现象是
②H中的现象是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐1】1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。
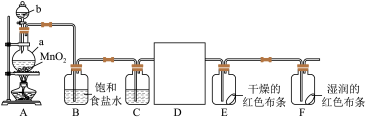
(1)仪器b的名称为___________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为___________ 。
(2)仪器a中发生反应的化学方程式为___________ 。根据氯气的性质D中的收集装置可以选择___________ (填序号)。
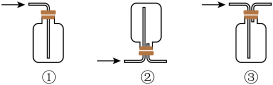
(3)下列有关该实验的说法中不正确 的是___________(填字母)。
(4)实验室还可用等物质的量的 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为___________ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中
| A.将b中溶液换为稀盐酸,同样可以产生氯气 |
| B.C中试剂是浓硫酸,目的是干燥氯气 |
| C.F中红色布条褪色,证明氯气具有漂白性 |
| D.可用湿润的淀粉碘化钾试纸检验氯气是否收集满 |
(4)实验室还可用等物质的量的
 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
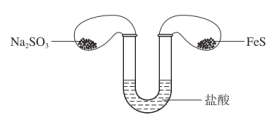
【推荐2】如下图所示,将两只气球中少量的 和
和 粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式_______ 。
 和
和 粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐3】科学探究可以培养学生良好的科学思维。某兴趣小组进行了金属燃烧实验:
试回答下列问题:
(1)进行1、2实验的目的是为研究铝和氧气反应的剧烈程度是否与氧气的____ 有关。
(2)某同学分析2、3实验后就得出如下结论:不同金属的活动性是不同的。其他同学认为这个结论不可靠,你认为他们的理由是____ 。
(3)小组同学认为镁和铝的活动性可以通过与氧气反应的剧烈程度来比较,你认为还可以通过____ 的实验来比较。
(4)在实验1中,有同学用细针去刺破液态铝外面的薄膜,观察到里面的液态铝依然没有流出来。实验后,同学们查阅资料获知该薄膜是氧化铝,其熔点明显高于酒精灯火焰的温度,由此推断,刺破薄膜后液态铝会迅速和____ 反应又会形成致密氧化膜,所以液态铝不会流出来。
| 实验 | 1 | 2 | 3 |
| 步骤 | 将一片铝箔在空气中用酒精灯加热 | 将另一片相同铝箔伸入到充满氧气的集气瓶中,引燃 | 将一段镁条在空气中用酒精灯加热 |
| 现象 | 铝箔不燃烧,熔化后也不滴下,外面立即形成一层薄膜 | 铝箔剧烈燃烧,发出耀眼白光 | 镁条剧烈燃烧,发出耀眼白光 |
(1)进行1、2实验的目的是为研究铝和氧气反应的剧烈程度是否与氧气的
(2)某同学分析2、3实验后就得出如下结论:不同金属的活动性是不同的。其他同学认为这个结论不可靠,你认为他们的理由是
(3)小组同学认为镁和铝的活动性可以通过与氧气反应的剧烈程度来比较,你认为还可以通过
(4)在实验1中,有同学用细针去刺破液态铝外面的薄膜,观察到里面的液态铝依然没有流出来。实验后,同学们查阅资料获知该薄膜是氧化铝,其熔点明显高于酒精灯火焰的温度,由此推断,刺破薄膜后液态铝会迅速和
您最近一年使用:0次



