草酸亚铁晶体( )是一种浅黄色固体,难溶于水。乙二酸又名草酸,是重要的络合剂、沉淀剂和还原剂。
)是一种浅黄色固体,难溶于水。乙二酸又名草酸,是重要的络合剂、沉淀剂和还原剂。
(1)利用草酸与乙醇制备草酸二乙酯的化学方程式为___________ 。
(2)以 、氨水及草酸制备电池级草酸亚铁晶体(
、氨水及草酸制备电池级草酸亚铁晶体( )的实验流程如下:
)的实验流程如下: 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是___________ 。
②证明“沉淀”已经完全的实验操作和现象是___________ 。
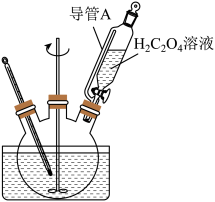
③“转化”在如图所示的装置中进行。导管A的作用是___________ 。转化过程中需不断搅拌的目的是___________ 。___________ 。
⑤测定草酸亚铁晶体( )纯度。
)纯度。
准确称取0.2500g样品于锥形瓶,加入适量的稀硫酸,用0.04500
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液18.00mL。计算样品中
溶液18.00mL。计算样品中 的纯度为
的纯度为___________ (保留三位有效数字)。(写出计算过程)
滴定反应: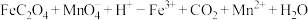 (未配平)。
(未配平)。
 )是一种浅黄色固体,难溶于水。乙二酸又名草酸,是重要的络合剂、沉淀剂和还原剂。
)是一种浅黄色固体,难溶于水。乙二酸又名草酸,是重要的络合剂、沉淀剂和还原剂。(1)利用草酸与乙醇制备草酸二乙酯的化学方程式为
(2)以
 、氨水及草酸制备电池级草酸亚铁晶体(
、氨水及草酸制备电池级草酸亚铁晶体( )的实验流程如下:
)的实验流程如下: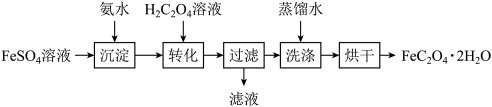
 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是②证明“沉淀”已经完全的实验操作和现象是
③“转化”在如图所示的装置中进行。导管A的作用是
⑤测定草酸亚铁晶体(
 )纯度。
)纯度。准确称取0.2500g样品于锥形瓶,加入适量的稀硫酸,用0.04500

 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液18.00mL。计算样品中
溶液18.00mL。计算样品中 的纯度为
的纯度为滴定反应:
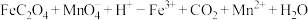 (未配平)。
(未配平)。
22-23高一下·江苏泰州·期末 查看更多[2]
更新时间:2023/06/29 07:07:42
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】(1)分别写出乙醛与银氨溶液、苯酚钠溶液中通入少量CO2反应的离子方程式:__________________________________ 、__________________________________ 。
(2)乙烯是一种重要的化工原料,以乙烯为原料衍生出部分化工产品的反应如下(部分反应条件已略去):请回答下列问题:
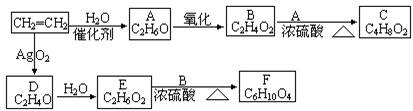
(1)A的化学名称是_____ ;
(2)B和A反应生成C的化学方程式为________ ,该反应的类型为_____________
(3)D(环状化合物)的结构简式为___________ ;
(4)F的结构简式为_____________ ;
(5)D的同分异构体的结构简式为___________ 。
(2)乙烯是一种重要的化工原料,以乙烯为原料衍生出部分化工产品的反应如下(部分反应条件已略去):请回答下列问题:

(1)A的化学名称是
(2)B和A反应生成C的化学方程式为
(3)D(环状化合物)的结构简式为
(4)F的结构简式为
(5)D的同分异构体的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】乙烯是重要的化工原料,根据所学知识用乙烯制备乙酸乙酯,无机试剂自选。
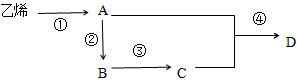
问题:(1)写出上述过程中②④两步的化学方程式,②________________ ,④_______________________ 。
(2)分别写出D在酸性条件和碱条件水解的化学方程式,_________________ ,________________________ 。

问题:(1)写出上述过程中②④两步的化学方程式,②
(2)分别写出D在酸性条件和碱条件水解的化学方程式,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有X、Y、Z三种元素,X是有机化合物中必含有的元素,Y是地壳里含量最高的元素,Z是质量最轻的元素,X与Y能结合成两种化合物A和B,A可以燃烧,B不可燃烧也不能支持燃烧,X与Z结合的化合物C是最简单的烃。由X、Y与Z三种元素组成的化合物D常用作实验室加热的燃料。
(1)试判断X、Y、Z各是什么元素(填名称)。X______ 、Y________ 、Z________ 。
(2)试判断A、B、C、D各是什么物质(填化学式)。
A___________ 、B___________ 、C____________ 、D___________ 。
(3)写出化合物A与Fe2O3反应的化学方程式____________________ 。
(4)已知常温下8g C在O2中完全燃烧放出444.8kJ的热量,试写出化合物C完全燃烧的热化学方程式:___________________________ 。
(5)欲用化合物D与Na反应制取并收集1g H2,需要D的质量_________ g;并写出化合物D与 反应的化学方程式:
反应的化学方程式:___________________ 。
(1)试判断X、Y、Z各是什么元素(填名称)。X
(2)试判断A、B、C、D各是什么物质(填化学式)。
A
(3)写出化合物A与Fe2O3反应的化学方程式
(4)已知常温下8g C在O2中完全燃烧放出444.8kJ的热量,试写出化合物C完全燃烧的热化学方程式:
(5)欲用化合物D与Na反应制取并收集1g H2,需要D的质量
 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锆及其化合物作为新材料,具有相当重要的意义。氧氯化锆(ZrOCl2)是制备锆系列材料的一种重要中间产品,用锆英砂(主要成分ZrSiO4)制备水合氧氯化锆有多种方法,目前使用较多的是“一酸一碱法”,其主要流程如图:
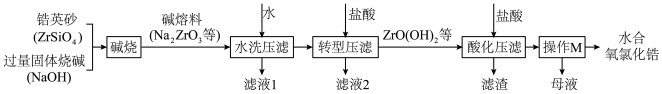
已知:①Na2ZrO3在强碱性的介质中不溶解或水解;②硅酸和原硅酸都具有吸附性。
回答下列问题:
(1)“碱烧”过程中生成“碱熔料”的化学方程式为___ 。
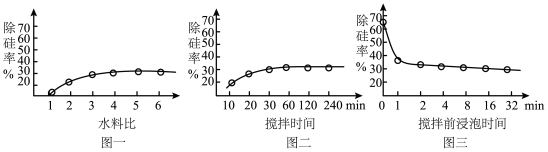
(2)“水洗压滤”工艺可以将30~70%的硅除去,如图表示的是各种工艺变化对水洗除硅率的影响,则为了提高除硅率应采取的措施是___ (任意回答两条即可)。
(3)硅的去除还有一部分是通过上述流程中的___ 工艺实现的,这一部分硅转化成的物质是___ (填化学式)。
(4)水洗压滤的主要目的是除硅,则转型压滤的主要目的是除去___ ,转型压滤过程中生成ZrO(OH)2的离子方程式为___ 。
(5)操作M包括___ 、过滤、洗涤、干燥;上述工艺若不加改进,锆的损失会比较大,为了减少锆的损失,应该改进的措施是___ 。
(6)称取3.220g产品(水合氧氯化锆),溶于盐酸配制成1000mL溶液,取25mL于锥形瓶中,加热至90℃以上,并滴入2滴二甲酚橙指示剂,趁热用0.0125mol·L-1EDTA标准溶液滴定,当溶液由红色变为黄色且半分钟不褪色时,消耗EDTA溶液20mL。计算水合氧氯化锆的化学式为___ (EDTA与ZrO2+在上述条件下以1:1比例反应)。

已知:①Na2ZrO3在强碱性的介质中不溶解或水解;②硅酸和原硅酸都具有吸附性。
回答下列问题:
(1)“碱烧”过程中生成“碱熔料”的化学方程式为
(2)“水洗压滤”工艺可以将30~70%的硅除去,如图表示的是各种工艺变化对水洗除硅率的影响,则为了提高除硅率应采取的措施是

(3)硅的去除还有一部分是通过上述流程中的
(4)水洗压滤的主要目的是除硅,则转型压滤的主要目的是除去
(5)操作M包括
(6)称取3.220g产品(水合氧氯化锆),溶于盐酸配制成1000mL溶液,取25mL于锥形瓶中,加热至90℃以上,并滴入2滴二甲酚橙指示剂,趁热用0.0125mol·L-1EDTA标准溶液滴定,当溶液由红色变为黄色且半分钟不褪色时,消耗EDTA溶液20mL。计算水合氧氯化锆的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
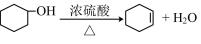
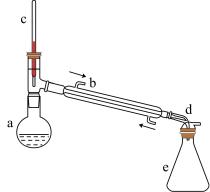
【推荐2】某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省)如下
相关数据如下:
实验步骤:
1、[合成]:在a中加入20.00g纯环己醇及2小块沸石,冷却搅动下缓慢加入10mL浓硫酸。b中通入冷却水后,缓慢加热a,控制馏出物的温度不超过90℃。
2、[提纯]:将反应后粗产物倒入分液漏斗中,依次用少量5% Na2CO3溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去CaCl2。再进行蒸馏最终获得12.30g纯环己烯。
回答下列问题:
(1)装置b的名称是_________________ 。加入沸石的目的是______________ 。
(2)本实验分液所得产物应从_____________ 倒出(填“上口”或“下口”)。
(3)提纯过程中加入Na2CO3溶液的目的是_________________
加入无水CaCl2的作用是_________________________________ 。
(4)本实验所得环己烯的产率是______________________ (产率= ×100%)
×100%)


相关数据如下:
| 相对分子质量 | 密度/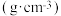 | 沸点/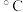 | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
1、[合成]:在a中加入20.00g纯环己醇及2小块沸石,冷却搅动下缓慢加入10mL浓硫酸。b中通入冷却水后,缓慢加热a,控制馏出物的温度不超过90℃。
2、[提纯]:将反应后粗产物倒入分液漏斗中,依次用少量5% Na2CO3溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去CaCl2。再进行蒸馏最终获得12.30g纯环己烯。
回答下列问题:
(1)装置b的名称是
(2)本实验分液所得产物应从
(3)提纯过程中加入Na2CO3溶液的目的是
加入无水CaCl2的作用是
(4)本实验所得环己烯的产率是
 ×100%)
×100%)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组甲、乙两位同学为测定Na2CO3和NaCl混合物中Na2CO3的质量分数,分别进行实验。回答下列问题:
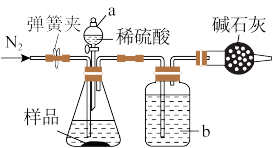
(1)甲同学用上图所示装置进行测定。称取一定质量的待测样品于锥形瓶中,反应前先打开弹簧夹,通入一段时间的N2,然后关闭弹簧夹,接上总质量为m g的干燥管,再打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗a的活塞,打开弹簧夹,再通入一段时间的N2,然后取下干燥管称得其质量为n g。
①洗气瓶b中盛放的液体是_______ (写名称)。
②锥形瓶中发生的反应的离子方程式为:_______ 。
③第一次通入N2的目的是_______ 。第二次通入N2的目的是_______ 。如果没有进行第一次通N2操作,测量的结果将会_______ (填“偏大”“偏小”或“不变”)。
④甲同学设计的该实验装置中存在一不合理之处,会导致测定结果出现误差。如何改进?_______ 。
(2)乙同学用图中所示方法和步骤进行实验:

①如过滤时发现洁净的烧杯中收集到的滤液中仍有浑浊,可能的原因是_______ (任写一条)。
②乙同学测得样品中Na2CO3的质量分数为_______ 。(用含x和y的代数式表示)

(1)甲同学用上图所示装置进行测定。称取一定质量的待测样品于锥形瓶中,反应前先打开弹簧夹,通入一段时间的N2,然后关闭弹簧夹,接上总质量为m g的干燥管,再打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗a的活塞,打开弹簧夹,再通入一段时间的N2,然后取下干燥管称得其质量为n g。
①洗气瓶b中盛放的液体是
②锥形瓶中发生的反应的离子方程式为:
③第一次通入N2的目的是
④甲同学设计的该实验装置中存在一不合理之处,会导致测定结果出现误差。如何改进?
(2)乙同学用图中所示方法和步骤进行实验:

①如过滤时发现洁净的烧杯中收集到的滤液中仍有浑浊,可能的原因是
②乙同学测得样品中Na2CO3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】从工业含镍的废液(主要含Ni2+,Cu2+,Fe2+,Ca2+,Zn2+等)中提纯得到硫酸镍晶体并回收胆矾晶体,某课题小组设计了图流程:
(1)基态Ni2+的价层电子排布式为_______ 。
(2)“滤渣”在空气中焙烧产生一种气体,其化学式为_______ 。
(3)请写出向“溶液1”中依次加入 、
、 的离子方程式
的离子方程式_______ 。
(4)若“溶液2”中 的浓度为0.01mol/L,取等体积的
的浓度为0.01mol/L,取等体积的 溶液与该溶液混合,要使反应结束时
溶液与该溶液混合,要使反应结束时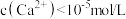 ,则所加
,则所加 溶液的浓度至少为
溶液的浓度至少为_______  。[已知室温下
。[已知室温下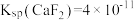 ]
]
(5)室温下选择萃取剂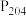 (二乙基已基磷酸,用HR表示),其萃取原理为(
(二乙基已基磷酸,用HR表示),其萃取原理为( ,试剂a为
,试剂a为_______ (填化学式);若溶液3加萃取剂前pH=3,c(Zn2+)=0.011mol/L,多次萃取后水相中c(H+)为1.3×10-2mol/L,则锌的萃取率为_______ %(结果保留一位小数,溶液体积变化忽略不计)。溶液pH对几种离子的萃取率的影响如图,萃取锌时,控制pH的范围为3~4原因是_______ 。
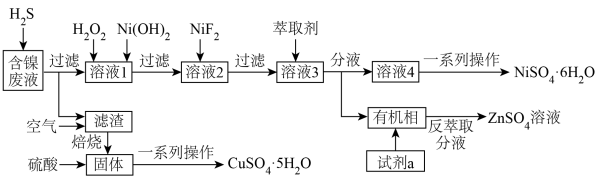
| 金属离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 4.2 | 6.3 | 1.5 | 11.8 | 6.2 | 6.9 |
| 沉淀完全的pH | 6.7 | 8.3 | 2.8 | 13.8 | 8.2 | 8.9 |
(1)基态Ni2+的价层电子排布式为
(2)“滤渣”在空气中焙烧产生一种气体,其化学式为
(3)请写出向“溶液1”中依次加入
 、
、 的离子方程式
的离子方程式(4)若“溶液2”中
 的浓度为0.01mol/L,取等体积的
的浓度为0.01mol/L,取等体积的 溶液与该溶液混合,要使反应结束时
溶液与该溶液混合,要使反应结束时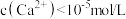 ,则所加
,则所加 溶液的浓度至少为
溶液的浓度至少为 。[已知室温下
。[已知室温下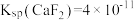 ]
](5)室温下选择萃取剂
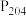 (二乙基已基磷酸,用HR表示),其萃取原理为(
(二乙基已基磷酸,用HR表示),其萃取原理为( ,试剂a为
,试剂a为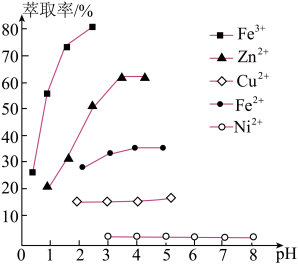
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】环己烯是重要的化工原料。其实验室制备流程如下:
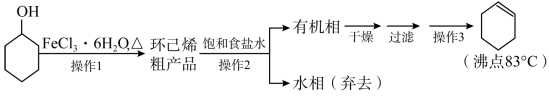
回答下列问题:
I.环己烯的制备与提纯
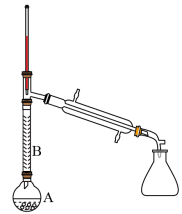
(1)操作1的装置如图所示(加热和夹持装置已略去)。
仪器B的作用为__________________________________________ 。
(2)操作2用到的玻璃仪器是____________________________ 。
(3)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,_________________ ,弃去前馏分,收集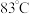 的馏分。
的馏分。

回答下列问题:

I.环己烯的制备与提纯
(1)操作1的装置如图所示(加热和夹持装置已略去)。
仪器B的作用为
(2)操作2用到的玻璃仪器是
(3)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,
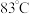 的馏分。
的馏分。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀,而被广泛用作高新科技材料,并被誉为“未来金属”,但在高温时钛化合能力极强,可以与氧、碳、氮及其他元素化合。以钛铁矿(主要成分 ,钛酸亚铁)为主要原料冶炼金属钛,同时获得副产品甲的工业生产流程如下:
,钛酸亚铁)为主要原料冶炼金属钛,同时获得副产品甲的工业生产流程如下:
(1)为使①反应进行得更充分,可采取的措施是___________ (写出两种);已知反应①钛铁矿和浓 反应的产物之一是
反应的产物之一是 ,写出该反应的化学方程式:
,写出该反应的化学方程式:____________ 。
(2)写出上述反应②的化学方程式:_____________ 。
(3)反应④要在氩气氛围中进行的理由是___________ ,最终所得到的金属钛中会混有少量杂质,可加入_____________ 溶解后除去。
(4)工业上用电解熔融的氯化镁制取镁单质,该反应的化学方程式为__________ 。
(5)如果取钛铁矿m吨,杂质的百分含量为w,最终生产出钛n吨(不考虑损耗),则m、n、w三者之间的数学关系是_____________ (已知Ti的相对原子质量为48)。
 ,钛酸亚铁)为主要原料冶炼金属钛,同时获得副产品甲的工业生产流程如下:
,钛酸亚铁)为主要原料冶炼金属钛,同时获得副产品甲的工业生产流程如下: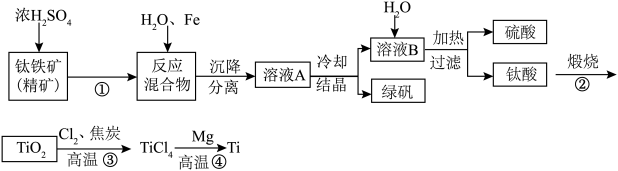
(1)为使①反应进行得更充分,可采取的措施是
 反应的产物之一是
反应的产物之一是 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)写出上述反应②的化学方程式:
(3)反应④要在氩气氛围中进行的理由是
(4)工业上用电解熔融的氯化镁制取镁单质,该反应的化学方程式为
(5)如果取钛铁矿m吨,杂质的百分含量为w,最终生产出钛n吨(不考虑损耗),则m、n、w三者之间的数学关系是
您最近一年使用:0次



