元素周期律是对元素性质的规律性总结,元素周期表是这种规律的呈现形式。利用元素周期律可以推测一些未知元素可能的性质。根据你所学的周期律,回答下列问题:
(1)元素周期表有几个周期,几个主族。正确选项是
(2)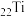 被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
(3)元素周期表中,第三电子层有一个未成对电子的元素有___________种(填序号)。
(1)元素周期表有几个周期,几个主族。正确选项是
| A.6,7 | B.7,7 | C.7,18 | D.7,14 |
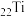 被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
被誉为21世纪明星金属,其最外层电子数为___________(填序号)。| A.1个 | B.2个 | C.3个 | D.5个 |
| A.2 | B.3 | C.4 | D.5 |
22-23高二下·上海青浦·期末 查看更多[3]
上海市青浦高级中学2022-2023学年高二下学期期末考试化学试题(已下线)1.2.1 原子结构与元素周期表(提高)(已下线)专题01 原子结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)
更新时间:2023-07-01 21:23:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,如图是元素周期表的一部分,回答下列问题:
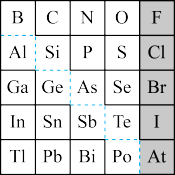
(1)元素Ga在元素周期表中的位置为:___ 。
(2)Sn的最高正价为___ ,Cl的最高价氧化物对应水化物的化学式为___ 。
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是___ 。(写化学式)
②原子半径比较:N___ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是
②原子半径比较:N
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分:
请回答下列问题:
(1)Z元素在周期表中的位置为________________ 。
(2)表中元素原子半径最大的是(写元素符号)________________ 。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是________ (填序号)。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol·L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为______________________________ ,生成硫酸铜物质的量为_______________________ 。
| 碳 | 氮 | Y | |
| X | 硫 | Z |
请回答下列问题:
(1)Z元素在周期表中的位置为
(2)表中元素原子半径最大的是(写元素符号)
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol·L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列为元素周期表中的一部分:

已知:⑤的氢化物常温下为气体,该气体可使湿润的红色石蕊试纸变蓝。
用化学式或元素符号回答下列问题:
(1) ④在周期表中的位置_______ 。
(2) ①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为_________ 。
(3) ①②⑥的简单离子半径由大到小的顺序是___________ 。(填离子符号)
(4) 用一个化学方程式证明Cl元素与⑦非金属性的强弱:____________ 。
(5) ①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为______ 。
(6) ⑥、⑦分别形成的氢化物沸点高的是_______ (填化学式)。原因是_______ 。
(7) ①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为_________ 。

已知:⑤的氢化物常温下为气体,该气体可使湿润的红色石蕊试纸变蓝。
用化学式或元素符号回答下列问题:
(1) ④在周期表中的位置
(2) ①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为
(3) ①②⑥的简单离子半径由大到小的顺序是
(4) 用一个化学方程式证明Cl元素与⑦非金属性的强弱:
(5) ①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为
(6) ⑥、⑦分别形成的氢化物沸点高的是
(7) ①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】近年来,我国航空航天事业成果显著,航空航天材料技术快速发展。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。基态钛原子的价层电子排布图为________ 。
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,基态镓原子电子占据最高能级的电子云轮廓图为____ 形。
(3)“C919”飞机机身使用复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的能量最低状态的是________ (填字母)。
A. B.
B.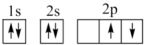
C. D.
D.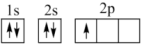
②氧原子的基态原子核外有________ 个未成对电子。
(4)下面是我们熟悉的物质:① ②金刚石 ③NaBr ④
②金刚石 ③NaBr ④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧Ne ⑨
⑧Ne ⑨ ⑩NaOH。这些物质中,只含共价键的是
⑩NaOH。这些物质中,只含共价键的是________ ;只含离子键的是________ ;不存在化学键的是________ ;属于共价化合物的是________ (填序号)
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。基态钛原子的价层电子排布图为
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,基态镓原子电子占据最高能级的电子云轮廓图为
(3)“C919”飞机机身使用复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的能量最低状态的是
A.
 B.
B.
C.
 D.
D.
②氧原子的基态原子核外有
(4)下面是我们熟悉的物质:①
 ②金刚石 ③NaBr ④
②金刚石 ③NaBr ④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧Ne ⑨
⑧Ne ⑨ ⑩NaOH。这些物质中,只含共价键的是
⑩NaOH。这些物质中,只含共价键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空:
(1)Si的价电子层的电子排布式为_____ 。
(2)基态硫原子价电子排布式为_____ 。
(3)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是_____ (填离子符号)。
(4)基态硅原子最外层的电子排布图为_____ 。
(1)Si的价电子层的电子排布式为
(2)基态硫原子价电子排布式为
(3)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
(4)基态硅原子最外层的电子排布图为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图为周期表中部分元素某种性质(X值)随原子序数变化的关系。___ (填元素符号)。
(2)同主族内不同元素的X值变化的特点是___ ;同周期内,随着原子序数的增大,X值的变化总趋势是___ 。周期表中X值的这种变化特点体现了元素性质的___ 变化规律。
(3)X值较小的元素集中在元素周期表的___ (填序号,下同)。
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是___ 。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱

(2)同主族内不同元素的X值变化的特点是
(3)X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近一年使用:0次



